
【题目】向浓度相等、体积均为100 mL的A、B两份NaOH溶液中,分别通入一定量的CO2后,逐滴加入0.1 mol/L的盐酸,产生CO2的体积(标准状况)与所加盐酸的体积关系如图所示。
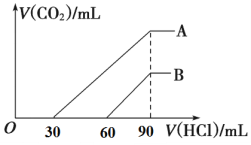
(1)A曲线表明,原溶液通入CO2 ________mL(标准状况)。
(2)B曲线表明,原溶液通入CO2后,所得溶液中溶质的物质的量之比为__________。
(3)原NaOH溶液的物质的量浓度为__________。
【答案】134.4mL 1:1 0.09mol/L
【解析】
氢氧化钠中通入二氧化碳反应为NaOH+CO2= Na2CO3+H2O、或NaOH+CO2= NaHCO3,可能的成分可能为氢氧化钠和碳酸钠,或碳酸钠,或碳酸钠和碳酸氢钠,或碳酸氢钠。然后向溶液中加入盐酸,可能存在的反应为:NaOH+HCl=NaCl+H2O; Na2CO3+HCl=NaCl+NaHCO3;NaHCO3+HCl=NaCl+H2O+CO2↑。分析若只含有碳酸钠,则前后两个阶段消耗的盐酸的量相等,若前者消耗盐酸的量多,则溶液成分为氢氧化钠和碳酸钠,若后者消耗的盐酸的量多,则溶质的成分为碳酸钠和碳酸氢钠。所以A为碳酸钠和碳酸氢钠,B为氢氧化钠和碳酸钠。
(1)(1)根据A曲线中30-90阶段中,计算碳酸氢钠的物质的量为0.1 mol/L×(90-30)×10-3 L =0.006mol,则二氧化碳的物质的量为0.006mol,标况下体积为0.006mol×22.4L/ mol =0.1344L=134.4mL。
(2)B曲线分析,60~90mL盐酸即0.003molHCl和碳酸氢钠反应NaHCO3+HCl=NaCl+H2O+CO2↑,所以n(NaHCO3)=0.003mol,而碳酸氢钠又是由碳酸钠和盐酸生成的,Na2CO3+HCl=NaCl+NaHCO3,所以n(Na2CO3)=0.003mol,碳酸钠消耗HCl0.003mol,即30mL。0~60mL盐酸即0.006molHCl和NaOH中和后和碳酸钠反应,所以和NaOH反应的HCl为0.006-0.003=0.003mol,所以n(NaOH)=0.003mol。故氢氧化钠和碳酸钠的物质的量比为0.003:0.003=1:1。
(3)曲线中盐酸的体积为90mL时气体达到最大值,此时溶液为氯化钠,根据钠和氯元素的关系分析,氢氧化钠和盐酸的物质的量相等,即0.1mol/L×0.09L=c(NaOH)×0.1L。解得c(NaOH)=0.09mol/L。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】设NA为阿伏伽德罗常数的值。下列说法正确的是
A.5NH4NO3 ![]() 2HNO3+4N2↑+9H2O反应中,生成28 g N2,转移的电子数目为3.75NA
2HNO3+4N2↑+9H2O反应中,生成28 g N2,转移的电子数目为3.75NA
B.室温下,1 L pH=13的NaOH溶液中,由水电离的OH- 数目为0.1NA
C.氢氧燃料电池正极消耗22.4 L(标准状况)气体时,电路中通过的电子数目为2NA
D.高温下,0.2 mol Fe与足量水蒸气反应,生成的H2分子数目为0.3 NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有下列几个反应:①向NaAlO2溶液中滴加盐酸;②向盐酸和AlCl3的混合溶液中滴加NaOH溶液;③向NaOH溶液中滴加AlCl3溶液;
⑴符合反应①的图象是______,符合反应②的图象是_____,符合反应③的图象是____;

(2)写出③步骤中的二个离子方程式__________________、________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在化学反应中,能引发化学反应的分子间碰撞称之为有效碰撞,这些分子称为活化分子。使普通分子变成活化分子所需提供的最低能量叫活化能,其单位用kJmol-1表示。请认真观察下图,然后回答问题。
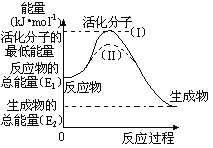
(1)图中反应是______(填“吸热”或“放热”)反应,该反应_______(填“需要”或“不需要”)环境先提供能量,该反应的△H=_________(用含E1、E2的代数式表示)。
(2)已知热化学方程式:H2(g)+1/2O2(g) =H2O(g) △H= -241.8kJmol-1,该反应的活化能为167.2 kJmol-1,则其逆反应的活化能为__________。
(3)对于同一反应,图中虚线(Ⅱ)与实线(I)相比,活化能_________,单位体积内活化分子的百分数________,因此反应速率_________,(前面的三个空填“增大”“减小”“不变”)你认为最可能的原因是_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图为蔗糖酶作用机理示意图,下列说法正确的是( )

A.该示意图说明酶具有高效性
B.图示过程能够保证酶保持较高的催化活性
C.一分子蔗糖可以水解为2分子葡萄糖
D.蔗糖酶不能催化麦芽糖水解是因为它们不能结合形成酶﹣底物复合物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对下列实验现象及其解释不正确的是( )
A.金属钠在Cl2中燃烧产生白烟,这是因为产生的NaCl固体颗粒分散到空气中所致
B.把烧红的铁丝放在氧气中,发出耀眼白光,产生黑色固体,这是因为该反应放热多,生成的Fe3O4为黑色
C.单质Mg、Al与O2反应,条件不同,可能产生不同的产物
D.镁带在空气中点燃发出耀眼光芒,常用于制照明弹,主要发生反应:2Mg+O2![]() 2MgO,其中,Mg作还原剂
2MgO,其中,Mg作还原剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于“同位素”、“同素异形体”、“同系物”、“同分异构体”的说法合理的是 ( )
A. 同位素是指质量数相同,中子数不同的同种元素的不同原子
B. 同素异形体是指由同种元素形成的不同单质
C. 互为同分异构体的两种物质分子式相同,化学性质一定相似
D. 具有相同的通式,组成上相差若干个“![]() ”原子团的有机物一定互为同系物
”原子团的有机物一定互为同系物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图中分别是两种烃的结构模型:
A.  B.
B. 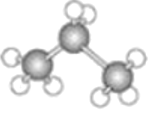
请回答下列问题:
(1)A、B两种模型分别是有机物的____________模型和____________模型。
(2)模型A可以表示分子中原子的相对位置和相对大小,以下物质的空间结构可以用模型A表示的是______。
A.![]() B.
B.![]() C.
C.![]() D.
D.![]()
(3)已知:模型B表示某烃M的结构。该烃与氯气反应生成另一有机物N,且M和N的式量相差34.5。
①写出M的结构简式:__________________。
②N的可能结构有______种。若N的分子中有2种不同化学环境的氢原子,则该过程的化学方程式是______________________________,此反应的类型是__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有下列仪器:

(1)海水蒸馏是由海水获得淡水的常用方法之一,在实验室里组成一套蒸馏装置肯定 需要上述仪器中的一部分,按照实验仪器从下到上、从左到右的顺序,依次是__________ (填序号);仪器⑤的冷凝水应从________(填“a”或“b”)口进入。
(2)海带等藻类物质经过处理后,可以得到碘水,欲从碘水中提取碘,需要上述仪器 中的______(填序号),该仪器名称为__________,向该碘水中加入四氯化碳以提取碘 单质的实验操作叫做_________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com