
亚氯酸钠(NaClO2)是一种重要的含氯消毒剂,主要用于水的消毒以及砂糖、油脂的漂白与杀菌。以下是过氧化氢法生产亚氯酸钠的工艺流程图:
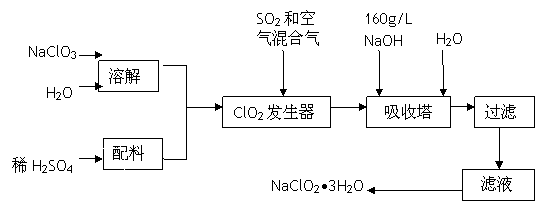
已知:①NaClO2的溶解度随温度升高而增大,适当条件下可结晶析出NaClO2•3H2O。
②纯ClO2易分解爆炸,一般用稀有气体或空气稀释到10%以下安全。
③160 g/L NaOH溶液是指160 gNaOH固体溶于水所得溶液的体积为1L。
(1) 160 g/L NaOH溶液的物质的量浓度为 。
(2)发生器中鼓入空气的作用可能是 (选填序号)。
a.将SO2氧化成SO3,增强酸性; b.稀释ClO2以防止爆炸;
c.将NaClO3氧化成ClO2
(3)吸收塔内的反应的化学方程式为 。
吸收塔的温度不能超过20℃,其目的是 。
(4)在碱性溶液中NaClO2比较稳定,所以吸收塔中应维持NaOH稍过量,判断NaOH是否过量的简单实验方法是 。
(5)吸收塔中为防止NaClO2被还原成NaCl,所用还原剂的还原性应适中。除H2O2
外,还可以选择的还原剂是 (选填序号)。
a.Na2O2 b.Na2S c.FeCl2
(6) 从滤液中得到NaClO2•3H2O粗晶体的实验操作依次是 (选填序号)。
a.蒸馏 b.蒸发 c.灼烧 d.过滤 e.冷却结晶
要得到更纯的NaClO2•3H2O晶体必须进行的操作是 (填操作名称)。
 快乐5加2金卷系列答案
快乐5加2金卷系列答案科目:高中化学 来源: 题型:
在Na2SO4、NaCl、NaOH的混合溶液中,含有Na+、SO42-、OH-的个数比是8:1:2,则溶液中Na2SO4、NaCl、NaOH的物质的量之比是( )
A.1:1:1 B.1:4:2 C.1:2:4 D.1:3:2
查看答案和解析>>
科目:高中化学 来源: 题型:
CO是对环境影响较大的气体,对它的合理控制和治理是优化我们生存环境的有效途径。
(1)工业上用CO和H2做原料可以合成甲醇,作为液体燃料。已知:
① 2H2(g)+CO(g)+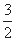 O2(g) = 2H2O(g)+CO2(g) ΔH1= -594.1kJ/mol
O2(g) = 2H2O(g)+CO2(g) ΔH1= -594.1kJ/mol
② 2CH3OH(l)+3O2(g) = 4H2O(g)+2CO2(g) ΔH2 = -1452kJ/mol
请写出用CO(g)和H2(g)合成1mol液态甲醇的热化学反应方程式:___________。
(2)一定温度下,在容积为2L的恒容容器中加入3mol H2和2mol CO,当反应2H2(g)+CO(g)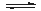 CH3OH(g)达到平衡时,测得容器内的压强是反应前压强的
CH3OH(g)达到平衡时,测得容器内的压强是反应前压强的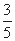 ,据此计算该温度下反应的平衡常数(写过程)。
,据此计算该温度下反应的平衡常数(写过程)。
(3)在恒温恒容的条件下,向(2)达到平衡的容器中再通入CO(g)和CH3OH(g),使得CO(g)和CH3OH(g)浓度均为原平衡的2倍,则平衡 。
A.向正反应方向移动 B.向逆反应方向移动
C.不移动 D.无法判断是否移动
查看答案和解析>>
科目:高中化学 来源: 题型:
已知下列热化学方程式: ( )
2H2(g)+O2(g)===2H2O(g);ΔH=-483.6 kJ/mol
H2(g)+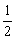 O2(g)===H2O(g);ΔH=-241.8 kJ/mol
O2(g)===H2O(g);ΔH=-241.8 kJ/mol
H2(g)+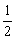 O2(g)===H2O(l);ΔH=-285.8 kJ/mol 则氢气的燃烧热为
O2(g)===H2O(l);ΔH=-285.8 kJ/mol 则氢气的燃烧热为
A.438.6 kJ/mol B.241.8 kJ/mol C.285.8 kJ/mol D.无法确定
查看答案和解析>>
科目:高中化学 来源: 题型:
下列解释物质用途或现象的反应方程式不准确的是
A.硫酸型酸雨的形成会涉及反应:2H2SO3+O2 2H2SO4
2H2SO4
B.热的纯碱溶液可以清洗油污的原因:CO32— +2H2O
 H2CO3+2OH¯
H2CO3+2OH¯
C.盛放NaOH溶液的试剂瓶不能用玻璃塞:SiO2+2OH¯=SiO32—+H2O
D.成分为盐酸的洁厕灵与84消毒液混合使用易中毒:Cl-+ ClO-+2H+= Cl2↑+ H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
有机化合物J是治疗心脏病药物的一种中间体,分子结构中含有3个六元环。其中一种合成路线如下:
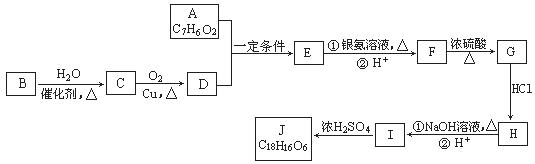
已知:
①A既能发生银镜反应,又能与FeCl3溶液发生显色反应,其核磁共振氢谱显示有4种氢,且峰面积之比为1︰2︰2︰1。
②有机物B是一种重要的石油化工产品,其产量可用来衡量国家的石油化工发展水平。
③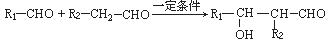
回答以下问题:
(1)A中含有的官能团名称是 。
(2)写出有机反应类型B→C ,F→G ,I→J 。
(3)写出F生成G的化学方程式 。
(4)写出J的结构简式 。
(5)E的同分异构体有多种,写出所有符合以下要求的E的同分异构体的结构简式
。
FeCl3溶液发生显色反应 ②能发生银镜反应 ③苯环上只有两个对位取代基 ④能发生水解反应。
查看答案和解析>>
科目:高中化学 来源: 题型:
甲醇质子交换膜燃料电池中将甲醇蒸气转化为氢气的两种反应原理是
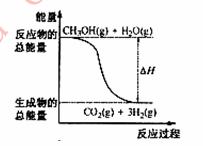
①CH3OH(g)+H2O(g)=CO2(g)+3H2(g) ΔH= + 49.0 kJ/mol
②CH3OH(g)+1/2O2(g)=CO2(g)+2H2(g) ΔH=-192.9 kJ/mol
下列说法正确的是( )
A.CH3OH的燃烧热为192.9 kJ/mol
B.反应①中的能量变化如右图所示
C.CH3OH转变成H2的过程一定要吸收能量
D.根据②推知:CH3OH(l)+1/2O2(g)=CO2(g)+2H2(g) ΔH > -192.9kJ/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
在1 000 K时,已知反应Ni(s)+H2O(g) 
 NiO(s)+H2(g)的平衡常数
NiO(s)+H2(g)的平衡常数
K=0.005 9。当水蒸气和氢气的物质的量浓度相等时,此反应( )
A.已达平衡状态 B.未达平衡状态,反应正向进行
C.未达平衡状态,反应逆向进行 D.无法确定
查看答案和解析>>
科目:高中化学 来源: 题型:
可逆反应A+B(s)⇌C达到平衡后,无论加压或降温,B的转化率都增大,则下列结论正确的是( )
|
| A. | A为固体,C为气体,正反应为放热反应 |
|
| B. | A、C均为气体,正反应为吸热反应 |
|
| C. | A为气体,C为固体,正反应为吸热反应 |
|
| D. | A为气体,C为固体,正反应为放热反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com