
可逆反应A+B(s)⇌C达到平衡后,无论加压或降温,B的转化率都增大,则下列结论正确的是( )
|
| A. | A为固体,C为气体,正反应为放热反应 |
|
| B. | A、C均为气体,正反应为吸热反应 |
|
| C. | A为气体,C为固体,正反应为吸热反应 |
|
| D. | A为气体,C为固体,正反应为放热反应 |
| 化学平衡建立的过程.. | |
| 专题: | 化学平衡专题. |
| 分析: | 加压或降温平衡,B的转化率都增大,平衡都向正反应方向移动,反应物气体的化学计量数之和大于生成物气体的化学计量数之和,且正反应为放热反应,以此解答该题. |
| 解答: | 解:加压或降温平衡,B的转化率都增大,平衡都向正反应方向移动,反应物气体的化学计量数之和大于生成物气体的化学计量数之和,且正反应为放热反应, 已知可逆反应A+B(s)⇌C,反应要满足反应物气体的化学计量数之和大于生成物气体的化学计量数之和,则A为气体,C为固体, 故选:D. |
| 点评: | 本题考查化学平衡的影响因素,题目难度不大,注意影响化学平衡的因素以及外界条件变化时平衡移动的方向 |


科目:高中化学 来源: 题型:
亚氯酸钠(NaClO2)是一种重要的含氯消毒剂,主要用于水的消毒以及砂糖、油脂的漂白与杀菌。以下是过氧化氢法生产亚氯酸钠的工艺流程图:
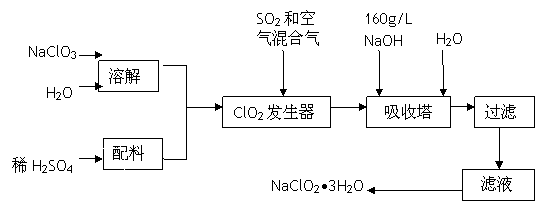
已知:①NaClO2的溶解度随温度升高而增大,适当条件下可结晶析出NaClO2•3H2O。
②纯ClO2易分解爆炸,一般用稀有气体或空气稀释到10%以下安全。
③160 g/L NaOH溶液是指160 gNaOH固体溶于水所得溶液的体积为1L。
(1) 160 g/L NaOH溶液的物质的量浓度为 。
(2)发生器中鼓入空气的作用可能是 (选填序号)。
a.将SO2氧化成SO3,增强酸性; b.稀释ClO2以防止爆炸;
c.将NaClO3氧化成ClO2
(3)吸收塔内的反应的化学方程式为 。
吸收塔的温度不能超过20℃,其目的是 。
(4)在碱性溶液中NaClO2比较稳定,所以吸收塔中应维持NaOH稍过量,判断NaOH是否过量的简单实验方法是 。
(5)吸收塔中为防止NaClO2被还原成NaCl,所用还原剂的还原性应适中。除H2O2
外,还可以选择的还原剂是 (选填序号)。
a.Na2O2 b.Na2S c.FeCl2
(6) 从滤液中得到NaClO2•3H2O粗晶体的实验操作依次是 (选填序号)。
a.蒸馏 b.蒸发 c.灼烧 d.过滤 e.冷却结晶
要得到更纯的NaClO2•3H2O晶体必须进行的操作是 (填操作名称)。
查看答案和解析>>
科目:高中化学 来源: 题型:
两个体积相同的容器,一个盛有CO,另一个盛有N2和C2H4,在同温同压下两容器内的气体一定具有相同的:①原子总数 ②质子总数 ③分子总数 ④质量( )
A.①② B.②③ C.①③ D.③④
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各表述与示意图一致的是( )

|
| A. | 图①表示N2O4(g)⇌2NO2(g)△H>0,N2O4转化率随温度、时间的变化 |
|
| B. | 图②中曲线表示反应2SO2(g)+O2(g)⇌2SO3(g)△H<0,正、逆反应的平衡常数K随温度的变化 |
|
| C. | 图③表示10 mL0.01 mol/LKMnO4酸性溶液与过量0.1mol/LH2C2O4溶液混合时,n(Mn2+)随时间的变化 |
|
| D. | 图④中a、b曲线分别表示反应CH2=CH2(g)+H2(g)→CH3CH3(g)△H<0,使用和未使用催化剂时,反应过程中的能量变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:
在一个体积固定的密闭容器中加入2 mol A和1 mol B,发生反应:2A(g)+B(g)⇌3C(g)+D(g),达到平衡时C的浓度为a mol/L.若维持容器体积和温度不变,按下列四种配比作为起始物质,达到平衡后,C的浓度仍为a mol/L的是( )
|
| A. | 4mol A+2mol B | B. | 2mol A+1mol B+3mol C+1mol D |
|
| C. | 3mol C+1mol D+1mol B | D. | 3mol C+1mol D |
查看答案和解析>>
科目:高中化学 来源: 题型:
有两只密闭容器A和B,A容器有一个可移动活塞使容器内保持恒压,B容器保持恒容,起始时向两只容器中分别充入等量的体积比为2:1的SO2和O2的混合气体,并使A和B容积相等.在保持400℃条件下使之发生反应:2SO2+O2⇌2SO3 填写下列空白:
(1)达到平衡所需时间A比B 短 ,A中SO2的转化率比B 大 .
(2)达到(1)所述平衡后,若向两容器通入数量不多的等量氩气,A容器的化学平衡移动,B容器的化学平衡 不 移动.
(3)达到(1)所述平衡后,向两容器中通入等量的原反应气体,达到平衡后,A中SO3的体积分数 不变 (增大、减小、不变),B容器中SO3的体积分数 增大 .
查看答案和解析>>
科目:高中化学 来源: 题型:
下列实验操作与预期实验目的或所得实验结论一致的是
| 选项 | 实验操作 | 实验目的或结论 |
| A | 某钾盐溶于盐酸,产生能使澄清石灰水变浑浊的无色无味气体 | 说明该钾盐是K2CO3 |
| B | 向含有少量FeCl3的MgCl2溶液中加入足量Mg(OH)2粉末,搅拌一段时间后过滤 | 除去MgCl2溶液中少量FeCl3 |
| C | 常温下,向饱和Na2CO3溶液中加少量BaSO4粉末,过滤,向洗净的沉淀中加稀盐酸,有气泡产生 | 说明常温下Ksp(BaCO3)<Ksp(BaSO4) |
| D | C2H5OH与浓硫酸170 ℃共热,制得的气体通入酸性KMnO4溶液 | 检验制得气体是否为乙烯 |
查看答案和解析>>
科目:高中化学 来源: 题型:
酸性条件下20mL、0.5mol/L的 KMnO4溶液可将25mL、2mol/L的FeSO4溶液中的 Fe2+氧化为Fe3+,
则KMnO4被还原的产物是( )
A.Mn2O3 B.Mn2+ C.MnO2 D.K2MnO4
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com