
【题目】镁在航空航天、国防工业等领域有广泛应用。某小组利用某工厂废弃物(主要含MgCO3、MgSiO3、Al2O3和Fe2O3)设计回收镁的工艺流程如下:
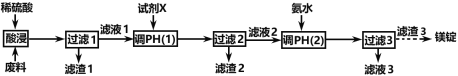
(1)酸浸过程中采用“粉碎废料、加热和搅拌、适当提高稀硫酸的浓度”等措施的目的是_________________________。
为了提高产品纯度,试剂X宜选择(________________)(填代号)。
A.CuO B.MgO C.MgCO3 D.氨水
(2)滤渣1的主要成分是____________:滤渣2的主要成分是____________(填化学式)。
(3)写出生成滤渣3的离子方程式_____________________。
(4)已知:298K,时,Ksp[Al(OH)3]=3.0 × 10-34, Ksp[Fe(OH)3]=4.0 × 10-38,加入试剂X,当Al3+开始沉淀时,溶液中c(Al3+)∕c(Fe3+)=________________。
(5)若废料中镁元素的质量分数为a% ,利用mkg这种废料按上述流程生产,最终回收到质量分数为b%的镁锭wkg,则它的产率为________% 。
(6)参照海水提镁的某些步骤和上述流程图,设计经三步由滤渣3得到镁锭的路线____________。
【答案】提高酸浸速率 BCD H2SiO3 Fe(OH)3、Al(OH)3 Mg2+ + 2NH3H2O = Mg(OH)2↓ + 2NH4+ 7500 100wb∕am 
【解析】
废弃物(主要含MgCO3、MgSiO3、Al2O3和Fe2O3)中加入稀硫酸,反应生成硫酸镁、硫酸铝和硫酸铁,以及二氧化碳和硅酸沉淀,因此过滤后的滤渣1为硅酸沉淀,滤液热中含有硫酸镁、硫酸铝和硫酸铁,根据实验目的,需要除去铁离子和铝离子,因此滤渣3为氢氧化镁,滤液2中含有镁离子,则加入试剂X可以除去铁离子和铝离子,滤渣2中含有Fe(OH)3、Al(OH)3,据此分析解答。
(1) 废弃物(主要含MgCO3、MgSiO3、Al2O3和Fe2O3)中加入稀硫酸,反应生成硫酸镁、硫酸铝和硫酸铁,以及二氧化碳和硅酸沉淀,酸浸过程中采用“粉碎废料、加热和搅拌、适当提高稀硫酸的浓度”等措施可以提高酸浸速率;为了提高产品纯度,不能引入新的杂质金属阳离子,因此试剂X可以选择MgO、MgCO3、氨水,通过可知pH值,除去铁离子和铝离子,故答案为:提高酸浸速率;BCD;
(2)根据上述分析,滤渣1的主要成分是H2SiO3,滤渣2的主要成分是Fe(OH)3、Al(OH)3,故答案为:H2SiO3;Fe(OH)3、Al(OH)3;
(3) 滤渣3为氢氧化镁,生成滤渣3的离子方程式为Mg2+ + 2NH3H2O = Mg(OH)2↓ + 2NH4+,故答案为:Mg2+ + 2NH3H2O = Mg(OH)2↓ + 2NH4+;
(4) 298K时,Ksp[Al(OH)3]=3.0 × 10-34, Ksp[Fe(OH)3]=4.0 × 10-38,当Al3+开始沉淀时,溶液中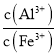 =
=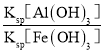 =
=![]() =7500,故答案为:7500;
=7500,故答案为:7500;
(5) mkg这种废料中含有的镁元素的质量为mkg ×a%,质量分数为b%的wkg镁锭中含有镁元素的质量为wkg×b%,则产率=![]() ×100%=
×100%=![]() %,故答案为:
%,故答案为:![]() ;
;
(6)滤渣3为氢氧化镁,可以用足量的盐酸溶解后得到氯化镁溶液,再在氯化氢气氛中蒸发得到氯化镁晶体,最终电解熔融的氯化镁得到镁,因此得到镁锭的路线为![]() ,故答案为:
,故答案为:![]() 。
。


 开心练习课课练与单元检测系列答案
开心练习课课练与单元检测系列答案 开心试卷期末冲刺100分系列答案
开心试卷期末冲刺100分系列答案科目:高中化学 来源: 题型:
【题目】化合物M可用于消毒剂、抗氧化剂、医药中间体。实验室由芳香烃A制备M的一种合成路线如下:

请回答:
(1)B的化学名称为___________;D中官能团的名称为______________________。
(2)由F生成G的反应类型为___________;F的分子式为___________。
(3)由E转化为F的第一步反应的化学方程式为______________________。
(4)M的结构简式为___________。
(5)芳香化合物Q为C的同分异构体,Q能发生银镜反应,其核磁共振氢谱有4组吸收峰。写出符合要求的Q的一种结构简式______________________。
(6)参照上述合成路线和信息,以苯甲酸乙酯和CH3MgBr为原料(无机试剂任选),设计制备 的合成路线_________________________________。
的合成路线_________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】奥运会禁止运动员使用兴奋剂.以下两种兴奋剂的结构分别为:
①利尿酸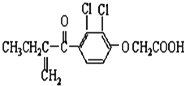 ②兴奋剂X
②兴奋剂X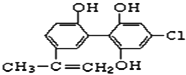
则关于它们的说法中正确的是( )
A.利尿酸分子中有三种含氧官能团,在核磁共振氢谱中共有六个峰
B.1mol兴奋剂X与足量浓溴水反应,最多消耗4molBr2
C.两种兴奋剂均属于芳香烃
D.两种分子中的所有原子均可能共平面
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用下列实验装置(部分夹持装置略去)进行相应的实验,能达到实验目的的是 ( )
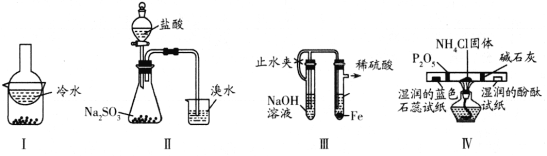
A. 加热装置I中的烧杯分离I2和高锰酸钾固体
B. 用装置II验证二氧化硫的漂白性
C. 用装置III制备氢氧化亚铁沉淀
D. 用装置IV检验氯化铵受热分解生成的两种气体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物M可广泛用于生物医学、海洋工程、日化用品等领域。其合成路线如图:
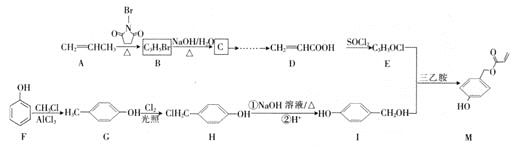
已知:R-COOH![]() R-COCl
R-COCl
回答下列问题:
(1)G的名称为___,D中含氧官能团的名称为___。
(2)M的分子式为___。
(3)F→G的反应类型为___。
(4)E的结构简式为___。
(5)写出B生成C的化学方程式:___。
(6)R为I的同分异构体,R的苯环上含有三个取代基的结构共有___种,写出其中核磁共振氢谱图中峰面积比为3:2:2:1的结构简式:___。
(7)参照本题信息,试写出以1-丁烯为原料制取![]() 的合成路线流程图(无机原料任选)___。合成路线流程图示例如下:
的合成路线流程图(无机原料任选)___。合成路线流程图示例如下:
H2C=CH2![]() CH3CH2Br
CH3CH2Br![]() CH3CH2OH
CH3CH2OH
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有a、b、c、d四个金属电极,有关的实验装置及部分实验现象如下:
实验装置 |
|
|
|
|
部分实验现象 | a极质量减小,b极质量增大 | b极有气体产生,c极无变化 | d极溶解,c极有气体产生 | 电流从a极流向d极 |
由此可判断这四种金属的活动性顺序是( )
A.![]() B.
B.![]() C.
C.![]() D.
D.![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电解KCl和NaNO3溶液可以得到KNO3溶液,电解装置如图所示,下列说法正确的是( )
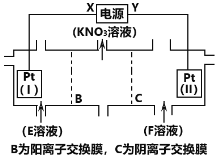
A.X为负极,F溶液为NaNO3溶液
B.电解一段时间,往Pt(I)附近滴入酚酞,溶液变红
C.电解的总反应为2H2O![]() 2H2↑ + O2↑
2H2↑ + O2↑
D.理论上,当得到0.1molKNO3时,Pt(II)上生成标准状况下1.12L气体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知反应2CH3OH(g)=CH3OCH3(g)+H2O(g)在某温度下的平衡常数为400。此温度下,在密闭容器中加入CH3OH,反应到某时刻测得各组分的浓度如下:
物质 | CH3OH | CH3OCH3 | H2O |
浓度/(mol·L-1) | 0.44 | 0.6 | 0.6 |
(1)比较此时正、逆反应速率的大小:v(正)____v(逆)(填“>”“<”或“=”)。
(2)若加入CH3OH后,经10min反应达到平衡,此时CH3OH的转化率__ ,该时间内反应速率v(CH3OH)=____ mol·L-1·min-1。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com