
【题目】由含碘废水制取碘酸钾的一种工艺如下:
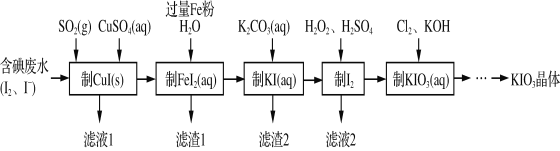
⑴ 写出KIO3在日常生活中的一个重要应用________________________。
⑵ 检验“含碘废水”中是否含有单质I2的常用试剂是________(写试剂名称)。
⑶ 通入SO2的目的是将I2还原为I-,该反应的离子方程式为______________________。
⑷ 工艺中五种物质的制备反应中,不涉及氧化还原反应的步骤是“制________”。
⑸ “制KI(aq)”时,该温度下水的离子积为Kw=1.0×10-13,Ksp[Fe(OH)2]=9.0×10-15。
为避免0.9 mol·L-1 FeI2溶液中Fe2+水解生成胶状物吸附I-,起始加入K2CO3必须保持溶液的pH不大于______。
⑹ “制KIO3溶液”反应的离子方程式为__________________。
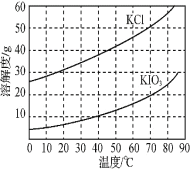
⑺ KCl、KIO3的溶解度曲线如图所示。流程中由“KIO3(aq)”得到KIO3晶体的操作步骤为_____________________。
【答案】食盐添加剂,补充碘成分,预防碘缺乏病 淀粉溶液 SO2+I2+2H2O=SO42-+2I-+4H+( 或2SO2+I2+2Cu2++4H2O=2CuI↓+2 SO42-+8H+) KI(aq) 6.0 5Cl2+I2+12OH-=2IO3-+10Cl-+6H2O 蒸发浓缩,降温结晶
【解析】
含碘废水制取碘酸钾晶体,由实验流程可知,含碘废水中加入SO2和硫酸铜制备CuI,发生2SO2+I2+2Cu2++4H2O═2CuI↓+2SO42-+8H+,滤液1含硫酸,过滤得到滤渣中加入铁粉、水制备FeI2,过滤得到滤渣1中含有Fe和Cu,滤液中加入碳酸钾制备KI,发生K2CO3+FeI2=FeCO3↓+2KI,滤渣2为FeCO3;酸性条件下KI、过氧化氢发生氧化还原反应生成碘,滤液2含硫酸钾,然后碘、氯气、KOH发生5Cl2+I2+12OH-═2IO3-+10Cl-+6H2O制备碘酸钾,结合溶解度曲线和物质的性质分析解答。
⑴ KIO3是日常生活中食用加碘盐的主要添加剂,可以预防碘缺乏病,故答案为:食盐添加剂,补充碘成分,预防碘缺乏病;
(2)因淀粉遇碘变蓝,因此检验“含碘废水”中是否含有单质I2,常用的试剂是淀粉溶液,故答案为:淀粉溶液;
(3)通入SO2的目的是将I2还原为I-,二氧化硫被氧化生成硫酸,反应的离子方程式为SO2+I2+2H2O═SO42-+2I-+4H+(或2SO2+I2+2Cu2++4H2O═2CuI↓+2SO42-+8H+),故答案为:SO2+I2+2H2O═SO42-+2I-+4H+(或2SO2+I2+2Cu2++4H2O═2CuI↓+2SO42-+8H+);
⑷ 根据工艺流程图,五种物质的制备反应中,只有制备KI溶液的过程中没有元素化合价的变化,不涉及氧化还原反应,故答案为:KI(aq);
(5)Ksp[Fe(OH)2]=9.0×10-15,现测得溶液中c(FeI2)为0.9 molL-1,则c(OH-)=![]() =10-7mol/L,此温度下,Kw=1.0×10-13,c(H+)=
=10-7mol/L,此温度下,Kw=1.0×10-13,c(H+)=![]() =10-6mol/L,pH=-lg10-6=6.0,故答案为:6.0;
=10-6mol/L,pH=-lg10-6=6.0,故答案为:6.0;
(6)“制KIO3溶液”时,氯气和碘单质与氢氧化钾溶液反应生成KIO3和氯化钾,反应的离子方程式为5Cl2+I2+12OH-═2IO3-+10Cl-+6H2O,故答案为:5Cl2+I2+12OH-═2IO3-+10Cl-+6H2O;
(7)由溶解度曲线图可知,KIO3的溶解度小于KCl且KIO3的溶解度随温度升高而增大,由KIO3溶液得到KIO3晶体,可以通过蒸发浓缩、降温结晶的方法得到,故答案为:蒸发浓缩、降温结晶。


 轻松暑假总复习系列答案
轻松暑假总复习系列答案科目:高中化学 来源: 题型:
【题目】A+、B2-、C-、D、E、F3+分别表示含10个电子的六种粒子(离子或分子)。其中:
a.A+、B2-、F3+核外电子层结构相同
b.C-是由两种元素组成的
c.D是两种元素组成的四原子分子
d.E在常温下是无色液体
e.往含F3+的溶液中滴加含C-的溶液至过量,先有白色沉淀生成,后白色沉淀消失
(1)C-的电子式___。
(2)A+、B2-、F3+离子半径由大到小的顺序为___(用离子符号表示)。
(3)含F3+的溶液中通入过量D,反应的离子方程式是___。
(4)A单质与E反应的离子方程式为___,生成的化合物中化学键的类型是___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25C时,0.1mol/L的3种溶液①盐酸②氨水③CH3COONa溶液。下列说法中,不正确的是
A. 3种溶液中pH最小的是①
B. 3种溶液中水的电离程度最大的是③
C. ①与②等体积混合后溶液显酸性
D. ①与③等体积混合后c(Na+)>c(Cl-)>c(H+)>c(CH3COO-)>c(OH-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碳和氮的氢化物是广泛的化工原料,回答下列问题:
(1)工业上合成氨的反应为N2(g)+3H2(g)![]() 2NH3(g) △H=-92.2kJ/mol,反应过程中能量变化如图I所示。
2NH3(g) △H=-92.2kJ/mol,反应过程中能量变化如图I所示。

①氨分解:2NH3(g)![]() N2(g)+3H2(g)的活化能为_________kJ/mol
N2(g)+3H2(g)的活化能为_________kJ/mol
②合成氨时加入铁粉可以加快生成NH3的速率,在图I中画出加入铁粉后的能量变化曲线。_______
(2)联氨作火箭燃料的反应为:2N2H4(l)+N2O4(l)=3N2(g)+4H2O(g) △H1
已知:2O2(g)+N2(g)=N2O4(1) △H2 N2H4(1)+O2(g)=N2(g)+2H2O(g) △H3
上述热效应之间的关系式为△H1=____。某新型火箭用液氧/煤油代替联氨/N2O4,这种替换可能的好处是___(一条即可)。
(3)天然气制氢气是工业上制氢气的主要方法之一,其主要反应如下:
i.CH4(g)+H2O(g)![]() CO(g)+3H2(g) ΔH=-+206.4kJ/mol,
CO(g)+3H2(g) ΔH=-+206.4kJ/mol,
ii.CO(g)+ H2O(g)![]() CO2(g)+H2(g) ΔH=-41.0kJ/mol
CO2(g)+H2(g) ΔH=-41.0kJ/mol
在一定温度下,2L的密闭容器中加入a molCH4和2amolH2O发生反应,t min时反应达平衡,测得容器内CObmol、CO2cmol。回答下列问题:
①下列可判断体系达到平衡状态的是_______。
A.CO的体积分数不变 B.容器内气体密度不变 C.3v(CH4)=v(H2) D.![]() 不再变化
不再变化
②0~tmin反应速率v(CO2)=_____,CH4的的转化率为_____,反应ⅱ的平衡常数K=______。
③图Ⅱ中T℃之后c(CO2)随温度升高而减小的原因是_________。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二氧化硫—空气质子交换膜燃料电池将化学能转变成电能的同时,实现了制硫酸、发电、环保三位一体的结合,降低了成本提高了效益,其原理如图所示。下列说法错误的是( )

A. Pt1电极附近发生的反应为:SO2+2H2O-2e-===SO![]() +4H+
+4H+
B. Pt2电极附近发生的反应为O2+4e-===2O2-
C. 该电池放电时电子从Pt1电极经过外电路流到Pt2电极
D. 相同条件下,放电过程中消耗的SO2和O2的体积比为2∶1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国科学家研发了一种室温下“可呼吸”的Na—CO2二次电池。将NaClO4溶于有机溶剂作为电解液,钠和负载碳纳米管的镍网分别作为电极材料,电池的总反应为:3CO2+4Na![]() 2Na2CO3+C。下列说法错误的是
2Na2CO3+C。下列说法错误的是

A. 放电时,ClO4-向负极移动
B. 充电时释放CO2,放电时吸收CO2
C. 放电时,正极反应为:3CO2+4e =2CO32-+C
D. 充电时,正极反应为:Na++e=Na
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某研究性学习小组为确定一种从煤中提取的液态烃X的结构,对其进行探究。
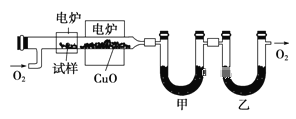
步骤一:这种碳氢化合物蒸气通过热的氧化铜(催化剂),氧化成二氧化碳和水,再用装有无水氯化钙和固体氢氧化钠的吸收管完全吸收.2.12g有机物X的蒸气氧化产生7.04g二氧化碳和1.80g水;
步骤二:通过仪器分析得知X的相对分子质量为106;
步骤三:用核磁共振仪测出X的1H核磁共振谱有2个峰,其面积之比为2∶3 (如图Ⅰ)

步骤四:利用红外光谱仪测得X分子的红外光谱如图Ⅱ,试填空:
①X的分子式为___________;X的习惯命名为___________;
②步骤二中的仪器分析方法称为___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I.有下列物质:①钠 ②金刚石 ③冰 ④Na2O2 ⑤MgCl2 ⑥氯化铵 ⑦水晶 ⑧Cl2
(1)属于原子晶体的是_________,属于金属晶体的是_________。
(2)既含有离子键又含有共价键的是_________。
(3)③熔化时克服作用力的有_________。
(4)Na2O2的电子式 ________________。
(5)②、③、⑤、⑦、⑧熔点由低到高的顺序为________________。
II.在生产生活以及化学科学研究中,水都有重要的作用。
(1)与H2O分子是等电子体的微粒_________(阴离子及分子各写一个)。
(2)水分子在特定条件下容易得到一个H+,形成水合氢离子(H3O+)。下列对上述过程的描述不合理的是__________。
A.微粒的形状发生了改变
B.氧原子的杂化类型发生了改变
C.微粒中的键角发生了改变
D.微粒的化学性质发生了改变
(3)向CuSO4溶液中加入氨水,溶液变成深蓝色,请写出发生此变化的离子方程式______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有X、Y、Z三种短周期元素,原子半径由大到小的顺序为Y>X>Z,原子序数之和为16。三种元素的常见单质在适当条件下可发生如图所示的变化,其中B和C均为10电子分子,以下说法不正确的是
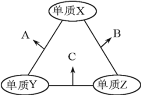
A.A和C不可能发生氧化还原反应
B.X元素位于ⅥA族
C.A不能溶解于B中
D.B的沸点高于C的沸点
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com