
【题目】Zn与硝酸反应时,硝酸溶液的浓度不同,产物也不相同。与不同浓度硝酸反应时,反应的Zn与被还原硝酸的物质的量关系如图。还原产物为NH4NO3的曲线是( )
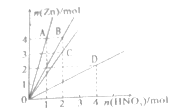
A.AB.BC.CD.D
 灵星计算小达人系列答案
灵星计算小达人系列答案 孟建平错题本系列答案
孟建平错题本系列答案科目:高中化学 来源: 题型:
【题目】羟氯喹是一种抗疟药物,被WHO支持用于新冠肺炎患者临床研究。某研究小组设计如下合成路线:
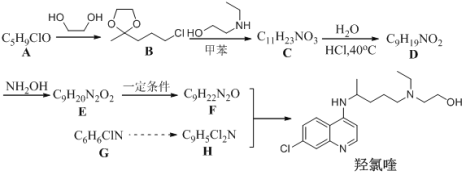
已知:
①
② ![]()
③
④苯环上连卤原子时,发生再取代反应主要生成邻、对位产物。
按要求回答下列问题:
(1)化合物A所含官能团的名称为___________________,化合物C的结构简式_______。
(2)下列说法正确的是___________________。
A. A到D过程中,乙二醇的作用是作为保护基团
B. 从合成路线推测,化合物B要密封干燥保存
C. E→F为加成反应
D. 羟氯喹的分子式为C18H26ClN3O
(3)D→E的化学方程式为____________________________。
(4)设计以苯为原料合成化合物G(用流程图表示,无机试剂任选)______________。
(5)写出同时符合下列条件的H的同分异构体的结构简式(不考虑立体异构):_______________。
1H-NMR和IR谱检测表明:
①苯环上有两种环境的不同氢,且两种氢的比例为2:1;②分子中含有氰基(-CN)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】水泥是重要的建筑材料。水泥熟料的主要成分为CaO、SiO2,并含有一定量的铁、铝和镁等金属的氧化物。实验室测定水泥样品中钙含量的过程如图所示:
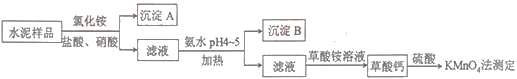
回答下列问题:
(1)沉淀A的主要成分是__。
(2)在分解水泥样品过程中,以盐酸为溶剂,氯化铵为助溶剂,还需加入几滴硝酸。加入硝酸的目的是__,请写出相应的离子方程式:__。
(3)草酸钙沉淀经稀H2SO4处理后,用KMnO4标准溶液滴定,通过测定草酸的量可间接获知钙的含量,实验中称取0.400g水泥样品,滴定时消耗了0.0500molL-1KMnO4溶液36.00mL。
①请配平此滴定过程中的反应。
___MnO![]() +___H++___H2C2O4——___Mn2++___CO2+___H2O
+___H++___H2C2O4——___Mn2++___CO2+___H2O
②求该水泥样品中钙的质量分数为___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某工业烟气中含有CO、CO2、N2、SO2等气体,用Na2SO3溶液吸收并回收SO2的过程如下图所示。
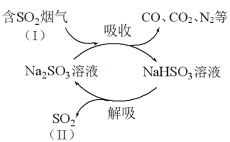
(1)SO2的浓度:I________II(填“>”或“<”)。
(2)在这个过程中可以循环使用的物质是________。
(3)上述吸收过程中主要反应的化学方程式是________。
(4)解吸过程需要加热,在这个过程中常伴有少量SO42-产生。
① 证明产物中含SO42-的实验方法是:取少量解吸产物的溶液,________(填操作和现象)。
② 产生SO42-的原因是_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学生用如图所示装置制取氯气,并收集氯气进行实验。
请完成下列问题:
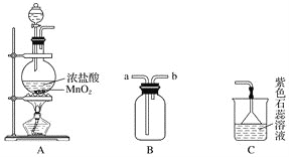
(1)装置A中发生反应的离子方程式为______________________________________。
(2)装置B如图中所示正放,则连接A的接口是________(填序号)。
(3)实验中可观察到装置C中紫色石蕊溶液的现象是__________________,其原因______________________________________________________________________。
(4)取出B中的集气瓶进行氯气与铜的反应实验,应该进行的操作是______________,然后立刻放入充满氯气的集气瓶中。实验中有同学提出应该在集气瓶底先放少量的水或细沙,你认为__________(填“需要”或“不需要”)放,理由是____________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】金属钛(Ti)因其硬度大、熔点高、常温时耐酸碱腐蚀而被广泛用作高新科技材料,被誉为“未来金属”。以钛铁矿(主要成分钛酸亚铁)为主要原料冶炼金属钛同时获得副产品甲的工业生产流程如下。请回答下列问题。
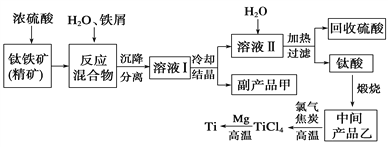
(1)钛酸亚铁(用R表示)与碳在高温下反应的化学方程式为2R+C═2Fe+2TiO2+CO2↑,钛酸亚铁的化学式为_______________;钛酸亚铁和浓H2SO4反应的产物之一是TiOSO4,反应中无气体生成,该反应的化学方程式为____________________。
(2)上述生产流程中加入铁屑的目的是_________________________,此时溶液Ⅰ中含有Fe2+、TiO2+和少量Mg2+等阳离子。常温下,其对应氢氧化物的Ksp如下表所示。
氢氧化物 | Fe(OH)2 | TiO(OH)2 | Mg(OH)2 |
Ksp | 8.0×10-16 | 1.0×10-29 | 1.8×10-11 |
①常温下,若所得溶液中Mg2+的物质的量浓度为0.0018mol/L,当溶液的pH等于_______时,Mg(OH)2开始沉淀。
②若将含有Fe2+、TiO2+和Mg2+的溶液加水稀释,立即析出大量白色沉淀,该反应的离子方程式为___________________________________________________________。
(3)中间产品乙与焦炭、氯气在高温下发生反应制取TiCl4的方程式为________。Mg还原TiCl4过程中必须在1070K的温度下进行,你认为还应该控制的反应条件是_________。除去所得金属钛中少量的金属镁可用的试剂是__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】浓硝酸具有强氧化性。
①把铜粉和铁粉混合物加入热的浓硝酸中,充分反应后,溶液中有铜剩余,则溶液中存在的金属阳离子为___。
②某稀硫酸与稀硝酸的混合溶液中,c(SO42-)+c(NO3-)=3.0mol·L-1。取200mL该混合酸,能溶解铜的最大质量为___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某实验小组同学利用如图装置对电化学原理进行了一系列探究活动。
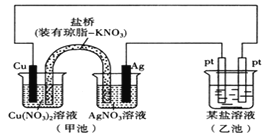
(1)甲池为装置__(填“原电池”或“电解池”)。
(2)甲池反应前,两电极质量相等,一段时间后,两电极质量相差28g,导线中通过__mol电子。
(3)实验过程中,甲池左侧烧杯中NO3-的浓度__(填“变大”、“变小”或“不变”)。
(4)其他条件不变,若用U形铜棒代替“盐桥”,工作一段时间后取出U形铜棒称量,质量___(填“变大”、“变小”或“不变”)。
(5)若乙池中的某盐溶液是足量AgNO3溶液,则乙池中左侧Pt电极反应式为___,工作一段时间后,若要使乙池溶液恢复原来浓度,可向溶液中加入___(填化学式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某微生物电池在运行时可同时实现净化有机物污水、净化含![]() 废水(pH约为6)和淡化食盐水,其装置示意图如图所示。图中,D和E为离子交换膜,Z为待淡化食盐水。(已知Cr3+完全沉淀所需的pH为5.6)下列说法不正确的是
废水(pH约为6)和淡化食盐水,其装置示意图如图所示。图中,D和E为离子交换膜,Z为待淡化食盐水。(已知Cr3+完全沉淀所需的pH为5.6)下列说法不正确的是
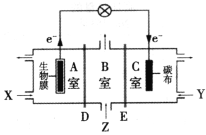
A.E为阴离子交换膜
B.X为有机物污水,Y为含![]() 废水
废水
C.理论上处理1 mol的![]() 的同时可脱除3 mol的NaC1
的同时可脱除3 mol的NaC1
D.C室的电极反应式为![]() +6e-+8H+==2Cr(OH)3↓+H2O
+6e-+8H+==2Cr(OH)3↓+H2O
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com