
����Ŀ���������һ�ֿ�űҩ���WHO֧�������¹ڷ������ٴ��о���ij�о�С��������ºϳ�·�ߣ�
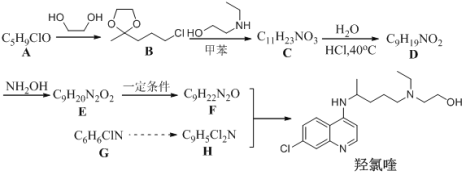
��֪��
��
�� ![]()
��
�ܱ�������±ԭ��ʱ��������ȡ����Ӧ��Ҫ�����ڡ���λ���
��Ҫ��ش��������⣺
(1)������A���������ŵ�����Ϊ___________________��������C�Ľṹ��ʽ_______��
(2)����˵����ȷ����___________________��
A. A��D�����У��Ҷ�������������Ϊ��������
B. �Ӻϳ�·���Ʋ⣬������BҪ�ܷ���ﱣ��
C. E��FΪ�ӳɷ�Ӧ
D. ����୵ķ���ʽΪC18H26ClN3O
(3)D��E�Ļ�ѧ����ʽΪ____________________________��
(4)����Ա�Ϊԭ�Ϻϳɻ�����G(������ͼ��ʾ�����Լ���ѡ)______________��
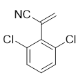
(5)д��ͬʱ��������������H��ͬ���칹��Ľṹ��ʽ(�����������칹)��_______________��
1H-NMR��IR��������
�ٱ����������ֻ����IJ�ͬ�⣬��������ı���Ϊ2:1���ڷ����к������(-CN)
���𰸡��ʻ�����ԭ�� 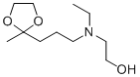 ABD
ABD 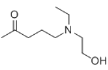 +NH2OH��
+NH2OH��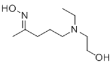 +H2O
+H2O 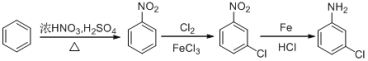
��������
A��HOCH2CH2OH��Ӧ����B������A�ķ���ʽ�����B�Ľṹ��֪AΪ![]() ��B������Ϣ1�ķ�Ӧ����C������B�ͷ�Ӧ��Ľṹ��֪CΪ
��B������Ϣ1�ķ�Ӧ����C������B�ͷ�Ӧ��Ľṹ��֪CΪ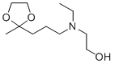 ��C��Ӧ����D������D�ķ���ʽ�Լ�D�ܷ����ķ�Ӧ�������Ʋ��D��Ӧ�ú����ʻ�������DΪ
��C��Ӧ����D������D�ķ���ʽ�Լ�D�ܷ����ķ�Ӧ�������Ʋ��D��Ӧ�ú����ʻ�������DΪ ��D��NH2OH����������Ϣ2�ķ�Ӧ����E������EΪ
��D��NH2OH����������Ϣ2�ķ�Ӧ����E������EΪ ��E��һ������������F���Ա�F��E�ķ���ʽ��֪�ù�����E�������⣬������ԭ��Ӧ����F��FӦΪ
��E��һ������������F���Ա�F��E�ķ���ʽ��֪�ù�����E�������⣬������ԭ��Ӧ����F��FӦΪ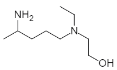 ��F��H��Ӧ��������ୣ����������F�Ľṹ�����Ʋ�F��H����������Ϣ1�ķ�Ӧ������H�Ľṹ��ʽӦΪ
��F��H��Ӧ��������ୣ����������F�Ľṹ�����Ʋ�F��H����������Ϣ1�ķ�Ӧ������H�Ľṹ��ʽӦΪ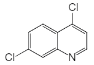 ����GΪ
����GΪ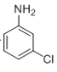 ��
��
(1)���ݷ�����֪AΪ![]() ���������Ϊ�ʻ��������ӣ����ݷ���C�Ľṹ��ʽΪ
���������Ϊ�ʻ��������ӣ����ݷ���C�Ľṹ��ʽΪ ��
��
(2)A�����ݷ�����֪A��D�Ĺ���A���ʻ������Ҷ�����Ӧ������C��D�Ĺ�����������ת��Ϊ�ʻ��������Ҷ�������������Ϊ�������ţ���A��ȷ��
B������C��D��Ӧ������֪��BҲ������ˮ��Ӧ������BҪ�ܷ���ﱣ�棬��B��ȷ��
C��E��F�Ĺ�����E�������⣬̼��˫����ͬʱ�����������ѣ�����Ϊ��ԭ��Ӧ�������Ǽӳɷ�Ӧ����C����
D����������୵Ľṹ��ʽ��֪�����ʽΪC18H26ClN3O����D��ȷ��
��������ѡABD��
(3)D����������Ϣ2�ķ�Ӧ����E����ѧ����ʽΪ +NH2OH��
+NH2OH�� +H2O��
+H2O��
(4)GΪ![]() ���������������ڼ�λ��ȡ����������������±ԭ��ʱ��������ȡ����Ӧ��Ҫ�����ڶ�λ����������������ʱ������������ԭ�ӣ�������Ϣ3��֪�����ϵ��������Ա���ԭ�ɰ��������Կ�����ͨ��������Ӧ�ڱ���������������Ȼ������Һ�Ⱥ����������Ȼ����Ĵ������·���ȡ����֮��ԭ�������ɰ��������Ժϳ�·�߿���Ϊ
���������������ڼ�λ��ȡ����������������±ԭ��ʱ��������ȡ����Ӧ��Ҫ�����ڶ�λ����������������ʱ������������ԭ�ӣ�������Ϣ3��֪�����ϵ��������Ա���ԭ�ɰ��������Կ�����ͨ��������Ӧ�ڱ���������������Ȼ������Һ�Ⱥ����������Ȼ����Ĵ������·���ȡ����֮��ԭ�������ɰ��������Ժϳ�·�߿���Ϊ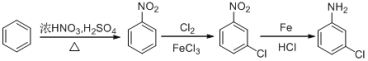 ��
��
(5)HΪ ����ͬ���칹�����㣺
����ͬ���칹�����㣺
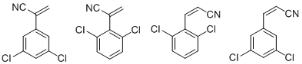
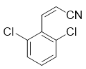
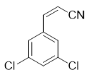
�ٱ����������ֻ����IJ�ͬ�⣬��������ı���Ϊ2:1��������3��ȡ��������������������ͬ��ȡ����λ�ڼ�λ������һ����ͬȡ����λ��������ͬȡ��������λ���λ��
�ڷ����к������(-CN)������������Ľṹ��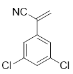 ��
�� ��
�� ��
�� ��
��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��HIn��ˮ��Һ�д������µ���ƽ�⣺HIn(��ɫ��![]() H+ + In-(��ɫ�����ʿ��������ָʾ����Ũ��Ϊ0.02 mol/L�����и���Һ�������ᣬ��ʯ��ˮ����NaCl��Һ����NaHSO4��Һ����Na2CO3��Һ���ް�ˮ��������ʹָʾ���Ժ�ɫ����
H+ + In-(��ɫ�����ʿ��������ָʾ����Ũ��Ϊ0.02 mol/L�����и���Һ�������ᣬ��ʯ��ˮ����NaCl��Һ����NaHSO4��Һ����Na2CO3��Һ���ް�ˮ��������ʹָʾ���Ժ�ɫ����
A. �٢ܢ� B. �ڢݢ� C. �٢� D. �ڢۢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ӷ���ʽ��д��ȷ����
A.FeCl3��Һ��Cu��ϣ�FeCl3��Cu = Fe2+��Cu2+ +3Cl-
B.��ȩ��Һ�м���������������Һ�����ȣ�HCHO+2[Ag(NH3)2]++2OH��![]() HCOO��+NH
HCOO��+NH![]() +2Ag��+3NH3+H2O
+2Ag��+3NH3+H2O
C.̼�����Ƶ�ˮ�ⷽ��ʽ��HCO![]() +H2O
+H2O![]() CO
CO![]() +H3O+
+H3O+
D.Ca(HCO3)2��Һ�м��������ˮ��Ca2++2HCO![]() +2NH3H2O=CaCO3��+2H2O+2NH
+2NH3H2O=CaCO3��+2H2O+2NH![]() +CO
+CO![]()
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��900 ��ʱ����2.0 L�����ܱ������г���0.40 mol�ұ���������Ӧ��
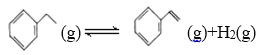
һ��ʱ���Ӧ�ﵽƽ�⣬��Ӧ�����вⶨ�IJ����������±���ʾ��
ʱ��/min | 0 | 10 | 20 | 30 | 40 |
n(�ұ�)/mol | 0.40 | 0.30 | 0.24 | n2 | n3 |
n(����ϩ)/mol | 0.00 | 0.10 | n1 | 0.20 | 0.20 |
����˵����ȷ����
A.���������������䣬�������г��벻���뷴Ӧ��ˮ������Ϊϡ�ͼ������ұ���ת���ʴ���50.0%
B.��Ӧ��ǰ20 min�ڵ�ƽ����Ӧ����v(H2)��0.008 mol��L��1��min��1
C.���������������䣬�������г��벻���뷴Ӧ��ˮ������Ϊϡ�ͼ�����ϵ����ѹ����ƽ��ʱ������ķ�ѹҲ���ӡ�
D.��ͬ�¶��£���ʼʱ�������г���0.10 mol�ұ���0.10 mol����ϩ��0.30 mol H2����ﵽƽ��ǰ��v����v��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������£���20 mL 0.01 mol/L CH3COOH��Һ����μ���0.01 mol/L ��NaOH��Һ����Һ��ˮ���������c(H+)�����NaOH��Һ������仯ʾ��ͼ���£�����˵����ȷ����
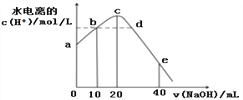
A. ��a��c���Դ���ĵ�����дٽ�����Ҳ����������
B. b��d������Һ��pH��ͬ
C. e����ʾ��Һ�У�c(Na+)=2c(CH3COO-)��2c(CH3COOH) = 0.01mol/L
D. ��b��d�Ĺ����У��ȴ���pH=7�ĵ�Ҳ����ˮ�����c(H+)=10-7�ĵ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������һ�����ص�Ԫ�أ������Գ����DZ������������ߵ�ɢ�з��䡣
(1)д��BF3����ʽ___________��B��F�γɹ��ۼ�ʱ�����õ��Ӷ�ƫ��_____ԭ�ӣ��ж�������_________________��
(2)����(H3BO3)��ˮ�е����������[B(OH)4]-����д������ĵ��뷽��ʽ___________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ֶ���������Ԫ��W��X��Y��Z��ԭ��������������W��X�ļ����Ӿ�����ͬ���Ӳ�ṹ��X��ԭ�Ӱ뾶�Ƕ���������Ԫ��ԭ�������ģ�W��Yͬ�壬Z��X�γɵ����ӻ������ˮ��Һ�����ԡ�����˵����ȷ���ǣ� ��
A.�����Ӱ뾶��![]()
B.W��X�γɵĻ���������ˮ����Һ�ʼ���
C.��̬�⻯������ȶ��ԣ�![]()
D.����������ˮ��������ԣ�![]()
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��̫���ܵ�ؿɷ�Ϊ����̫���ܵ�أ�������̫���ܵ�أ����黯��(GaAs)��ͭ������(CIGS)������(CdS)�����ܸ߷���̫���ܵ�صȣ�Al-Ni�����缫���ݴ˻ش����⣺
(1)��(Ni)�����ڱ��е�λ��Ϊ______��Sԭ�ӵļ۵����Ų�ʽΪ________��Ga��As��Se�ĵ�һ�������ɴ�С��˳����________��
(2)Na3As3��Asԭ�ӵ��ӻ���ʽΪ_____��AsCl3�Ŀռ乹��Ϊ____��
(3)GaAs�۵�Ϊ1238�棬GaN�۵�ԼΪ1500����GaAs�۵����GaN��ԭ��Ϊ__________��
(4)д��һ����SO42-��Ϊ�ȵ�����ķ���_________��
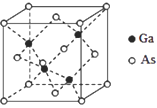
(5)GaAs�ľ����ṹ��ͼ��ʾ������Asԭ���γɵĿ�϶���������������κ����������Σ��þ�����Gaԭ��������϶����Ϊ_____����֪GaAs���ܶ�Ϊ��g/cm3��Ga��As��Ħ�������ֱ�Ϊ MGa g/mol��MAsg/mol����GaAs������Ga֮�����̾���Ϊ________pm��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Zn�����ᷴӦʱ��������Һ��Ũ�Ȳ�ͬ������Ҳ����ͬ���벻ͬŨ�����ᷴӦʱ����Ӧ��Zn�뱻��ԭ��������ʵ�����ϵ��ͼ����ԭ����ΪNH4NO3�������ǣ� ��
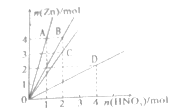
A.AB.BC.CD.D
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com