
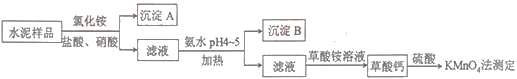
【题目】水泥是重要的建筑材料。水泥熟料的主要成分为CaO、SiO2,并含有一定量的铁、铝和镁等金属的氧化物。实验室测定水泥样品中钙含量的过程如图所示:
回答下列问题:
(1)沉淀A的主要成分是__。
(2)在分解水泥样品过程中,以盐酸为溶剂,氯化铵为助溶剂,还需加入几滴硝酸。加入硝酸的目的是__,请写出相应的离子方程式:__。
(3)草酸钙沉淀经稀H2SO4处理后,用KMnO4标准溶液滴定,通过测定草酸的量可间接获知钙的含量,实验中称取0.400g水泥样品,滴定时消耗了0.0500molL-1KMnO4溶液36.00mL。
①请配平此滴定过程中的反应。
___MnO![]() +___H++___H2C2O4——___Mn2++___CO2+___H2O
+___H++___H2C2O4——___Mn2++___CO2+___H2O
②求该水泥样品中钙的质量分数为___。
【答案】SiO2 将样品中可能存在的Fe2+氧化为Fe3+ 3Fe2++4H++NO![]() =3Fe3++NO↑+2H2O 2 6 5 2 10 8 45.0%
=3Fe3++NO↑+2H2O 2 6 5 2 10 8 45.0%
【解析】
水泥熟料的主要成分为CaO、SiO2,并含有一定量的铁、铝和镁等金属的氧化物,加入氯化铵、盐酸和硝酸,由于二氧化硅与酸不反应,则得到的沉淀A为SiO2,滤液中含有Ca2+、Fe3+、Al3+、Mg2+等离子,加入氨水调节pH4~5,可生成Al(OH)3、Fe(OH)3沉淀,加热的目的是防止生成胶体而难以分离,滤液主要含有Ca2+,加入草酸铵可生成草酸钙沉淀,加入硫酸用高锰酸钾测定,发生5Ca2+~5H2C2O4~2KMnO4,根据高锰酸钾的量可计算含量。
(1)由以上分析可知沉淀A为SiO2,故答案为:SiO2;
(2)铁离子在pH较小时易生成沉淀,加入硝酸可氧化亚铁离子生成铁离子,相应的离子方程式:3Fe2++4H++NO![]() =3Fe3++NO↑+2H2O;
=3Fe3++NO↑+2H2O;
故答案为:将样品中可能存在的Fe2+氧化为Fe3+;3Fe2++4H++NO![]() =3Fe3++NO↑+2H2O;
=3Fe3++NO↑+2H2O;
(3)①在硫酸条件下,高锰酸钾将C2O42-氧化为CO2,自身被还原为MnSO4,依据氧化还原反应得失电子守恒、原子个数守恒写出反应的离子方程式:2MnO4-+5H2C2O4+6H+=2Mn2++10CO2↑+8H2O,故答案为:2MnO4-+5H2C2O4+6H+=2Mn2++10CO2↑+8H2O;
②反应的关系式为5Ca2+~5H2C2O4~2KMnO4,
n(KMnO4)=0.0500mol·L-1×36.00mL=1.800mmol,n(Ca2+)=4.500mmol,水泥中钙的质量分数为![]() ×100%=45.00%,故答案为:45.00%。
×100%=45.00%,故答案为:45.00%。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】下列离子方程式书写正确的是
A.FeCl3溶液和Cu混合:FeCl3+Cu = Fe2++Cu2+ +3Cl-
B.甲醛溶液中加入足量的银氨溶液并加热:HCHO+2[Ag(NH3)2]++2OH﹣![]() HCOO﹣+NH
HCOO﹣+NH![]() +2Ag↓+3NH3+H2O
+2Ag↓+3NH3+H2O
C.碳酸氢钠的水解方程式:HCO![]() +H2O
+H2O![]() CO
CO![]() +H3O+
+H3O+
D.Ca(HCO3)2溶液中加入过量氨水:Ca2++2HCO![]() +2NH3H2O=CaCO3↓+2H2O+2NH
+2NH3H2O=CaCO3↓+2H2O+2NH![]() +CO
+CO![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】四种短周期主族元素W、X、Y、Z的原子序数依次增大,W、X的简单离子具有相同电子层结构,X的原子半径是短周期主族元素原子中最大的,W与Y同族,Z与X形成的离子化合物的水溶液呈中性。下列说法正确的是( )
A.简单离子半径:![]()
B.W与X形成的化合物溶于水后溶液呈碱性
C.气态氢化物的热稳定性:![]()
D.最高价氧化物的水化物的酸性:![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】太阳能电池可分为:硅太阳能电池,化合物太阳能电池,如砷化镓(GaAs)、铜铟镓硒(CIGS)、硫化镉(CdS),功能高分子太阳能电池等,Al-Ni常作电极。据此回答问题:
(1)镍(Ni)在周期表中的位置为______;S原子的价电子排布式为________;Ga、As和Se的第一电离能由大到小的顺序是________。
(2)Na3As3中As原子的杂化方式为_____;AsCl3的空间构型为____。
(3)GaAs熔点为1238℃,GaN熔点约为1500°,GaAs熔点低于GaN的原因为__________。
(4)写出一种与SO42-互为等电子体的分子_________。
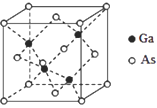
(5)GaAs的晶胞结构如图所示,其中As原子形成的空隙类型有正八面体形和正四面体形,该晶胞中Ga原子所处空隙类型为_____。已知GaAs的密度为ρg/cm3,Ga和As的摩尔质量分别为 MGa g/mol和MAsg/mol,则GaAs晶胞中Ga之间的最短距离为________pm。
查看答案和解析>>
科目:高中化学 来源: 题型:
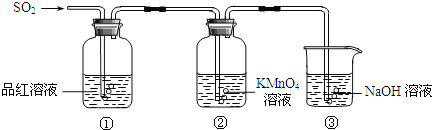
【题目】某小组同学利用如图所示装置探究二氧化硫气体的性质.
请回答:
(1)实验室用铜和浓硫酸共热制取二氧化硫,反应的化学方程式是 .
(2)当观察到②中溶液颜色变浅时,①中的现象是 .
(3)装置③的作用是 .
(4)①、②中的现象说明二氧化硫具有的性质是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于2—环己基丙烯(![]() )和2—苯基丙烯(
)和2—苯基丙烯(![]() )的说法中正确的是( )
)的说法中正确的是( )
A.二者均可使溴水、高锰酸钾褪色,且褪色原理相同
B.2—苯基丙烯分子中所有碳原子一定共平面
C.二者可与足量的氢气在一定条件下反应得到同一种产物,此产物的一氯代物有5种
D.二者可以通过加成聚合反应形成高分子化合物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】环己酮(![]() )在生产生活中有重要的用途,可在酸性溶液中用环己醇间接电解氧化法制备,其原理如图所示。下列说法正确的是
)在生产生活中有重要的用途,可在酸性溶液中用环己醇间接电解氧化法制备,其原理如图所示。下列说法正确的是
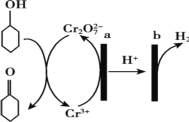
A.a 极与电源负极相连
B.a 极电极反应式是 2Cr3+- 6e- +14OH-= Cr2O72-+7H2O
C.b 极发生氧化反应
D.理论上生成 1mol 环己酮时,有 1molH2 生成
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Zn与硝酸反应时,硝酸溶液的浓度不同,产物也不相同。与不同浓度硝酸反应时,反应的Zn与被还原硝酸的物质的量关系如图。还原产物为NH4NO3的曲线是( )
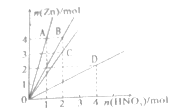
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以碘为原料,通过电解制备 KIO3 的实验装置如右图所示。电解前,先将一定量的精制碘溶于过 量 KOH 溶液,溶解时发生反应:3I2+6KOH=5KI+KIO3+3H2O,将该溶液加入某电极区。将 KOH 溶液加入另一电极区,电解槽用水冷却。下列说法不正确的是
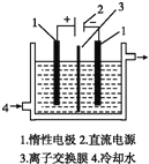
A.产品 KIO3 在阳极区得到B.离子交换膜为阴离子交换膜
C.电解时,须不断补充 KOHD.阴极区加入的是 KOH 溶液,发生还原反应生成 H2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com