
【题目】对下列现象或事实的解释正确的是![]()
选项 | 现象或事实 | 解释 |
A | 用热的纯碱溶液洗去油污 |
|
B | 漂白粉在空气中久置变质 | 漂白粉中的 |
C | 施肥时,草木灰 |
|
D | 钢铁在潮湿的空气中容易生锈 | 钢铁在空气中发生了析氢腐蚀 |
A.AB.BC.CD.D
科目:高中化学 来源: 题型:
【题目】下列有关热化学方程式的叙述正确的是( )
A. 已知2H2(g)+O2(g) =2 H2O(g) △H=-483.6kJ·mol-1,则氢气的燃烧热△H=-241.8 kJ/mol
B. 已知2C(s)+2O2(g)=2CO2(g)△H1;2C(s)+O2(g)=2CO(g)△H2,则△H1>△H2
C. 含20.0g NaOH的稀溶液与稀盐酸完全中和,放出28.7kJ的热量,则稀醋酸和稀NaOH溶液反应的热化学方程式为: NaOH(aq)+CH3COOH(aq) = CH3COONa(aq) + H2O(l) △H =-57.4kJ·mol-1
D. CO(g)的燃烧热是283.0 kJ/mol,则2CO2(g)=2CO(g)+O2(g) △H=+566.0 kJ/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.(1)工业废水中常含有Cu2+等重金属离子,直接排放会造成污染,目前在工业废水处理过程中,依据沉淀转化的原理,常用FeS等难溶物质作为沉淀剂除去这些离子。已知室温下Ksp(FeS)=6.3×10-18,Ksp(CuS)=1.3×10-36。请用离子方程式说明上述除杂的原理__。
(2)在t℃时,某NaOH稀溶液中,c(H+)=10-amol/L,c(OH-)=10-bmol/L,已知a+b=12,则该温度下水的离子积常数KW=__。在该温度下,将100mL0.1mol/L的稀硫酸与100mL0.4mol/L的NaOH溶液混合后,溶液的pH=___。
Ⅱ.工业生成尿素的原理是以NH3和CO2为原料合成尿素,反应的化学方程式为2NH3(g)+ CO2(g)![]() CO(NH2)2(1)+H2O(1),该反应的平衡常数和温度关系如下:
CO(NH2)2(1)+H2O(1),该反应的平衡常数和温度关系如下:
T/℃ | 165 | 175 | 185 | 195 |
K | 111.9 | 74.1 | 50.6 | 34.8 |
(1)ΔH___0(填“>”、“<”或“=”)。
(2)在一定温度和压强下,若原料气中的NH3和CO2的物质的量之比(氨碳比)n(NH3)∶n(CO2)=x,如图是氨碳比(x)与CO2平衡转化率(α)的关系,α随着x增大而增大的原因是___。
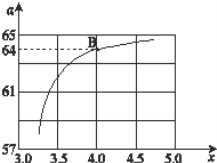
(3)图中的B点对应的NH3的平衡转化率为__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于![]() 溶液的叙述正确的是
溶液的叙述正确的是![]()
A.![]() 俗名纯碱,其水溶液显弱碱性
俗名纯碱,其水溶液显弱碱性
B.该溶液中![]() 、
、![]() 、
、![]() 可以大量共存
可以大量共存
C.加水稀释该溶液,溶液中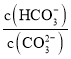 增大
增大
D.向该溶液中加入足量的氢氧化钙溶液的离子方程式为:![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ某兴趣小组的同学用下图所示装置研究有关电化学的问题![]() 甲、乙、丙三池中溶质足量
甲、乙、丙三池中溶质足量![]() ,当闭合该装置的开关K时,观察到电流计的指针发生了偏转。请回答下列问题:
,当闭合该装置的开关K时,观察到电流计的指针发生了偏转。请回答下列问题:
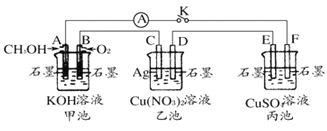
(1)甲、乙、丙三池中为原电池的是______ (填“甲池”、“乙池”或“丙池”)。
(2)写出甲池中A电极的电极反应式____________。
(3)丙池中F电极为______ (填“正极”、“负极”、“阴极”或“阳极”),该池的总反应化学方程式为_________。
(4)当乙池中C电极质量减轻![]() 时,甲池中B电极理论上消耗
时,甲池中B电极理论上消耗![]() 的体积为____mL(标况)。
的体积为____mL(标况)。
(5)一段时间后,断开开关K。下列物质能使丙池恢复到反应前浓度的是____ (填选项字母)。
A.Cu ![]()
![]()
![]()
Ⅱ控制适合的条件,将反应![]() ,设计成如上图所示装置。请回答下列问题:
,设计成如上图所示装置。请回答下列问题:
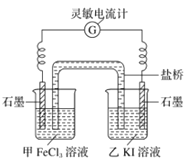
(6)反应开始时,乙中石墨电极上发生___(填“氧化”或“还原”)反应,电极反应式为_______。盐桥中的__ (填“阳”或“阴”)离子向甲溶液方向移动。
(7)电流计读数为0时,反应达到平衡状态,此时在甲中加入![]() 固体,则甲中的石墨作______
固体,则甲中的石墨作______![]() 填“正”或“负”
填“正”或“负”![]() 极,该电极的电极反应式为_______________。
极,该电极的电极反应式为_______________。
(Ⅲ)高铁电池是一种新型可充电电池,与普通高能电池相比,该电池长时间保持稳定的放电电压。高铁电池的总反应为:![]()
![]()
![]() 。
。
(8)放电时负极反应为______, 充电时阳极反应为_______,放电时正极附近溶液的碱性___![]() 选填“增强”“减弱”或“不变”
选填“增强”“减弱”或“不变”![]() 。
。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列方程式书写正确的是( )
A.NaHSO4在水溶液中的电离方程式:NaHSO4=Na++HSO4-
B.H2SO3的电离方程式:H2SO3![]() 2H++SO32-
2H++SO32-
C.CO32-的水解方程式:CO32-+H2O![]() HCO3-+OH-
HCO3-+OH-
D.CaCO3的电离方程式:CaCO3![]() Ca2++CO32-
Ca2++CO32-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】采用CO与H2反应合成再生能源甲醇,反应如下:CO(g)+ 2H2(g)![]() CH3OH(g),在一容积可变的密闭容器中充有10molCO和20mol H2,在催化剂作用下发生反应生成甲醇。CO的平衡转化率(α)与温度(T)、压强(p)的关系如图所示。则下列理解不符合题意的是
CH3OH(g),在一容积可变的密闭容器中充有10molCO和20mol H2,在催化剂作用下发生反应生成甲醇。CO的平衡转化率(α)与温度(T)、压强(p)的关系如图所示。则下列理解不符合题意的是
A. B点的速率比C点的大
B. A、B、C三点的平衡常数KA、KB、KC的大小关系为:KA=KB>KC
C. 若达到平衡状态A时,容器的体积为10L,则在平衡状态B时容器的体积为2L
D. 合成甲醇的反应为放热反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某实验小组学生用50 mL 0.50 mol·L1盐酸与50 mL 0.55 mol·L1 NaOH溶液在如图所示的装置中进行中和反应,通过测定反应过程中放出的热量计算中和热。下列说法正确的是

A. 实验过程中没有热量损失
B. 图中实验装置缺少环形玻璃搅拌棒
C. 烧杯间填满碎泡沫塑料的作用是固定小烧杯
D. 酸或碱的物质的量越大,所测中和热的数值越大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对下列图像描述正确的是

A. 图①可表示将氨气通入醋酸溶液至过量过程中溶液导电性的变化
B. 根据图②可判断可逆反应A2(g)+3B2(g)![]() 2AB3(g)的ΔH>0
2AB3(g)的ΔH>0
C. 图③表示等体积、等pH的盐酸与醋酸溶液分别与足量的锌粉发生反应产生氢气的体积(V)随时的变化的示意图
D. 图④可表示压强对可逆反应A(g)+B(g)![]() 2C(g)+D(g)的影响,乙的压强大
2C(g)+D(g)的影响,乙的压强大
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com