
 已知
已知  可简写为
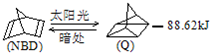
可简写为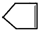 利用某些有机物之间的转化可贮存太阳能,如原降冰片二烯(NBD)经太阳光照转化成四环烷(Q)的反应为如图所示下列有关说法不正确的是( )
利用某些有机物之间的转化可贮存太阳能,如原降冰片二烯(NBD)经太阳光照转化成四环烷(Q)的反应为如图所示下列有关说法不正确的是( )| A、物质Q比NBD更稳定 |
| B、物质Q的一氯取代物只有3种 |
| C、一定条件下,1 mol NBD最多可与2 mol Br2发生加成反应 |
| D、NBD和Q二者互为同分异构体 |
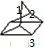 ,则Q的一氯取代物只有3种,故B正确;
,则Q的一氯取代物只有3种,故B正确;

 活力课时同步练习册系列答案
活力课时同步练习册系列答案 学业测评一课一测系列答案
学业测评一课一测系列答案科目:高中化学 来源: 题型:
| A、溶液中c(H+)和c(OH-)都减小 |
| B、溶液中c(H+)增大 |
| C、NH3?H2O电离平衡向左移动 |
| D、溶液pH增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、pH=1的溶液中 K+、CrO42-、SO42-、NH4+ |
| B、饱和氯水中 Cl-、NO3-、Na+、SO32- |
| C、能使pH试纸变红的溶液 NH4+、Na+、SO42-、Fe2+ |
| D、FeCl2溶液中 K+、Na+、SO42-、AlO2- |
查看答案和解析>>
科目:高中化学 来源: 题型:
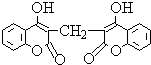 某农民偶然发现他的一头小母牛食用腐败草料后,血液不会凝固.化学家由此得到启发,从腐败草料中提取出结构简式为如图所示的双香豆素.下列关于双香豆素的推论中错误的是( )
某农民偶然发现他的一头小母牛食用腐败草料后,血液不会凝固.化学家由此得到启发,从腐败草料中提取出结构简式为如图所示的双香豆素.下列关于双香豆素的推论中错误的是( )| A、有望将它发展制得一种抗凝血药 |
| B、它无嗅并略具芳香味,因而可用来制备致命性出血型的杀鼠药 |
| C、它可由化合物和甲醛(HCHO)通过缩合反应制得 |
| D、它易溶于水、乙醇、乙醚等有机溶剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、在Zn跟ICl的反应中,ZnI2既是氧化产物又是还原产物 |
| B、在H2O跟ICl的反应中,ICl是氧化剂H2O是还原剂 |
| C、在Zn跟ICl的反应中,ZnCl2既是氧化产物又是还原产物 |
| D、在H2O跟ICl的反应中,ICl既是氧化剂又是还原剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:
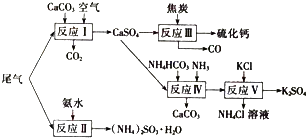
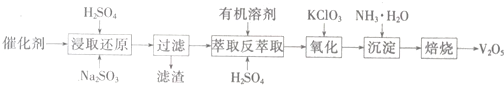
查看答案和解析>>
科目:高中化学 来源: 题型:
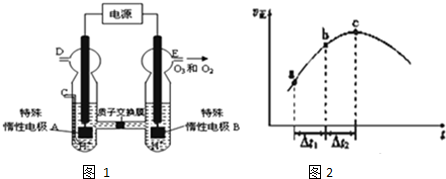
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com