
【题目】用足量的CO还原8 g铁的氧化物,把生成的CO2全部通入到过量的澄清石灰水中,得到的沉淀干燥后质量为15g,则此铁氧化物的化学式是
A. Fe2O3 B. FeO C. Fe3O4 D. Fe3O4和FeO的混合物
科目:高中化学 来源: 题型:
【题目】用下列实验装置进行相应实验,装置合理且能达到实验目的的是

A. 装置①:用氯化铵和氢氧化钙制NH3 B. 装置②:收集NO气体
C. 装置③:从饱和食盐水中提取氯化钠 D. 装置④:探究氧化性:KMnO4>Cl2>I2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在强酸性溶液中能大量共存,并且溶液为无色透明的离子组是( )
A.NH4+,Al3+,SO42-,NO3-
B.K+,Na+,S2-,Cl-
C.K+,NH4+,MnO4-,SO42-
D.Na+,K+,NO3-,HCO3-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向20 mL某浓度的AlCl3溶液中滴加2 molL-1的NaOH溶液时,得到Al(OH)3沉淀的质量(g)与所滴加NaOH溶液的体积(mL)关系如图所示,试回答下列问题:

(1)图中A点表示沉淀的化学式是_____,其物质的量是_____。
(2)反应至A点时消耗NaOH溶液的体积为________。
(3)AlCl3溶液的浓度为________。
(4)假设溶液中有0. 39克Al(OH)3沉淀,则此时用去NaOH溶液体积为____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室用燃烧法测定某固体有机物A的分子组成,测定装置如图所示(铁架台、铁夹、酒精灯等未画出):
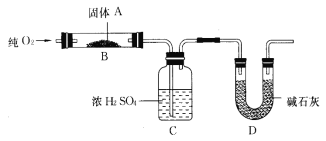
取17.1 g A放入B装置中,持续通入过量O2燃烧,生成CO2和H2O,请回答下列有关问题:
(1)通入过量O2的目的是_______________________________;
(2) D装置的作用是______________________________,有同学认为该套装置有明显的缺陷,需要改进,该同学判断的理由是___________________________;
(3)通过该实验,能否确定A中是否含有氧元素,其理由?_____________________________ ;
(4)若A的摩尔质量为342 g/mol,C装置增重9.9 g,D装置增重26.4 g,则A的分子式为______________________________;
(5)A可发生水解反应,1 mol A可水解生成2 mol同分异构体,则A在催化剂作用下水解的化学方程式为_______________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮元素能形成NH3、NO2、HNO3等多种化合物。
(1)实验室制取氨气的化学方程式为___________________________;用水吸收多余的氨气时,如将导管直接插入冷水中,会产生倒吸现象,产生该现象的原因为_________________。
(2)氨气是工业制备硝酸的原料,该过程中第一步反应的化学方程式为__________。
(3)将体积为VmL的试管充满NO2后倒扣在水中,见下图,充分反应后试管中的溶液体积为__________,欲使试管中NO2完全被吸收(假设试管中溶液的溶质不向水槽中扩散),还需进行的操作为_____________。
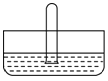
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列示意图与对应的反应情况符合的是
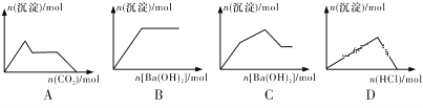
A. 向含0.01mol KOH和0.01mol Ca(OH)2的混合溶液中缓慢通入CO2至过量
B. 向NaHSO4溶液中逐滴加入Ba(OH)2溶液至过量
C. 向KAl(SO4)2溶液中逐滴加入Ba(OH)2溶液至过量
D. 向NaAlO2溶液中逐滴加入盐酸至过量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】可逆反应2SO2+O2![]() 2SO3,正反应速率分别用v(SO2)、v(O2)、v(SO3)(mol·L-1·min-1)表示,逆反应速率分别用v′(SO2)、v′(O2)、v′(SO3)(mol·L-1·min-1)表示,当反应达到化学平衡时,正确的关系是( )
2SO3,正反应速率分别用v(SO2)、v(O2)、v(SO3)(mol·L-1·min-1)表示,逆反应速率分别用v′(SO2)、v′(O2)、v′(SO3)(mol·L-1·min-1)表示,当反应达到化学平衡时,正确的关系是( )
①v(SO2)=v′(SO2) ②v(O2)=v′(SO2)=v(SO3)
③v(O2)=![]() v′(SO2) ④v′(SO2)=v′(O2)=v′(SO3)
v′(SO2) ④v′(SO2)=v′(O2)=v′(SO3)
A. ①②③④B. ①②③C. ②③④D. ①③
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)已知可逆反应:M(g)+N(g)![]() P(g)+Q(g) ΔH>0,请回答下列问题:
P(g)+Q(g) ΔH>0,请回答下列问题:
①在某温度下,反应物的起始浓度分别为c(M)=1 mol·L-1,c(N)=2.4 mol·L-1;达到平衡后,M的转化率为60%,此时N的转化率为________。
②若反应温度升高,M的转化率________(填“增大”、“减小”或“不变”)。
③若反应温度不变,反应物的起始浓度分别为c(M)=4 mol·L-1,c(N)=a mol·L-1;达到平衡后,c(P)=2 mol·L-1,a=________。
④若反应温度不变,反应物的起始浓度为c(M)=c(N)=c(P)=c(Q)=2mol·L-1,此时v(正)_____v(逆)(填“>”、“<”或“=”)
(2)合成氨工业对国民经济和社会发展具有重要的意义。其原理为:N2(g)+3H2(g)![]() 2NH3(g) ΔH=-92.4 kJ/mol,据此回答以下问题:
2NH3(g) ΔH=-92.4 kJ/mol,据此回答以下问题:
①根据温度对化学平衡的影响规律可知,对于该反应,温度越高,其平衡常数的值越________。
②对于合成氨反应而言,下列有关图像一定正确的是(选填序号)________。
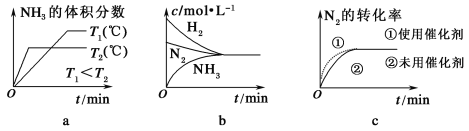
③相同温度下,有恒容密闭容器A和恒压密闭容器B,两容器中均充入1 mol N2和3 mol H2,此时两容器的体积相等。在一定条件下反应达到平衡状态,A中NH3的体积分数为a,放出热量Q1 kJ;B中NH3的体积分数为b,放出热量Q2 kJ。则:a________b(填“>”、“=”或“<”,下同),Q1________Q2,Q1________92.4。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com