
��15�֣�
��1����֪��
�״���ϩ����Ӧ�٣�2CH3OH(g)��C2H4 (g)��2H2O(g) ��H1����29��0 KJ��mol��1
�״���ˮ��Ӧ�ڣ�2CH3OH(g)��CH3OCH3(g)��H2O(g)��H2����24��0 KJ��mol��1
�Ҵ��칹����Ӧ�ۣ�CH3CH2OH(g)��CH3OCH3(g)) ��H3��+50��8 KJ��mol��1
����ϩ����ֱ��ˮ�Ϸ�ӦC2H4 (g)��H2O(g)��C2H5OH(g)�ġ�H�� KJ��mol��1
��2���ھ��Ʊ���ʳ��ˮ�м���̼����刺��Ʊ�С�մ�NaHCO3��������ȡ�Ȼ����Ϊ���ϻ��һ���ᴿΪ��ҵ�Ȼ�李�
��д�������Ʊ�С�մ�Ļ�ѧ����ʽ��__________________________________��
���˳�С�մ��ĸҺ��ȡ�Ȼ�������ַ�������ͨ�백����ȴ����ʳ�Σ����ˣ���ͨ������ȴ����ʳ�Σ����ˡ����з������������Ȼ�淋Ĵ��ȸ��ߣ���ԭ���� ������������ŵ�������Һ���� ��
��3��Ǧ���仯������������أ������豸��X���߷������ϵȡ�PbO2����PbO�����������Һ��Ӧ�Ƶã���Ӧ�����ӷ���ʽΪ ��PbO2Ҳ����ͨ��ʯīΪ�缫��Pb(NO3)2��Cu(NO3)2�Ļ����ҺΪ���Һ�����ȡ�����������ĵ缫��Ӧʽ �����Һ�м���Cu(NO3)2��ԭ���� ��
��14�֣� ��1��-45.8
��2�� ��NH4HCO3+NaCl��NaHCO3��+NH4Cl ��ĸҺ�к����Ȼ�泥�ͨ�백����ȴ����ʳ�Σ��������Ȼ�淋�������ֱ��ѭ��ʹ��
��3��PbO+ClO-= PbO2+Cl- Pb2++2H2O-2e- = PbO2��+ 4H+
�������������ͭ�������ᷢ��Pb2++2e- =Pb�� ������Ч����Pb2+��ʹPb2+�������ʽ��͡�
��������
�����������1�����ݸ�˹���ɣ���-��-�ۿɵ������Ȼ�ѧ����ʽ������ϩ����ֱ��ˮ�Ϸ�ӦC2H4 (g)��H2O(g)��C2H5OH(g)�ġ�H����-��-��=����24��0+29-50.8��kJ/mol=-45.8kJ/mol��
��2���ٸ��������ܽ�ȵIJ�ͬ���Ȼ��Ƶ��ܽ�ȴ���̼�����Ƶ��ܽ�ȣ������͵��Ȼ�����Һ�м���̼����泥�������̼�����Ƴ������Ȼ�泥���ѧ����ʽ��NH4HCO3+NaCl��NaHCO3��+NH4Cl��
��I��II�����������Ƿ�ͨ�백������ͨ�백�������Ȼ�淋�Ũ��������ʳ�κ����������������Ȼ�淋�������������I���˺����Һ�к��а��������Բ���ѭ��ʹ�ã�����II���˺����ҺΪ�Ȼ��ƣ���ֱ��ѭ��ʹ�ã�
��3��PbO��������Ʒ�Ӧ����PbO2��PbԪ�صĻ��ϼ����ߣ���ClԪ�صĻ��ϼ۽��ͣ����Դ���������ӱ���ԭΪ�����ӣ����ӷ���ʽ��PbO+ClO-= PbO2+Cl-�����ʱ����������������Ӧ����Ϊ�õ��ؿ���ȡPbO2������������Pb2+ʧȥ������ˮ�������PbO2���缫��Ӧʽ��Pb2++2H2O-2e- = PbO2��+ 4H+��������������ͭ���������������ӷŵ磬���������ŵ����Pb2+������Pb�����������ϵõ�PbO2���������٣�Pb2+�������ʽ��͡�
���㣺�����˹���ɵ�Ӧ�ã���ʵ�鷽���ķ������绯ѧ��Ӧԭ����Ӧ��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2014-2015����ʡ�߶���ѧ����ĩ��ѧ�Ծ��������棩 ���ͣ�ѡ����
�����йس����ܽ�ƽ���˵����ȷ����
A��Ksp(AB2)С��Ksp(CD)����AB2���ܽ��С��CD���ܽ��
B����AgCl�ij����ܽ�ƽ����ϵ�У���������ˮ��AgCl��Ksp����
C����AgI�ij����ܽ�ƽ����ϵ�У�����K2S���壬AgI������ת��ΪAg2S����
D����CaCO3�ij����ܽ�ƽ����ϵ�У�ͨ��CO2���壬�ܽ�ƽ�ⲻ�ƶ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ���㽭ʡ����3�½β������ۻ�ѧ�Ծ��������棩 ���ͣ�ѡ����
������Ԫ��X��Y��Z��W��Q��Ԫ�����ڱ��е�λ����ͼ��ʾ������XԪ��ԭ�����������������ڲ��������3����������˵����ȷ����
X | Y | ||
Z | W | Q |
A��X��W�������γ�Ħ��������ͬ�Ļ������������������Ϊ1��2
B����X��ZԪ�صij���������Ϊ���Ӿ���
C���������Ӧ��ˮ�������ԣ�W��Q
D��ԭ�Ӱ뾶��С��ϵ��Q>W>Z>Y
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ�����ʡ��ұ�и�����ѧ����ĩ�������ۻ�ѧ�Ծ��������棩 ���ͣ������
��15�֣��о�̼���仯��������Ҫ���塣
��1����ѧ����CO2��H2�����״���ȼ�ϡ�
��֪���״���ȼ���Ȧ�H= -726.5kJ/mol��������ȼ���Ȧ�H= -285.8kJ/mol��
���³�ѹ�£�CO2(g)��H2(g)��Ӧ����CH3OH(l)���Ȼ�ѧ����ʽ ��
��2��460��ʱ����4L�ܱ������г���1mol CO2��3.25mol H2����һ�������·�Ӧ�����CO2��CH3OH(g)�����ʵ�����ʱ��ı仯��ϵ��ͼ��ʾ��
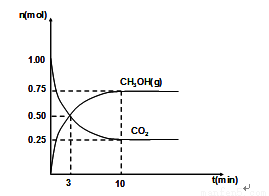
�ٴӷ�Ӧ��ʼ��3minʱ��H2O(g)��ƽ����Ӧ���� ��
�����д�ʩ�м��ܼӿ췴Ӧ��������ʹH2��ת����������� ��
A��ʹ�ø���Ч�Ĵ���
B����ԭ�������ٳ���1mol CO2
C����ԭ�������ٳ���1mol He
D�������������
E�����״���ʱ�������
�����÷�Ӧ���ʱ�Ϊ��H��������ʾ��ͼ��ȷ����˵����Ӧ�ﵽƽ��״̬����________��
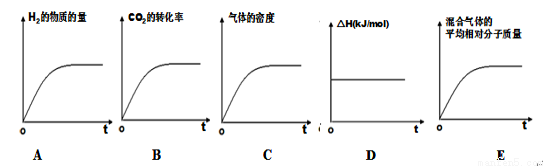
�ܸ������£��˷�Ӧ�Ļ�ѧƽ�ⳣ��Ϊ ��
��3����ѧ���о����֣��������õ������CO2��ԭΪ̼�⻯���ԭ������ͼ��ʾ���������Һ��һ�ּ��Σ�����CxHyΪC2H4�����ԭ�����ܷ�ӦʽΪΪ�� ��
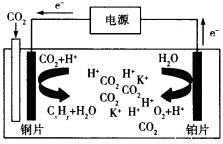
��4����֪
��ѧʽ | ����ƽ�ⳣ�� |
HCN | K=4.9��10-10 |
H2CO3 | K1=4.3��10-7��K2=5.6��10-11 |
��25��ʱ�����HCN��NaCN�Ļ����Һ��pH=11����c(HCN)/c(CN-)=_________��
����NaCN��Һ��ͨ������CO2��������Ӧ�����ӷ���ʽΪ��________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ�����ʡ��ұ�и�����ѧ����ĩ�������ۻ�ѧ�Ծ��������棩 ���ͣ�ѡ����
������ͼ��ʾװ�ý�������ʵ�飬�ܵó���Ӧʵ����۵���
ѡ�� | �� | �� | �� | ʵ����� |
|
A�� | ϡ���� | Na2S | Ư�۾���Һ | ���ԣ�����>������>������ | |
B�� | Ũ���� | KMnO4 | Na2S��Һ | �����ԣ�KMnO4> Cl2>S | |
C�� | Ũ��ˮ | NaOH | ��̪ | ���ԣ�NaOH >NH3��H2O | |
D�� | Ũ���� | Na2SO3 | BaCl2��Һ | SO2������Ա��ξ�����Ӧ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ�����ʡ������ѧ�ڵ�һ���¿������ۺϻ�ѧ�Ծ��������棩 ���ͣ�ѡ����
һ�����͵��Ҵ���أ����û����������ܼ�������ܷ�ӦΪ��C2H5OH +3O2 �� 2CO2 +3H2O,���ʾ����ͼ,����˵����ȷ����

A��a��Ϊ��ص�����
B����ع���ʱ������a���ص��߾������ٵ�b��
C����ظ����ĵ缫��ӦΪ��4H+ + O2 + 4e�� = 2H2O
D����ع���ʱ,1mol�Ҵ�������ʱ����12mol����ת��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ�����ʡ�����и�����ѧ����Ͽ������ۻ�ѧ�Ծ��������棩 ���ͣ�ʵ����
[ѡ��2����ѧ�뼼��]��15�֣�����������Ϊ���Ͻ��ά���ء��������仯�����ڹ�ҵ���������Ź㷺��Ӧ�á��ӷϷ�����(��Ҫ�ɷ���V2O5��VOSO4��K2SO4��SiO2��)�л���V2O5����������ͼ���£�

��ش�
��1�����в����ǰ�����Ϸ����������Ŀ���� ��д��������з���������ԭ��Ӧ�����ӷ���ʽ ��
��2��ʵ�����н�����ȡ��Һ����ʱ���õ��IJ��������� ���ڢ۱仯���̿ɼ�Ϊ(��ʽR��ʾVO2+��HA��ʾ�л���ȡ��)R2(SO4)n(ˮ��)+2n HA(�л���) 2RAn(�л���) + n H2SO4(ˮ��)��Ϊ��ߢ�����ȡ�ٷ��ʣ�Ӧ��ȡ�Ĵ�ʩ��____ ��
2RAn(�л���) + n H2SO4(ˮ��)��Ϊ��ߢ�����ȡ�ٷ��ʣ�Ӧ��ȡ�Ĵ�ʩ��____ ��
��3��25��Cʱ��ȡ����������������õ��������ʺ���ҺpH֮���ϵ���±���
pH | 1.3 | 1.4 | 1.5 | 1.6 | 1.7 | 1.8 | 1.9 | 2.0 | 2.1 |
��������% | 88.1 | 94.8 | 96.5 | 98.0 | 98.8 | 98.8 | 96.4 | 93.1 | 89.3 |
ͨ���ϱ����ݷ�������ʵ�������У����м��백ˮ��������Һ�����pHΪ______��
��4���ڱ���NH4VO3�Ĺ����У����������ļ���ֵ�������꣩���¶ȱ仯����������ͼ��ʾ����NH4VO3�ڷֽ������ ��

A���ȷֽ�ʧȥH2O���ٷֽ�ʧȥNH3
B���ȷֽ�ʧȥNH3���ٷֽ�ʧȥH2O
C��ͬʱ�ֽ�ʧȥH2O��NH3
D��ͬʱ�ֽ�ʧȥH2��N2��H2O
��5��ȫ��Һ���ܵ�صĵ������ҺΪVOSO4��Һ����صĹ���ԭ��ΪVO2+��V2+��2H+ VO2+��H2O��V3+����طŵ�ʱ�����ĵ缫��ӦʽΪ ��
VO2+��H2O��V3+����طŵ�ʱ�����ĵ缫��ӦʽΪ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ�긣��ʡ�����и�������������ۻ�ѧ�Ծ��������棩 ���ͣ�ѡ����
��ҵ�ϣ���ǿ�����������õ�ⷨ��ȥ��ˮ�е�CN-��װ����ͼ��ʾ�����η����ķ�Ӧ��:
��CN- ��2e- +2OH- �TCNO- +H2O
��2Cl- һ2e�T�TCl2 ��
��3Cl2 +2CNO- +8OH-�TN2 +6Cl-ʮ2CO32-+4H2O
����˵����ȷ����

A�����缫�Ϸ����ķ�ӦΪFeһ2eһ�TFe2+
B��ͨ���������ҺpH��������
C��Ϊ��ʹ����������������Ҫ���ϲ���NaCl
D����ȥ1 mol CN-�����·������ת��5 mol����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015�㶫ʡ��������ɽ����ѧ�ڸ�һ��ѧ��ĩ�Ծ��������棩 ���ͣ�ѡ����
Ư���������ƣ�NaClO2���ڳ�����ڰ����ɱ���һ�꣬�����ᣨHClO2Ϊ���ᣩ���ȶ��ɷֽ⣬��Ӧ�����ӷ���ʽΪ��5HClO2=4ClO2��+H��+Cl��+2H2O����NaClO2��Һ�еμ�H2SO4����ʼʱHClO2�ֽⷴӦ��Ӧ���������ӦѸ�٣���ԭ����
A�������������£��������Ƶ���������ǿ
B����Һ�е�Cl���������
C��ClO2�ݳ���ʹ��Ӧ��������Ũ�Ƚ���
D����Һ�е�H���������
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com