
��15�֣��о�̼���仯��������Ҫ���塣
��1����ѧ����CO2��H2�����״���ȼ�ϡ�
��֪���״���ȼ���Ȧ�H= -726.5kJ/mol��������ȼ���Ȧ�H= -285.8kJ/mol��
���³�ѹ�£�CO2(g)��H2(g)��Ӧ����CH3OH(l)���Ȼ�ѧ����ʽ ��
��2��460��ʱ����4L�ܱ������г���1mol CO2��3.25mol H2����һ�������·�Ӧ�����CO2��CH3OH(g)�����ʵ�����ʱ��ı仯��ϵ��ͼ��ʾ��
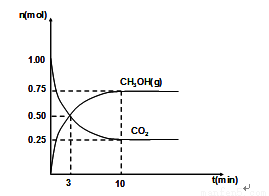
�ٴӷ�Ӧ��ʼ��3minʱ��H2O(g)��ƽ����Ӧ���� ��
�����д�ʩ�м��ܼӿ췴Ӧ��������ʹH2��ת����������� ��
A��ʹ�ø���Ч�Ĵ���
B����ԭ�������ٳ���1mol CO2
C����ԭ�������ٳ���1mol He
D�������������
E�����״���ʱ�������
�����÷�Ӧ���ʱ�Ϊ��H��������ʾ��ͼ��ȷ����˵����Ӧ�ﵽƽ��״̬����________��
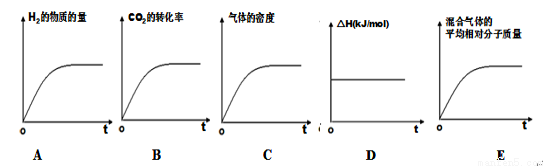
�ܸ������£��˷�Ӧ�Ļ�ѧƽ�ⳣ��Ϊ ��
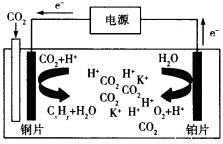
��3����ѧ���о����֣��������õ������CO2��ԭΪ̼�⻯���ԭ������ͼ��ʾ���������Һ��һ�ּ��Σ�����CxHyΪC2H4�����ԭ�����ܷ�ӦʽΪΪ�� ��
��4����֪
��ѧʽ | ����ƽ�ⳣ�� |
HCN | K=4.9��10-10 |
H2CO3 | K1=4.3��10-7��K2=5.6��10-11 |
��25��ʱ�����HCN��NaCN�Ļ����Һ��pH=11����c(HCN)/c(CN-)=_________��
����NaCN��Һ��ͨ������CO2��������Ӧ�����ӷ���ʽΪ��________________��
��15�֣���
��1��CO2(g)+3H2(g)=CH3OH(l)+H2O(l) ��H= -130.9 kJ/mol ��2�֣�
��2����0.042mol/(l��min) ��1�֣� ����BD ��2�֣�����BE ��2�֣�����36 ��2�֣���
��3��2CO2+ 2H2O =C2H4+3O2 ��2�֣�
��4����2.0��10-2 ��2�֣�����CN-+ CO2+ H2O =HCN+ HCO3- ��2�֣�
��������
�����������1���״�ȼ�յ��Ȼ�ѧ����ʽ��CH3OH(l)+3/2O2(g)= CO2(g)+ 2H2O(l) ��H= -726.5kJ/mol������ȼ�յ��Ȼ�ѧ����ʽ��H2(g)+1/2O2(g)= H2O(l) ��H= -285.8kJ/mol�����ݸ�˹���ɣ���������ȥ����ʽ����3��ȥ��ʽ�ɵ������������̼��Ӧ���ɼ״����Ȼ�ѧ����ʽ����ΪCO2(g)+3H2(g)=CH3OH(l)+H2O(l) ��H= -130.9 kJ/mol��
��2���ٴӷ�Ӧ��ʼ��3minʱ���״������ʵ�������0.50mol����ˮ���������ʵ���Ҳ����0.50mol������H2O(g)��ƽ����Ӧ������0.50mol/4L/3min=0.042 mol/(l��min)��
��A��ʹ�ô�����ֻ�ܼӿ췴Ӧ���ʣ����ܸı�ƽ�⣬����������ת���ʲ��䣬����B����ԭ�������ٳ���1mol CO2����Ӧ���Ũ������Ӧ���ʼӿ죬ͬʱƽ�������ƶ�����������ת����������ȷ��C����ԭ�������ٳ���1mol He����������ѹǿ���������ʵ�Ũ�Ȳ��䣬��Ӧ���ʺ�ƽ�ⶼ���䣬����D����С�������������ѹǿ����Ӧ���ʼӿ죬ͬʱƽ�������ƶ���������ת����������ȷ����ѡBD��
��A����������ʼ���ʵ�������0�������ⲻ��������B��������̼��ת���������ﵽƽ��ʱ������������ȷ��C����Ϊ�Ǻ���������������ܶ�ʼ�ղ��䣬�����ж�Ϊƽ��״̬������D��һ����ѧ��Ӧ�ķ�Ӧ��ֻ�뷴Ӧ�����������״̬�йأ����Է�Ӧ��ʼ�ղ��䣬����E���÷�Ӧ����������ʵ��������仯�Ŀ��淴Ӧ�����������ƽ����Է�������Ҳ�����仯���ﵽƽ��ʱ�����ٱ仯����ȷ����ѡBE��
�ܸ���ͼ���֪��ƽ��ʱ�״������ʵ�����0.75mol��������̼�����ʵ�����0.25mol����ˮ���������ʵ�����0.75mol�����������ʵ�����3.25-0.75��3=1mol������ƽ�ⳣ���Ķ��壬��������µ�ƽ�ⳣ��K=(0.75/4)2/(1/4))30.25/4=36��
��3�����ݵ��ӵ��ƶ������֪��ͭ��Ϊ����������Ϊ�����������Ƕ�����̼�õ������������ӽ��Ϊ��ϩ��ˮ��������ˮʧȥ���ӣ����������������ӣ������ܷ�Ӧ�Ƕ�����̼��ˮ��Ӧ������ϩ����������ѧ����ʽ��2CO2+ 2H2O =C2H4+3O2��
��4������ΪHCN�ĵ��볣��K=4.9��10-10=c(H+) c(CN-)/ c(HCN)��pH=11����c(H+)=10-11mol/L����c(HCN)/c(CN-)= c(H+)/K=2.0��10-2��
����NaCN��Һ��ͨ������CO2�����ݱ�����ĵ��볣����֪�����ԣ�H2CO3��HCN��HCO3-������NaCN��̼�����ƣ�����������̼���ƺ�HCN����Ӧ�Ļ�ѧ����ʽΪNaCN+H2O+CO2=HCN+NaHCO3��
���㣺�����˹���ɵ�Ӧ�ã���ѧƽ��״̬���жϣ���ѧƽ���ƶ���Ӧ�ã����볣����Ӧ��


 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2014-2015����ʡ��һ��ѧ����ĩ��ѧ�Ծ��������棩 ���ͣ�ѡ����
��25�桢1��105Paʱ����������H2��Cl2��CO2��C2H2����������
A��H2��������� B��C2H2ԭ�������
C��CO2�ܶ���� D��Cl2���Ӽ�ƽ���������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015����ʡ�߶���ѧ����ĩ���Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
���и������ʵľ����У���ѧ��������ͬ����������Ҳ��ͬ����
A��SiO2��SO2 B��NaCl��HCl
C��CO2��H2O D��CH4��KCl
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ���㽭ʡ�����и���һģ���ۻ�ѧ�Ծ��������棩 ���ͣ��ƶ���
(18��)��A��B��C��D��E��F�Ƕ�����Ԫ����ɵ���ѧ���������ʣ����ǵ�ת����ϵ��ͼ��ʾ(���ַ�Ӧ������ȥ)��
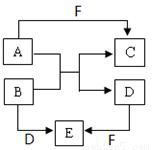
��1��������ת�����Ƿ�������ԭ��Ӧ��B��D��E����ͬ�ֽ���Ԫ�أ�FΪǿ����ֲ�����ȥ��
��B+D��E�����ӷ���ʽΪ ��CΪͬ����Ԫ�ع��ɵ�1��1�ͻ������C�ĵ���ʽΪ ��
��2����A��D��FΪ���ʣ�B��C��EΪ�����BΪ���ַǽ���Ԫ������ɵĻ������E�Ļ�ѧʽΪ ��A+B��C+D�Ļ�ѧ����ʽΪ ��
�ס��Ҷ��Ƕ�Ԫ���廯�����32g�ķ�ĩ��������Ũ���Ტ���ȣ���ȫ�ܽ����ɫ��Һ�������Һ�м�������Ba(NO3)2��Һ�����ˡ�ϴ�ӡ�����ó���46.6g����Һ���ٵμ�NaOH��Һ���ֳ�����ɫ������
���ҵĿ�ʯ��Ȼ���д����϶࣬��ȡһ�����ң�����ϡ����ʹ��ȫ���ܽ⣬��Һ��ΪA��B���ȷݣ���A�м�����������������Һ�����ˡ�ϴ�ӡ����յú���ɫ����28g���������������ɫ��������Ԫ����ͬ����B�м���8.0gͭ�۳�ַ�Ӧ����ˡ�ϴ�ӡ������ʣ�����1.6g��
��1��д�����ɼ������ӵĽṹʾ��ͼ ��32g��������Ũ�����з�Ӧת�Ƶĵ�����Ϊ ���������������г�����յĻ�ѧ����ʽΪ ��
��2���ҵĻ�ѧʽ ��ϡ�����ܽ��ҵĻ�ѧ����ʽΪ ��
��3�����������������г�����յ��������ͨ��һ����A��Һ�У��÷�Ӧ�����ӷ���ʽΪ �����ʵ��֤���˲���Ӧ�����Һ�н���Ԫ�صĻ��ϼ� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ���㽭ʡ�����и���һģ���ۻ�ѧ�Ծ��������棩 ���ͣ�ѡ����
����˵����ȷ����
A���Թܡ��ձ���������������Բ����ƿ�����þƾ��Ƽ���
B���ò�����պȡ������ˮ������pH��ֽ�ϣ�Ȼ�����ɫ�����գ��ɲⶨ������ˮ��pHֵ
C��������������ͭ����Һ���Լ������ᡢ�����Ǻ͵���������Һ
D���ñ�NaOH��Һ�ζ����ᣬ�ζ��ܼ��첿���ڵζ�ǰ�����ݣ��ζ��յ�ʱ�������ݣ���ⶨ�����ƫ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ�����ʡ��ұ�и�����ѧ����ĩ�������ۻ�ѧ�Ծ��������棩 ���ͣ�ѡ����
NA��ʾ�����ӵ�������ֵ�������£���ȥ��ͼ��ʾװ���еIJ���Ƭ��ʹ���������ַ�Ӧ������˵����ȷ����
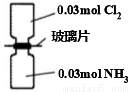
A����Ӧǰ����������Ϊ1.344L
B��װ���в��������İ�ɫ����
C����Ӧǰ������������䣬��Ϊ0.06 NA��
D��������������ˮ��������Һ����0.01 NA��NH4+
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ�����ʡ������ѧ�ڵ�һ���¿������ۺϻ�ѧ�Ծ��������棩 ���ͣ������
��15�֣�
��1����֪��
�״���ϩ����Ӧ�٣�2CH3OH(g)��C2H4 (g)��2H2O(g) ��H1����29��0 KJ��mol��1
�״���ˮ��Ӧ�ڣ�2CH3OH(g)��CH3OCH3(g)��H2O(g)��H2����24��0 KJ��mol��1
�Ҵ��칹����Ӧ�ۣ�CH3CH2OH(g)��CH3OCH3(g)) ��H3��+50��8 KJ��mol��1
����ϩ����ֱ��ˮ�Ϸ�ӦC2H4 (g)��H2O(g)��C2H5OH(g)�ġ�H�� KJ��mol��1
��2���ھ��Ʊ���ʳ��ˮ�м���̼����刺��Ʊ�С�մ�NaHCO3��������ȡ�Ȼ����Ϊ���ϻ��һ���ᴿΪ��ҵ�Ȼ�李�
��д�������Ʊ�С�մ�Ļ�ѧ����ʽ��__________________________________��
���˳�С�մ��ĸҺ��ȡ�Ȼ�������ַ�������ͨ�백����ȴ����ʳ�Σ����ˣ���ͨ������ȴ����ʳ�Σ����ˡ����з������������Ȼ�淋Ĵ��ȸ��ߣ���ԭ���� ������������ŵ�������Һ���� ��
��3��Ǧ���仯������������أ������豸��X���߷������ϵȡ�PbO2����PbO�����������Һ��Ӧ�Ƶã���Ӧ�����ӷ���ʽΪ ��PbO2Ҳ����ͨ��ʯīΪ�缫��Pb(NO3)2��Cu(NO3)2�Ļ����ҺΪ���Һ�����ȡ�����������ĵ缫��Ӧʽ �����Һ�м���Cu(NO3)2��ԭ���� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ�����ʡ�����и�����ѧ����Ͽ������ۻ�ѧ�Ծ��������棩 ���ͣ�ѡ����
���мס��ҡ����������ֶ�����Ԫ�أ�����֮��Ĺ�ϵ���£�
��ԭ�Ӱ뾶���ף������ң���
��ԭ�ӵ���������������+��=��+��=8
��ԭ�ӵĺ�����Ӳ�������>��=��=2��
������Ԫ�ص���Ҫ���ϼۣ��������+�����=2
������˵������ȷ����
A����Ԫ�ص��������5�����ӣ����⻯�ﺬ�м��Լ�
B������Ԫ���б��ķǽ�������ǿ��������������Ӧ�ĺ�����������ǿ
C����Ԫ�ص��������Ӧ��ˮ��������Ԫ������������Ӧˮ����ǡ����ȫ��Ӧ�γɵ�����Һ������
D���ҡ�����Ԫ���γɵļ��⻯���ȶ��Ա���ǿ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ�긣��ʡ�����и�����ѧ����������ۻ�ѧ�Ծ� �������棩 ���ͣ�ѡ����
������ʵ��˵��̼�ķǽ�����ǿ�ڹ����
A��2C+SiO2=Si+2CO B���ȶ��ԣ�CH4>SiH4
C��CaCO3+SiO2=CaSiO3+CO2 D�����ʯ�����磬������ܵ���
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com