
【题目】氯化苄(C6H5CH2Cl)为无色液体,是一种重要的有机化工原料。现在实验室模拟工业上用甲苯与干燥氯气在光照条件下加热反应合成氯化苄、分离出氯化苄并检验样品的纯度,其装置(夹持装置略去)如图所示:

回答下列问题:
(1)仪器E的名称是_____________;其作用是_______________________________________。
(2)装置B中的溶液为___________________。
(3)用恒压滴液漏斗代替分液漏斗的优点是__________________________________________。
(4)装置A中反应的离子方程式为__________________________________________________。
(5)反应结束后,关闭K1和K2,打开K3,加热三颈烧瓶,分馏出氯化苄,应选择温度范围为______℃。
物质 | 溶解性 | 熔点(℃) | 沸点(℃) |
甲苯 | 极微溶于水,能与乙醇、乙醚等混溶 | -94.9 | 110 |
氯化苄 | 微溶于水,易溶于苯、甲苯等有机溶剂 | -39 | 178.8 |
二氯化苄 | 不溶于水,溶于乙醇、乙醚 | -16 | 205 |
三氯化苄 | 不溶于水,溶于乙醇、乙醚和苯 | -7 | 220 |
(6)检测氯化苄样品的纯度:
①称取13.00g样品于烧杯中,加入50.00mL 4 molL-1 NaOH水溶液,水浴加热1小时,冷却后加入35.00mL 40% HNO3,再将全部溶液转移到容量瓶中配成100mL溶液。取20.00mL溶液于试管中,加入足量的AgNO3溶液,充分振荡,过滤、洗涤、干燥,称量固体质量为2.87g,则该样品的纯度为_____%(结果保留小数点后1位)。
②实际测量结果可能偏高,原因是__________________________________________________。
【答案】球形冷凝管 导出Cl2、HCl气体,冷凝回流甲苯 饱和食盐水 使漏斗与烧瓶内压强一致,液体顺利流下 2MnO4-+10Cl-+16H+=2Mn2++5Cl2↑+8H2O 178.8-205 97. 3 样品混有二氯化苄、三氯化苄等杂质
【解析】
(1)根据装置图回答仪器E的名称;仪器E可以冷凝回流甲苯,导出Cl2、HCl气体;(2)装置A制取的氯气中含有杂质氯化氢,据此分析B装置的试剂;(3)恒压滴液漏斗使漏斗与烧瓶内压强一致,液体顺利流下;(4)装置A中高锰酸钾与浓盐酸反应生成氯化钾、氯化锰、氯气和水;(5)分馏出氯化苄温度应高于氯化苄的沸点,低于二氯化苄的沸点;(6)根据关系式![]() 计算样品纯度。二氯化苄、三氯化苄中氯元素的质量分数大于氯化苄;
计算样品纯度。二氯化苄、三氯化苄中氯元素的质量分数大于氯化苄;
(1)根据装置图可知,仪器E的名称是球形冷凝管;冷凝管E的作用是导出Cl2、HCl气体,冷凝回流甲苯;(2)装置A制取的氯气中含有杂质氯化氢,装置B的作用是除去氯气中的氯化氢,所以B中的试剂是饱和食盐水;(3)用恒压滴液漏斗代替分液漏斗的优点是使漏斗与烧瓶内压强一致,液体顺利流下;(4)装置A中高锰酸钾与浓盐酸反应生成氯化钾、氯化锰、氯气和水,反应的离子方程式为2MnO4-+10Cl-+16H+=2Mn2++5Cl2↑+8H2O;(5)分馏出氯化苄温度应高于氯化苄的沸点,低于二氯化苄的沸点,所以应选择温度范围是178.8-205℃;(6)设样品中C6H5CH2Cl的质量为xg;
![]()
126.5g 143.5g
xg 2.87![]()
x=12.65g
样品纯度为![]() 97.3%,
97.3%,
二氯化苄、三氯化苄中氯元素的质量分数大于氯化苄,样品若混有二氯化苄、三氯化苄等杂质会使测量结果偏高。


 尖子生新课堂课时作业系列答案
尖子生新课堂课时作业系列答案 英才计划同步课时高效训练系列答案
英才计划同步课时高效训练系列答案科目:高中化学 来源: 题型:
【题目】如图是在法国拍卖会拍卖的我国圆明园兽首﹣﹣兔首和鼠首,拍卖台上渴望回家的铜器兔首和鼠首看上去仍熠熠生辉.下列对其原因的分析,最可能的是( )

A.它们的表面都电镀上了一层耐腐蚀的黄金
B.环境污染日趋严重,它们表面的铜绿被酸雨溶液洗去
C.铜的活动性比氢弱,因此不易被氧化
D.它们是含一定比例金、银、锡、锌的铜合金
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于有机化合物的说法正确的是( )
A. 分子式为C8H8O2的芳香族化合物中属于羧酸的同分异构体有3种
B. 麦芽糖的水解产物有两种,且互为同分异构体
C. 等质量的苯和苯乙烯(![]() )完全燃烧,消耗氧气的体积相同
)完全燃烧,消耗氧气的体积相同
D. 分子式为C4H8Cl2且含有两个甲基的有机物有4种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度时,在2 L的密闭容器中,X、Y、Z三种物质的量随时间的变化曲线如图所示。
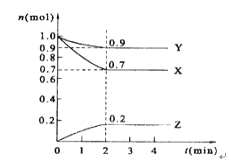
(1)X的转化率是_______;
(2)由图中所给数据进行分析,该反应的化学方程式为_______________;
(3)反应从开始至2分钟末,用Z的浓度变化表示的平均反应速率为v(Z)=__________;
(4)当反应进行到第___min,该反应达到平衡。若三种物质都是气体,平衡时Y所占体积的百分比为______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究CO2与CH4的反应使之转化为CO和H2,对减缓燃料危机,减少温室效应具有重要的意义。
(1)已知CH4(g)+CO2(g)![]() 2CO(g)+2H2(g) △H=+248kJ·mol-1、△S=310J mol-1·K-1,该反应能自发进行的温度范围为____________________。
2CO(g)+2H2(g) △H=+248kJ·mol-1、△S=310J mol-1·K-1,该反应能自发进行的温度范围为____________________。
(2)在密闭恒容容器中通入物质的量浓度均为0.1 mol·L-1的CH4与CO2,在一定条件下发生反应
CH4(g)+CO2(g)![]() 2CO(g)+2H2(g),测得CH4的平衡转化率与温度、压强的关系如图所示。
2CO(g)+2H2(g),测得CH4的平衡转化率与温度、压强的关系如图所示。

①工业生产时一般会选用P4和1250℃进行合成,请解释其原因__________________________。
②在压强为P4、1100℃的条件下,该反应5min时达到平衡点X,则用CO表示该反应的速率为________________,该温度下,反应的平衡常数为_____________________(保留3位有效数字)。
(3) CO和H2在工业上还可以通过反应C(s)+H2O(g) ![]() CO(g)+H2 (g)来制取,在恒温恒容下,如果从反应物出发建立平衡,可认定已达平衡状态的是________________________。
CO(g)+H2 (g)来制取,在恒温恒容下,如果从反应物出发建立平衡,可认定已达平衡状态的是________________________。
A.体系压强不再变化 B.H2、CO和H2O的物质的量之比为1:1:1
C.混合气体的密度保持不变 D.气体平均相对分子质量保持不变
(4) 甲烷燃料电池可以提升能量利用率。下图是利用甲烷燃料电池电解100mL 1mol·L -1食盐水,电解一段时间后,收集到标准状况下的氢气2.24L(设电解后溶液体积不变)。
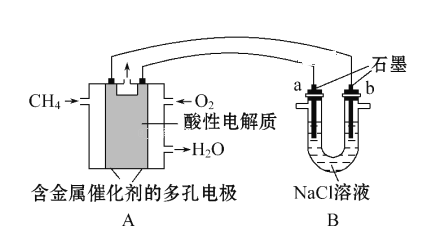
①甲烷燃料电池的负极反应式: _____________________________________________
②电解后溶液的pH= __________________________(忽略氯气与氢氧化钠溶液反应)。
③阳极产生气体的体积在标准状况下是 __________________L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学反应中的能量变化是由化学反应中旧化学键断裂时吸收的能量与新化学键形成时放出的能量不同引起的。如图为N2(g)和O2(g)反应生成NO(g)过程中的能量变化:
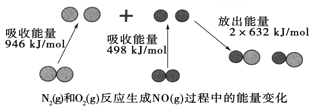
下列说法中正确的是
A. 1mol N2(g)和1 mol O2(g)完全反应放出的能量为180 kJ
B. 通常情况下,N2(g)和O2(g)混合能直接生成NO
C. 1 mol N2(g)和1 mol O2(g)具有的总能量小于2 mol NO(g)具有的总能量
D. NO是一种酸性氧化物,能与NaOH溶液反应生成盐和水
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)已知:H2(g)+O2(g)H2O(g),反应过程中能量变化如图所示,则:
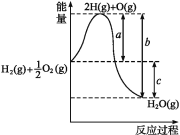
①a、b、c分别代表什么意义?a_;b_;c_。
②该反应是_反应(填“吸热”或“放热”),ΔH_0(填“>”或“<”)。
(2)发射“天宫”一号的火箭使用的推进剂是液氢和液氧,这种推进剂的优点是__________。(请写两条)
(3)已知:H2(g)+O2(g)H2O(l) ΔH=-285.8 kJ·mol-1
H2(g)H2(l) ΔH=-0.92 kJ·mol-1
O2(g)O2(l) ΔH=-6.84 kJ·mol-1
H2O(l)H2O(g) ΔH=+44.0 kJ·mol-1
请写出液氢和液氧生成气态水的热化学方程式:________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】组成糖原和核酸的化学元素分别是
A. C H O N和C H O N P S
B. C H O和C H O N P
C. C H O P和C H O N S
D. C H O S和C H O N S
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com