
����Ŀ���ο���ͼ����Ҫ��ش��������⣺ 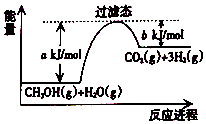
��1���״����ӽ���Ĥȼ�ϵ�ؽ��״�����ת��Ϊ������һ��ԭ����CH3OH��g����H2O��Ӧ����CO2��H2 �� ���ڷ�Ӧ��ϵ�м����������Ӧ������������Ӧ��� a�ı仯�������������С���������䡱������Ӧ�ȡ�H�ı仯�������������С���������䡱������д��CH3OH��g����H2O��g����Ӧ���Ȼ�ѧ����ʽ ��
��2���״����ӽ���Ĥȼ�ϵ���н��״�����ת��Ϊ��������һ�ַ�Ӧԭ���ǣ�
CH3OH��g��+ ![]() O2��g��CO2��g��+2H2��g����H=��c kJ/mol
O2��g��CO2��g��+2H2��g����H=��c kJ/mol
��֪H2O��g��H2O��l����H=��d kJ/mol��
��״�ȼ���ȵ��Ȼ�ѧ����ʽΪ ��
���𰸡�
��1����С�����䣻CH3OH��g��+H2O��g��=CO2��g��+3H2��g����H=+��a��b��kJ/mol
��2��CH3OH��g��+ ![]() O2��g��=CO2��g��+2H2O��l����H=��2a��2b+3c+2d��kJ/mol
O2��g��=CO2��g��+2H2O��l����H=��2a��2b+3c+2d��kJ/mol
���������⣺��1���������ͷ�Ӧ�Ļ�ܣ��ӿ췴Ӧ���ʣ���a��С�����������ܸı��ܣ�����Ӧ�ȡ�H���䣬��Ӧ����ͼ������������������ڷ�Ӧ�������������Ϊ���ȷ�Ӧ����ͼ��֪��1mol �״���1mol ˮ������Ӧ����CO2���������յ�����Ϊ��a��b��kJ����Ӧ�Ȼ�ѧ����ʽΪ��CH3OH��g��+H2O��g��=CO2��g��+3H2��g����H=+��a��b��kJ/mol���ʴ�Ϊ����С�� ���䣻CH3OH��g��+H2O��g��=CO2��g��+3H2��g����H=+��a��b��kJ/mol����2����֪����CH3OH��g��+ ![]() O2��g��=CO2��g��+2H2��g����H=c kJ/mol��
O2��g��=CO2��g��+2H2��g����H=c kJ/mol��
��H2O��g��=H2O��l����H=d kJ/mol����CH3OH��g��+H2O��g��=CO2��g��+3H2��g����H=+��a��b��kJ/mol�����ݸ�˹���ɢ١�3��2�����۩��ڣ��ɵã�CH3OH��g��+ ![]() O2��g��=CO2��g��+2H2O��l����H=��2a��2b+3c+2d��kJ/mol���ʴ�Ϊ��CH3OH��g��+
O2��g��=CO2��g��+2H2O��l����H=��2a��2b+3c+2d��kJ/mol���ʴ�Ϊ��CH3OH��g��+ ![]() O2��g��=CO2��g��+2H2O��l����H=��2a��2b+3c+2d��kJ/mol��
O2��g��=CO2��g��+2H2O��l����H=��2a��2b+3c+2d��kJ/mol��
��1���������ͷ�Ӧ�Ļ�ܣ��ӿ췴Ӧ���ʣ���a��С�����������ܸı��ܣ�����Ӧ�ȡ�H���䣮����ͼ���֪��Ӧ��=akJ/mol��bkJ/mol������CH3OH��g����H2O��g����Ӧ���Ȼ�ѧ����ʽΪCH3OH��g��+H2O��g��=CO2��g��+3H2��g����H=+��a��b��kJ/mol����2����֪������CH3OH��g��+ ![]() O2��g��=CO2��g��+2H2��g����H=c kJ/mol����H2O��g��=H2O��l����H=d kJ/mol����CH3OH��g��+H2O��g��=CO2��g��+3H2��g����H=+��a��b��kJ/mol�����ݸ�˹���ɢ١�3��2�����۩��ڣ��ɵã�
O2��g��=CO2��g��+2H2��g����H=c kJ/mol����H2O��g��=H2O��l����H=d kJ/mol����CH3OH��g��+H2O��g��=CO2��g��+3H2��g����H=+��a��b��kJ/mol�����ݸ�˹���ɢ١�3��2�����۩��ڣ��ɵã�


 ��У����ϵ�д�
��У����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪����1mol H2��g���е�H��H����Ҫ����436.4KJ������������1mol O2��g���еĹ��ۼ���Ҫ����498KJ������������H2O��g���е�1mol H��O���ܷų�462.8KJ������������˵����ȷ���ǣ�������
A.����1 mol H2O�еĻ�ѧ����Ҫ����925.6 KJ������
B.2H2��g��+O2��g���T2H2O��g����H=��480.4 KJ?mol��1
C.2H2O��l���T2H2��g��+O2��g����H=471.6 KJ?mol��1
D.H2��g��+ ![]() O2��g���TH2O��l����H=��240.2KJ?mol��1
O2��g���TH2O��l����H=��240.2KJ?mol��1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������Զ�������г���Ӧ��ԭ���ԭ���Ĵ���������ͼΪ��صĹ���ʾ��ͼ��������ɢ���봫�����������е缫�Ϸ�����Ӧ���������ͻ���յ����źţ��±��г��˴������弰���е缫�ϲ��ַ�Ӧ���
�������� | ���ֵ缫��Ӧ���� |
NO2 | NO |
Cl2 | HCl |
CO | CO2 |
H2S | H2SO4 |
������˵������ȷ���ǣ� ��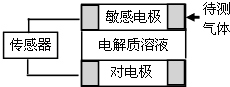
A.����������ʱ�����е缫�����������
B.���Cl2����ʱ�����е缫�ĵ缫��ӦΪ��Cl2+2e���T2Cl��
C.���H2S����ʱ���Ե缫����������Ե缫�ϵĵ缫��ӦʽΪO2+2H2O+4e���T4OH��
D.���H2S��CO���������ͬ�����ݿ�������ʱ���������ϲ����ĵ�����С��ͬ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������ˮ���¶ȼƴ��飬������ˮ���ϸ���һ�������Ա����ж����������ǣ� ��
A.ɳ��B.���C.ʯ��D.��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ͼ����ѧ��ѧ�г�������֮���һЩ��Ӧ��ϵ�����в��ֲ���δд���������£�X��H�ǹ��壬����X�������ӻ����1 mol X�ֽ�õ�A��B��C�����ʵ���֮��Ϊ1 : 1 : 2 ; B��G��Һ�壬�����Ϊ���塣
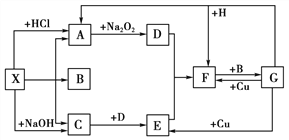
�Խ�����и��⣺
��1��д���������ʵĻ�ѧʽ��X________��B________��G______________
��2��д�����з�Ӧ�Ļ�ѧ����ʽ��
C��D��E��______________
A��D��______________
G + H��A+F��______________
��3��д�����з�Ӧ�����ӷ���ʽ��
G��Cu��E��______________
��4����ҵ�Ϻϳ�C���ϳɺ���ü�ѹ����Һ�������ӻ�������з����C�������������������C��ԭ����______________
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������������ǵĽ���ϢϢ��أ�Ŀ�ҹ�ͨ�����6����Ⱦ�������Ũ���������������ָ����AQI����SO2��NO2����CO������3���е���Ⱦ�
��1������3������ֱ������������������������������ѧʽ����
��2�����������г�����NaClO2��Һ��Ϊ���ռ�����ͬʱ����������������������������ӦClO2��+2SO32��2SO42��+Cl�� �� �÷�Ӧ��ƽ�ⳣ��K�ı���ʽΪ��
��3�����÷�Ӧ6NO2+8NH3�T7N2+12H2O���ɵ�صķ���������ʵ����Ч��������������ŷţ����ỷ����Ⱦ�����ܳ�����û�ѧ�ܣ�װ����ͼ��ʾ��д���缫A�ĵ缫����ʽ �� ���������4.48L������ʱ��ͨ���缫B�ĵ�����Ϊ 
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ȷ��ʾ���з�Ӧ�����ӷ���ʽ��(����)
A. ��Cl2ͨ���Ȼ�������Һ:Fe2++Cl2![]() Fe3++2Cl-
Fe3++2Cl-
B. ����ͨ��ˮ��:Cl2+H2O![]() 2H++Cl-+ClO-
2H++Cl-+ClO-
C. FeCl3��Һ��ͨ������İ�ˮ: Fe3++3OH-![]() Fe(OH)3��
Fe(OH)3��
D. Cl2ͨ���ռ���Һ��:Cl2+2OH-![]() Cl-+ClO-+H2O
Cl-+ClO-+H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������Ԫ��W��X��Y��Z��ԭ��������������Ԫ��W��һ�ֵ������۵��Ӳ�ȴ�ı�ʯ��Y��ԭ�Ӱ뾶�����ж���������Ԫ�������X��Zͬ���壬��X��Y��Z����Ԫ���γɵ�һ��������ˮ����ϡ���ᣬ�д̼�������������ش��������⣺
��1��YԪ��λ�����ڱ��е�λ����_____________________��
��2��ZԪ����______����X��Z����Ԫ���γɵĻ�������______________��
��3������Ԫ���е�_______________Ԫ�����γɻ���������Ԫ����
��4��ijͬѧ��ͬ����Ԫ�����ʵݱ����ʵ��ʱ���Լ����һ��ʵ�鷽��������¼���й�ʵ���������±���

��д���пո��s
��ʵ��Ŀ�ģ�____________________________ ��
����ʵ�鷽�����Ӧ��ʵ�������ǣ�ʵ�鷽��2��Ӧ��ʵ��������___________�����ϱ��еķ���A.......F����ʵ�鷽��3��Ӧ��ʵ��������__________________________��
�۵ó����ɣ�ͬ����Ԫ�ش�����_________________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����н����У����������쳣����ʢ��Ũ�����������ǣ� ��
A.MgB.CuC.AgD.Fe
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com