
【题目】填写下列空白:
(1)一定质量的Al2(SO4)3中含有2.7 g Al3+,含有________个SO42-;溶于水得100 mL溶液,所得溶液的物质的量浓度为________ mol·L-1。
(2)同温同压下,同质量的CO2和SO2,它们的密度之比为________,氧原子数之比为________。
(3)要使NH3与CH4含相同数目的H原子,则NH3和CH4的物质的量之比为__________。
(4)标准状况下,密度为0.75 g·L-1的NH3与CH4组成的混合气体中,NH3的体积分数为__________,该混合气体对氢气的相对密度为________。
(5)已知ag A和bg B恰好完全反应生成0.2 mol C和dg D,则C的摩尔质量为____________。
【答案】9.03×1022(或0.15NA) 0.5 11∶16 16∶11 4∶3 80% 8.4 5(a+b-d) g·mol-1
【解析】
(1)找准物质的量关系:Al2(SO4)3~2Al3+~3SO42-计算可得;
(2)同温同压下,同质量的CO2和SO2,它们的密度与摩尔质量成正比,氧原子数与摩尔质量成反比;
(3)设NH3与CH4含氢原子物质的量均为12mol,则n(NH3)=4mol,n(CH4)=3mol;
(4)标准状况下,混合气体平均摩尔质量=![]() =16.8
=16.8![]() 。该混合气体对氢气的相对密度
。该混合气体对氢气的相对密度![]() =8.4;
=8.4;
(5)由质量守恒定律和![]() =
=![]() 可知。
可知。
(1)n(Al3+)=![]() =0.1 mol,n(SO42-)=
=0.1 mol,n(SO42-)=![]() n(Al3+)=0.15 mol,含有9.03×1022(或0.15NA)个SO42-。n[Al2(SO4)3]=0.05 mol,溶于水得100 mL溶液,所得溶液的物质的量浓度=
n(Al3+)=0.15 mol,含有9.03×1022(或0.15NA)个SO42-。n[Al2(SO4)3]=0.05 mol,溶于水得100 mL溶液,所得溶液的物质的量浓度=![]() = 0.5 mol·L-1;
= 0.5 mol·L-1;
(2)![]() =
=![]() =
=![]() ,同温同压下,气体的Vm相同,同质量的CO2和SO2,它们的密度与摩尔质量成正比,则
,同温同压下,气体的Vm相同,同质量的CO2和SO2,它们的密度与摩尔质量成正比,则![]() =
=![]() ==
==![]() =
=![]() 。
。![]() =
=![]() ,同质量的CO2和SO2,且1个CO2分子和1个SO2分子均含2个氧原子,则氧原子数与分子的物质的量成正比,氧原子数与摩尔质量成反比,则氧原子数之比为16∶11;
,同质量的CO2和SO2,且1个CO2分子和1个SO2分子均含2个氧原子,则氧原子数与分子的物质的量成正比,氧原子数与摩尔质量成反比,则氧原子数之比为16∶11;
(3)NH3与CH4含相同数目的H原子,设NH3与CH4/span>含氢原子物质的量均为12mol,则n(NH3)=4mol,n(CH4)=3mol,则NH3和CH4的物质的量之比为4∶3;
(4)标准状况下,密度为0.75 g·L-1的NH3与CH4组成的混合气体,混合气体平均摩尔质量=![]() =16.8
=16.8![]() ,设NH3体积分数为x,则CH4体积分数为1-x,所以有:17x + 16
,设NH3体积分数为x,则CH4体积分数为1-x,所以有:17x + 16![]() (1-x) = 16.8,解得x=80%。该混合气体对氢气的相对密度
(1-x) = 16.8,解得x=80%。该混合气体对氢气的相对密度![]() =8.4;
=8.4;
(5)已知ag A和bg B恰好完全反应生成0.2 mol C和dg D,由质量守恒定律知:m(C)=(a+b-d)g,则C的摩尔质量为![]() 。
。


科目:高中化学 来源: 题型:
【题目】已知 X(g)+3Y(g) ![]() 2Z(g) ΔH=-akJ·mol-1。一定条件下将1 molX 和3 molY通入2 L的恒容密闭容器中,反应10 min时,测得Y的物质的量为2.4 mol。下列说法正确的是
2Z(g) ΔH=-akJ·mol-1。一定条件下将1 molX 和3 molY通入2 L的恒容密闭容器中,反应10 min时,测得Y的物质的量为2.4 mol。下列说法正确的是
A. 在10 min内,X和Y反应放出的热量为0.3 a kJ
B. 在l0min时,X和Z的物质的量之比为1:2
C. 达到平衡状态时,X、Y的浓度不再改变
D. 升髙反应温度,逆反应速率增大,正反应速率减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为了研究化学反应A+BC+D的能量变化情况,某同学设计了如图所示装置。当向盛有A的试管中滴加试剂B时,看到U形管中甲处液面下降乙处液面上升。

试回答下列问题:
(1)该反应为_______反应(填“放热”或“吸热”)。
(2)A和B的总能量比C和D的总能量_______(填“高”或“低”)。
(3)物质中的化学能通过化学反应转化成_______释放出来。
(4)反应物化学键断裂吸收的能量_______(填“高”或“低”)于生成物化学键形成放出的能量。
(5)写出一个符合题中条件的化学方程式:____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某研究性学习小组设计了一组实验来探究第ⅦA族元素原子的得电子能力强弱规律。下图中A、B、C是三个可供选择制取氯气的装置,装置D的玻璃管中①②③④处依次放置蘸有NaBr溶液、淀粉碘化钾溶液、NaOH浓溶液和品红溶液的棉球。

(1)写出装置B中指定仪器的名称a________,b_________。
(2)实验室制取氯气还可采用如下原理:2KMnO4+16HCl(浓)===2KCl+2MnCl2+5Cl2↑+8H2O。依据该原理需要选择A、B、C装置中的________装置制取氯气。
(3)反应装置的导气管连接装置D的________(填“X”或“Y”)导管,试回答下列问题
①处所发生反应的离子方程式:____________________;
②处的现象:____________________;
③处所发生反应的离子方程式:__________________________。
(4)装置D中④的作用是__________________。
(5)某同学根据①②两处棉球颜色的变化得出结论:Cl、Br、I原子的得电子能力依次减弱。上述实验现象________(填“能”或“不能”)证明该结论、理由是___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用下图所示实验装置进行相应实验,能达到实验目的的是

A. 用①所示的操作可检查装置的气密性
B. 用②所示的装置制取少量的NO
C. 用③所示的装置干燥H2、NH3、CO2等
D. 用④所示装置制取Fe(OH)2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B是两种有刺激气味的气体。试根据下列实验事实填空。
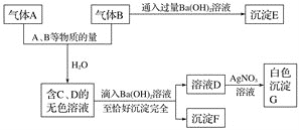
(1)写出A~F各物质的化学式:
A__________、B__________、C__________、D__________、E__________、F__________。
(2)写出A、B跟水反应的离子方程式:______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Be(OH)2是两性的,跟强酸反应时生成Be2+,跟强碱反应时生成BeO22—。现有三份等物质的量浓度、等体积的BeCl2、MgCl2、AlCl3溶液(配制时均加入少量盐酸),现将一定浓度的NaOH溶液分别滴入三种溶液中至过量,NaOH溶液的体积x(mL)与生成沉淀的物质的量y(mol)的关系如图所示,则与BeCl2、MgCl2、AlCl3三种溶液对应的图像正确的是( )

A. ⑤③① B. ②③④ C. ③⑤④ D. ③②①
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以铅蓄电池为电源,石墨为电极电解CuSO4溶液,装置如下图。若一段时间后Y电极上有6.4 g红色物质析出,停止电解。下列说法正确的是

A. a为铅蓄电池的负极
B. 电解过程中,铅蓄电池的负极增重30.3g
C. 电解结束时,左侧溶液质量增重8g
D. 铅蓄电池工作时正极电极反应式为:PbSO4+2e-=Pb+SO42-
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com