
【题目】已知 X(g)+3Y(g) ![]() 2Z(g) ΔH=-akJ·mol-1。一定条件下将1 molX 和3 molY通入2 L的恒容密闭容器中,反应10 min时,测得Y的物质的量为2.4 mol。下列说法正确的是
2Z(g) ΔH=-akJ·mol-1。一定条件下将1 molX 和3 molY通入2 L的恒容密闭容器中,反应10 min时,测得Y的物质的量为2.4 mol。下列说法正确的是
A. 在10 min内,X和Y反应放出的热量为0.3 a kJ
B. 在l0min时,X和Z的物质的量之比为1:2
C. 达到平衡状态时,X、Y的浓度不再改变
D. 升髙反应温度,逆反应速率增大,正反应速率减小
【答案】C
【解析】
反应10min时,测得Y的物质的量为2.4mol,则参加反应的Y为3mol-2.4mol=0.6mol,物质的量与热量成正比;参加反应的Y为0.6mol,由X(g)+3Y(g)![]() 2Z(g)可知,生成Z为0.4mol,消耗X为0.2mol;平衡时各物质的浓度不变;升高温度,正逆反应速率均增大。
2Z(g)可知,生成Z为0.4mol,消耗X为0.2mol;平衡时各物质的浓度不变;升高温度,正逆反应速率均增大。
反应10min时,测得Y的物质的量为2.4mol,则参加反应的Y为3mol-2.4mol=0.6mol,物质的量与热量成正比,则放出的热量为0.63×akJ=0.2akJ,A错误;参加反应的Y为0.6mol,由X(g)+3Y(g)![]() 2Z(g)可知,生成Z为0.4mol,消耗X为0.2mol,则l0min时,X和Z的物质的量之比为(1mol-0.2mol):0.4mol=2:1,B错误;平衡时各物质的浓度不变,则达到平衡状态时,X、Y的浓度不再改变,C正确;升高温度,正逆反应速率均增大,该反应为放热反应,逆反应速率增大的倍数大于正反应速率增大的倍数,平衡逆向移动,D错误。
2Z(g)可知,生成Z为0.4mol,消耗X为0.2mol,则l0min时,X和Z的物质的量之比为(1mol-0.2mol):0.4mol=2:1,B错误;平衡时各物质的浓度不变,则达到平衡状态时,X、Y的浓度不再改变,C正确;升高温度,正逆反应速率均增大,该反应为放热反应,逆反应速率增大的倍数大于正反应速率增大的倍数,平衡逆向移动,D错误。
故选C。


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】处于平衡状态的反应2 H2 S(g) ![]() 2H2(g)+S2(g)
2H2(g)+S2(g) ![]() H>0,不改变其他条件的情况下合理的说法是
H>0,不改变其他条件的情况下合理的说法是
A.加入催化剂,反应途径将发生改变,![]() H也将随之改变
H也将随之改变
B.升高温度,正逆反应速率都增大,H2S分解率也增大
C.增大压强,平衡向逆反应方向移动,将引起体系温度降低
D.若体系恒容,注人一些H2后达新平衡,H2浓度将减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】①NaCl、②干冰、③冰、④Na2O2、⑤白磷(P4)、⑥金刚石、⑦Na2CO3、⑧钠。以上物质中属于离子晶体的是____________;属于分子晶体的是____________(填序号)。氯化钡是无色晶体,溶于水,水溶液能导电,熔点1 560 ℃。它可能属于____________晶体。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向密闭容器中充入物质的量浓度均为 0.1 mol/L的CH4和 CO2,在一定条件下发生反应CH4(g)+CO2(g)![]() 2CO(g)+2H2(g),测得CH4的平衡转化率与温度及压强的关系如图所示。下列说法不正确的是
2CO(g)+2H2(g),测得CH4的平衡转化率与温度及压强的关系如图所示。下列说法不正确的是
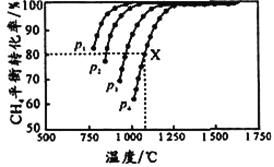
A. 平衡时CO与H2的物质的量比为1:1
B. p1、p2、p3、p4由大到小的顺序为p1<p2<p3<p4
C. 1100℃,p4条件下,该反应10 min时达到平衡点X,则ν(CO2) = 0.008 molL-1min-1
D. 随着温度升高,该反应的平衡常数减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(12分)现有一定量含有Na2O杂质的Na2O2试样,用下图的实验装置测定Na2O2试样的纯度。(可供选用的反应物只有CaCO3固体、6 mol/L盐酸、6 mol/L硫酸和蒸馏水)
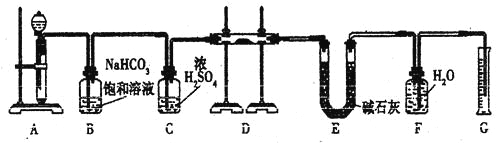
回答下列问题:
(1)装置A中液体试剂选用 ,理由是 。
(2)装置B的作用是 。
装置C的作用是 。
装置E中碱石灰的作用是 。
(3)装置D中发生反应的化学方程式是 。
(4)若开始时测得样品的质量为2.0 g,反应结束后测得气体体积为224 mL(标准状况),则Na2O2试样的纯度为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I、乙酸乙酯是重要的有机合成中间体,广泛应用于化学工业。实验室利用如图的装置制备乙酸乙酯。
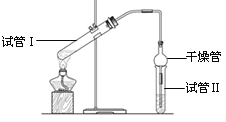
(1)与教材采用的实验装置不同,此装置中采用了球形干燥管,其作用是:_____________。
(2)请写出用CH3CH218OH制备乙酸乙酯的化学方程式:_____________,反应类型为_______。
(3)为了证明浓硫酸在该反应中起到了催化剂和吸水剂的作用,某同学利用上图所示装置进行了以下4个实验。实验开始先用酒精灯微热3min,再加热使之微微沸腾3min。实验结束后充分振荡小试管Ⅱ再测有机层的厚度,实验记录如下:
实验 编号 | 试管Ⅰ中的试剂 | 试管Ⅱ中的试剂 | 有机层的厚度/cm |
A | 2 mL乙醇、1 mL乙酸、 1mL18mol·L-1 浓硫酸 | 饱和Na2CO3溶液 | 3.0 |
B | 2 mL乙醇、1 mL乙酸 | 0.1 | |
C | 2 mL乙醇、1 mL乙酸、 3 mL 2mol·L-1 H2SO4 | 0.6 | |
D | 2 mL乙醇、1 mL乙酸、盐酸 | 0.6 |
①实验D的目的是与实验C相对照,证明H+对酯化反应具有催化作用。实验D中应加入盐酸的体积和浓度分别是______mL和_____mol·L-1 。
②分析实验_________________(填实验编号)的数据,可以推测出浓H2SO4的吸水性提高了乙酸乙酯的产率。
(4)若现有乙酸90g,乙醇138g发生酯化反应得到80g乙酸乙酯,试计算该反应的产率为______________(用百分数表示,保留一位小数)。
II、已知乳酸的结构简式为![]() 。试回答:
。试回答:
①乳酸分子中的官能团有:_____________________________________(写名称);
②乳酸与足量金属钠反应的化学方程式为________________________________;
③已知—COOH不会发生催化氧化,写出加热时,乳酸在Cu作用下与O2反应的化学方程式:________________________________________________;
④腈纶织物产泛地用作衣物、床上用品等。腈纶是由CH2=CH-CN聚合而成的。 写出在催化剂、加热条件下制备腈纶的化学方程式________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时在10 mL 0.1mol·L—1Na2CO3溶液中逐滴加入0.1 mol·L—1HCl溶液20 mL,溶液中部分含碳微粒的物质的量随溶液pH的变化如图所示。下列说法正确的是( )

A. 0.1 mol·L—1Na2CO3溶液中c(Na+)+c(H+)=c(OH—)+c(CO32—)+c(HCO3—)
B. 当加入10mL盐酸时,所得混合溶液pH>7
C. 当pH=8时,c(Na+)=c(CO32—)+c(HCO3—)+c(H2CO3)
D. 在M点:c(CO32—)=c(HCO3—)>c(Na+)>c(OH—)>c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向300 mL 1 mol·L-1的稀硝酸中,加入5.6 g铁粉,充分反应后,铁粉全部溶解(假设还原产物只有NO),下列说法不正确的是( )
A. 最终所得溶液中既有Fe2+又有Fe3+
B. 最终溶液中,硝酸无剩余
C. 标准状况下生成NO的体积为1.68 L
D. 再向最终所得溶液中滴加稀硝酸,无明显变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】填写下列空白:
(1)一定质量的Al2(SO4)3中含有2.7 g Al3+,含有________个SO42-;溶于水得100 mL溶液,所得溶液的物质的量浓度为________ mol·L-1。
(2)同温同压下,同质量的CO2和SO2,它们的密度之比为________,氧原子数之比为________。
(3)要使NH3与CH4含相同数目的H原子,则NH3和CH4的物质的量之比为__________。
(4)标准状况下,密度为0.75 g·L-1的NH3与CH4组成的混合气体中,NH3的体积分数为__________,该混合气体对氢气的相对密度为________。
(5)已知ag A和bg B恰好完全反应生成0.2 mol C和dg D,则C的摩尔质量为____________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com