
【题目】Mg、Ni、Cu、Zn 等元素在生产、生活中有着广泛的应用。回答下列问题:
(1)Mg、Ni、Cu 等金属可能形成金属互化物。金属互化物的结构类型丰富多样,确定某种金属互化物是晶体还是非晶体可通过___________测定。
(2)根据 Cu、Zn 的原子结构比较第一电离能:I1(Cu)_________ I1(Zn)(填“大于”、 “等于”或“小于”),理由是_____________________。
(3)[Ni(NH3)6](NO3)2 中不存在的化学键为___________(填序号)。
a.离子键 b.金属键 c.配位键 d.氢键
(4)镍基合金储氢的研究已取得很大进展。
①图甲是一种镍基合金储氢后的晶胞结构示意图。
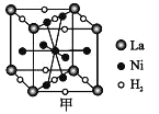
该合金储氢后,H2 与 Ni 的物质的量之比为___________。
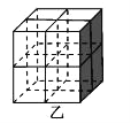
②Mg2NiH4 是一种储氢的金属氢化物。在 Mg2NiH4 晶胞中,Ni 原子占据如图乙的顶点和面心,Mg2+处于乙图八个小立方体的体心。Mg2+位于 Ni 原子形成的___________ (填“八面体空隙”或“四面体空隙”)。 晶体的密度为ρg·cm-3,NA表示阿伏加德罗常数,Mg2+和 Ni 原子的最短距离为__________cm(用含ρ和 NA 的代数式表示)。
【答案】X—射线衍射实验 小于 Zn原子轨道中电子处于全满状态,较难失电子,Cu失去一个电子内层电子达到全充满稳定状态 b 3:5 四面体空隙 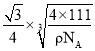
【解析】
(1)确定某种金属互化物是晶体还是非晶体可通过X—射线衍射实验测定;
(2)轨道中电子处于全满、全空、半满时较稳定,失去电子需要的能量较大,Zn原子轨道中电子处于全满状态,Cu失去一个电子内层电子达到全充满稳定状态,所以Cu较Zn易失电子;
(3)[Ni(NH3)6](NO3)2中NH3与Ni2+之间为配位键;[Ni(NH3)6]2+与NO3-之间为离子键;
(4)①根据晶胞结构示意图计算晶胞中H2 与 Ni个数比;
②Ni 原子占据如图乙的顶点和面心,Mg2+处于乙图八个小立方体的体心,则Mg2+位于 Ni 原子形成四面体空隙;Mg2+和 Ni 原子的最短距离为晶胞体对角线的![]() ,再根据晶胞密度计算。
,再根据晶胞密度计算。
(1)确定某种金属互化物是晶体还是非晶体可通过X—射线衍射实验测定,故答案为:X—射线衍射实验;
(2)轨道中电子处于全满、全空、半满时较稳定,失去电子需要的能量较大,基态Cu的核外电子排布式为[Ar]3d104s1,基态Zn的核外电子排布式为[Ar]3d104s2,Zn原子轨道中电子处于全满状态,较难失电子,而Cu失去1个电子成为Cu+:[Ar]3d10,,Cu+达到全满结构,较稳定,Cu失去1个电子更容易,则第一电离能Cu<Zn,故答案为:小于;Zn原子轨道中电子处于全满状态,较难失电子,Cu失去一个电子内层电子达到全充满稳定状态;
(3)[Ni(NH3)6](NO3)2中NH3与Ni2+之间为配位键;[Ni(NH3)6]2+与NO3-之间为离子键,不存在金属键,故答案为:b;
(4)①根据晶胞结构示意图计算晶胞中H2数目为![]() ,Ni数目为
,Ni数目为![]() ,则H2 与 Ni 的物质的量之比为3:5,故答案为:3:5;
,则H2 与 Ni 的物质的量之比为3:5,故答案为:3:5;
②Ni 原子占据如图乙的顶点和面心,Mg2+处于乙图八个小立方体的体心,则Mg2+位于 Ni 原子形成四面体空隙;该晶胞中Ni原子个数![]() ,Mg2+个数为8,由化学式可知H原子个数为16,则晶胞质量为
,Mg2+个数为8,由化学式可知H原子个数为16,则晶胞质量为![]() ,晶体的密度为ρg·cm-3,则晶胞的边长为:
,晶体的密度为ρg·cm-3,则晶胞的边长为: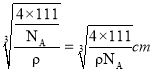 ,Mg2+和 Ni 原子的最短距离为晶胞体对角线的
,Mg2+和 Ni 原子的最短距离为晶胞体对角线的![]() ,则Mg2+和 Ni 原子的最短距离为
,则Mg2+和 Ni 原子的最短距离为 ,故答案为:四面体空隙;
,故答案为:四面体空隙;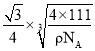 。
。


 口算题卡加应用题集训系列答案
口算题卡加应用题集训系列答案科目:高中化学 来源: 题型:
【题目】某课题组以纳米Fe2O3 作为电极材料制备锂离子电池(另一极为金属锂和石墨的复合材料),通过在室温条件下对锂离子电池进行循环充放电,成功地实现了对磁性的可逆调控(如图)。以下说法正确的是( )
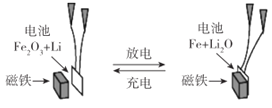
A.放电时,正极的电极反应式为Fe2O3+6Li++6e-=2Fe+3Li2O
B.该电池可以用水溶液做电解质溶液
C.放电时,Fe作电池的负极,Fe2O3作电池的正极
D.充电时,电池被磁铁吸引
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表是元素周期表的一部分,回答下列问题:
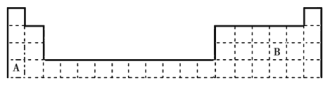
(1)B在周期表中的位置是__;写出A、B的单质之间发生反应的化学方程式:__。
(2)写出表中位于长周期的卤族元素的名称:__;属于短周期的碱金属元素的元素符号为__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于如图所示①、②两个装置的叙述,正确的是( )
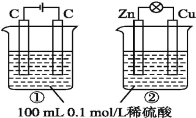
A.装置名称:①是原电池,②是电解池
B.硫酸浓度变化:①增大,②减小
C.电极反应式:①中阳极:4OH--4e-=2H2O+O2↑、②中负极:Zn-2e-=Zn2+
D.离子移动方向:①中H+向阴极方向移动,②中H+向负极方向移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上以金属镍废料(除NiO外,还含有少量的FeO、Fe2O3) 为原料生产Ni2O3的流程如下:
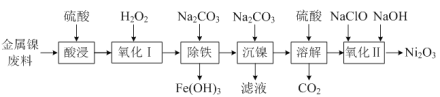
(1) “酸浸”时,Fe2O3发生反应的化学方程式为_____。
(2) “氧化Ⅰ”时,加入双氧水的目的是_____。
(3) “沉镍”时,检验Ni2+沉淀完全的操作是_____。
(4) “氧化Ⅱ”时,发生反应的离子方程式为_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度时,在2L容器中,某一反应中A、B的物质的量随时间变化的曲线如图所示,由图中数据分析得:

(1)在4min末时,A.B的物质的量浓度c(A)___c(B);在该温度下达到化学平衡时c(A)___c(B)(以上填“>”“<”或“=”);
(2)从反应开始至4min时,A的平均反应速率为___;
(3)该反应的化学方程式为___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在标准状况下,①![]() 氮气②
氮气②![]() 二氧化碳③
二氧化碳③![]() ,含分子数最多的是__________(填序号,下同);质量最大的是__________;体积最小的是_________。
,含分子数最多的是__________(填序号,下同);质量最大的是__________;体积最小的是_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定条件下,下列物质不能与二氧化硅反应的是( )
①焦炭 ②纯碱 ③碳酸钙 ④氢氟酸 ⑤高氯酸 ⑥氢氧化钾 ⑦氧化钙⑧ 氮气
A.③⑤⑦⑧B.⑤⑦⑧C.⑤⑧D.⑤⑦
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度时,在 2L 容器中发生 A 、B 两种物之间的转化反应 ,A、B 物质的量随时间变化的曲线如图所示,下列说法正确的是
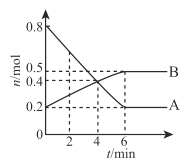
A.该反应的化学方程式是A![]() 2B
2B
B.2 min 时,正反应速率大于逆反应速率
C.4 min 时,A 、B 的物质的量相等且反应达到了平衡状态
D.反应开始至 6min,A 的平均反应速率为0. lmol/(Lmin)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com