
【题目】下列实验装置应用于铜与浓硫酸反应制取二氧化硫和硫酸铜晶体,能达到实验目的的是
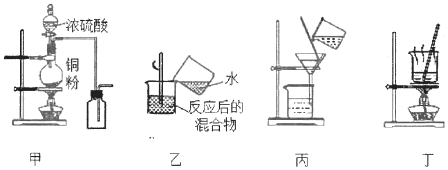
A. 用图甲装置制取并收集二氧化硫
B. 用图乙装置向反应后的混合物中加水稀释
C. 用图丙装置过滤出稀释后混合物中的不溶物
D. 用图丁装置将硫酸铜溶液蒸发结晶
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】二硫代碳酸钠(Na2CS3)在农业上用作杀菌剂和杀线虫剂,在工业上用于处理废水中的重金属离子。某化学兴趣小组对Na2CS3的一些性质进行探究。回答下列问题:
(1)在试管中加入少量三硫代碳酸钠样品,加水溶解,所得溶液pH=10,由此可知H2CS3是____酸(填“强”或“弱”)。向该溶液中滴加酸性KMnO4溶液,紫色褪去,由此说明Na2CS3具有____性。
(2)为了测定某Na2CS3溶液的浓度,按图装置进行实验。将35.0 mLNa2CS3溶液置于下列装置A的三颈瓶中,打开仪器d的活塞,滴入足量2.0 mol/L稀H2SO4,关闭活塞。

已知:![]() CS2和H2S均有毒:CS2不溶于水,沸点46℃,与C02某些性质相似,与NaOH作用生成Na2COS2和H2O。
CS2和H2S均有毒:CS2不溶于水,沸点46℃,与C02某些性质相似,与NaOH作用生成Na2COS2和H2O。
①仪器d的名称是____。反应开始时需要先通入一段时间N2,其作用为____。
②B中发生反应的离子方程式是____。
③反应结束后打开活塞k,再缓慢通入热N2 一段时间,其目的是____。
④为了计算三硫代碳酸铀溶液的浓度,可测定B中生成沉淀的质量。称量B中沉淀质量之前需要进行的实验操作名称是____,若B中生成沉淀的质量为8.4g则35.0 mL三硫代碳酸钠溶液的物质的量浓度是____。
⑤若反应结束后将通热N2改为通热空气,通过测定C中溶液质量的增加值来计算三硫代碳酸钠溶液的浓度时,计算值____<填“偏高”“偏低”或“无影响”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】食用酒精常用淀粉发酵制备,下列说法正确的是( )
A.淀粉属于化合物
B.淀粉溶液和酒精均能产生丁达尔效应
C.淀粉溶液和酒精可用碘水鉴别
D.淀粉转化为乙醇不属于氧化还原反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】人们应用原电池原理制作了多种电池,以满足不同的需要。以下每小题中的电池广泛使用于日常生活、生产和科学技术等方面,请根据题中提供的信息填空。
(1)蓄电池在放电时起原电池作用,在充电时起电解池的作用。铅蓄电池在放电时发生的电池反应式为:Pb+PbO2+2H2SO4=2PbSO4+2H2O。负极反应式为________________反应一段时间后负极的质量_________(填“增重”或“减少”或“不变”)
(2)燃料电池是一种高效、环境友好的供电装置,如图是甲烷燃料电池原理示意图,该电池极的负电极反应式是:_____________________;正极电极反应式_______________

(3)将铝片和铜片用导线相连,分别插入浓硝酸中(a组)和插入烧碱溶液中(b组),都形成了原电池,在a组原电池中,负极材料为___________;写出b组插入烧碱溶液中形成原电池的负极反应式:_________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列卤代烃在KOH醇溶液中加热不反应的是
①![]() ②
②![]() ③(CH3)3C—CHBr2 ④CHCl2—CHBr2 ⑤
③(CH3)3C—CHBr2 ④CHCl2—CHBr2 ⑤![]() ⑥CH3Cl
⑥CH3Cl
A. ①③⑥ B. ②③⑤ C. 全部 D. ②④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度和压强下,在2L的密闭容器中合成氨气:![]() 。反应过程中反应物和生成物的物质的量随时间的变化如图所示。下列说法错误的是
。反应过程中反应物和生成物的物质的量随时间的变化如图所示。下列说法错误的是

A.0~10min内,以NH3表示的平均反应速率为![]()
B.10~20min内,![]()
C.该反应在20min时达到化学平衡状态
D.N2的平衡转化率与H2平衡转化率相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】FePO4是一种难溶于水的白色固体,可作金属防腐剂,也可用于制备电动汽车电池的正极材料 LiFePO4。实验室利用FeSO4·7H2O和H3PO4(弱酸)制备FePO4、 LiFePO4流程如下图:
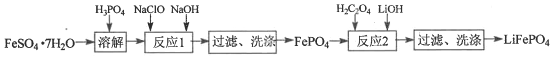
回答下列问题:
(1)“溶解”时H3PO4不宜过量太多的原因是_________________________________。
(2)①洗涤FePO4沉淀的操作是__________________________________________________。
②若经多次洗涤后所得“FePO4”仍呈棕色,则“FePO4”最可能混有的杂质是___________。
(3)“反应1”时总反应的离子方程式是:_________________________________。
(4)“反应2”时总反应的化学方程式是:2LiOH+6H2C2O4+2FePO4=2LiFePO4+ 7CO2+ 5X+7H2O,其中X的化学式为___________;每生成1 mol LiFePO4,该反应转移___________mole-。
(5)LiFePO4电池稳定性高、安全、对环境友好,该电池的总反应式是:LiFePO4+C6![]() Li1- xFePO4+LixC6,其放电时工作原理如图所示。则:
Li1- xFePO4+LixC6,其放电时工作原理如图所示。则:
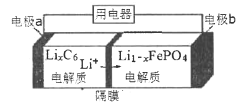
充电时,a极的电极名称为___________;放电时,b极的电极反应式为:_________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,pH=1的乙酸溶液和pH=13的NaOH溶液,下列叙述中正确的是
A. 两种溶液等体积混合后,溶液呈碱性
B. 乙酸溶液中c(CH3COOH)大于NaOH溶液中c(Na+)
C. 分别稀释10倍,两溶液的pH之和大于14
D. 若两溶液混合后pH=7,则有c(Na+)=c(CH3COO-)+c(CH3COOH)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com