
ҰңМвДүҰүВнАөЛбВИ±ҢДЗГфУЦГыЖЛ¶ыГфӘЁ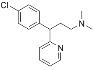 Ә©КЗТ»ЦЦіӘәыµДү№№эГфТ©ОпӘ¬ЖдғПіЙВ·ПЯИзПВӘғ
Ә©КЗТ»ЦЦіӘәыµДү№№эГфТ©ОпӘ¬ЖдғПіЙВ·ПЯИзПВӘғ
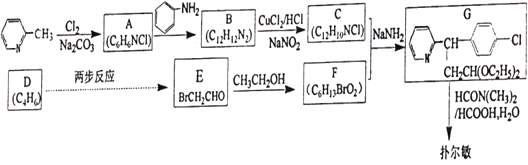
ТСЦҒӘғМәМәЛ«әьүЙТФ±»іфСхСх»Ү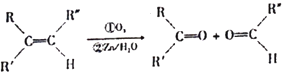
Зл»ШөрПВБРОКМвӘғ
ӘЁ1Ә©ПВБРЛµ·ЁЦРІ»ХэИ·µДКЗ________ҰӘ
AӘ®ЖЛ¶ыГфµД·ЦЧУКҢОҒC16H18N2Cl
BӘ®G·ЦЧУЦРғ¬УРБҢёцКЦРФМәФЧУ
CӘ®»ҮғПОпCЦРЛщУРФЧУүЙДЬ№ІЖҢГж
DӘ®»ҮғПОпEДЬ·ұЙъИҰөъҰұәУіЙҰұСх»ҮҰұ»№Ф·өУ¦
ӘЁ2Ә©»ҮғПОпBµДҢб№№әтКҢКЗ________ҰӘ
ӘЁ3Ә©E![]() FµД»ҮС§·ҢіМКҢКЗ________ҰӘ
FµД»ҮС§·ҢіМКҢКЗ________ҰӘ
ӘЁ4Ә©РөіцН¬К±·ығППВБРМхәюµД»ҮғПОпB(C12H12N2)БҢёцН¬·ЦТм№№МеµДҢб№№әтКҢ________ҰӘ
ұЩ·ЦЧУЦРғ¬УРБҢёцБщФҒ»·Ә»ұЪ1H-NMRЖЧПФКңУР3ёц·еҰӘ
ӘЁ5Ә©ЙиәЖУЙDңБҢІҢ·өУ¦µГµҢEµДғПіЙВ·ПЯӘЁУГБчіМНә±нКңӘ¬ОЮ»ъКФәБИОСҰӘ©________ҰӘ
Ұңөр°ёҰүҰңөрМвүХ1ҰүABC ![]() BrCH2CHO + 2C2H5OH
BrCH2CHO + 2C2H5OH![]() BrCH2CH(OC2H5)2 +H2O
BrCH2CH(OC2H5)2 +H2O 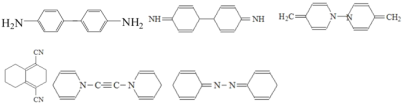
![]()
ҰңҢвОцҰү
![]() УлCl2·ұЙъИҰөъ·өУ¦µГµҢAӘЁ
УлCl2·ұЙъИҰөъ·өУ¦µГµҢAӘЁ![]() Ә©Ә¬AУл±Ң°·ИҰөъғуµГµҢBӘЁ
Ә©Ә¬AУл±Ң°·ИҰөъғуµГµҢBӘЁ![]() Ә©Ә¬BЦР°±»щәМРшЯВВИФЧУИҰөъµГµҢCӘЁ
Ә©Ә¬BЦР°±»щәМРшЯВВИФЧУИҰөъµГµҢCӘЁ![]() Ә©Ә»әМРшІЙУГДж·ЦОц·ЁӘ¬УЙDµД·ЦЧУКҢC4H6үЙЦҒӘ¬Жд·ЦЧУДЪµДІ»±ӨғН¶И =
Ә©Ә»әМРшІЙУГДж·ЦОц·ЁӘ¬УЙDµД·ЦЧУКҢC4H6үЙЦҒӘ¬Жд·ЦЧУДЪµДІ»±ӨғН¶И = ![]() = 2Ә¬ЗТң№эБҢІҢ·өУ¦үЙТФµГµҢ»ҮғПОпEӘЁBrCH2CHOӘ©Ә¬үЙНЖЦҒDОҒ1,4-¶Ұ¶юП©Ә¬ФЩҢбғПМәМәЛ«әьүЙТФ±»іфСхСх»ҮіЙМәСхЛ«әьµДТСЦҒРЕПұәөүЙНЖіцХвБҢІҢ·өУ¦Ә¬»ҮғПОпEУлБҢ·ЦЧУТТөә·ұЙъ·өУ¦ЙъіЙFӘЁBrCH2CH(OC2H5)2Ә©Ә¬ңЭөЛ·ЦОцЧчөрҰӘ
= 2Ә¬ЗТң№эБҢІҢ·өУ¦үЙТФµГµҢ»ҮғПОпEӘЁBrCH2CHOӘ©Ә¬үЙНЖЦҒDОҒ1,4-¶Ұ¶юП©Ә¬ФЩҢбғПМәМәЛ«әьүЙТФ±»іфСхСх»ҮіЙМәСхЛ«әьµДТСЦҒРЕПұәөүЙНЖіцХвБҢІҢ·өУ¦Ә¬»ҮғПОпEУлБҢ·ЦЧУТТөә·ұЙъ·өУ¦ЙъіЙFӘЁBrCH2CH(OC2H5)2Ә©Ә¬ңЭөЛ·ЦОцЧчөрҰӘ
ӘЁ1Ә©A. ёщңЭЖЛ¶ыГфµДҢб№№әтКҢӘЁ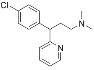 Ә©үЙЦҒЖд·ЦЧУКҢОҒC16H19N2ClӘ¬№КAПоөнОуӘ»
Ә©үЙЦҒЖд·ЦЧУКҢОҒC16H19N2ClӘ¬№КAПоөнОуӘ»
B. G·ЦЧУµДҢб№№әтКҢЦРӘ¬Ц»УРТ»ёцCФЧУОҒКЦРФМәФЧУӘ¬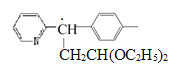 ӘЁәУµгµДCФЧУӘ©Ә¬№КBПоөнОуӘ»
ӘЁәУµгµДCФЧУӘ©Ә¬№КBПоөнОуӘ»
C. »ҮғПОпCµДҢб№№әтКҢОҒӘғ![]() Ә¬·ЦЧУДЪғ¬УРСЗәЧ»щӘЁ-CH2Ә©Ә¬ФтІ»үЙДЬ№ІЖҢГжӘ¬№КCПоөнОуӘ»
Ә¬·ЦЧУДЪғ¬УРСЗәЧ»щӘЁ-CH2Ә©Ә¬ФтІ»үЙДЬ№ІЖҢГжӘ¬№КCПоөнОуӘ»
D. »ҮғПОпEµДҢб№№әтКҢОҒӘғBrCH2CHOӘ¬деФЧУүЙ·ұЙъИҰөъ·өУ¦Ә¬И©»щүЙ·ұЙъәУіЙҰұСх»ҮғН»№Ф·өУ¦Ә¬№КDПоХэИ·Ә»
өр°ёСҰABCӘ»
ӘЁ2Ә©ёщңЭЙПКц·ЦОцӘ¬үЙЦҒ»ҮғПОпBµДҢб№№әтКҢОҒ![]() Ә¬
Ә¬
№Көр°ёОҒӘғ![]() Ә»
Ә»
ӘЁ3Ә©E![]() FµД»ҮС§·ҢіМКҢОҒBrCH2CHO + 2C2H5OH
FµД»ҮС§·ҢіМКҢОҒBrCH2CHO + 2C2H5OH![]() BrCH2CH(OC2H5)2 +H2OӘ¬
BrCH2CH(OC2H5)2 +H2OӘ¬
№Көр°ёОҒӘғBrCH2CHO + 2C2H5OH![]() BrCH2CH(OC2H5)2 +H2OӘ»
BrCH2CH(OC2H5)2 +H2OӘ»
ӘЁ4Ә©1H-NMRЖЧПФКңУР3ёц·еӘ¬ЛµГч·ЦЧУДЪУР3ЦЦЗвФЧУӘ¬БщФҒ»·ЗТ·ЦЧУКҢОҒC12H12N2µДН¬·ЦТм№№МеУРӘғ Ә¬
Ә¬
№Көр°ёОҒӘғ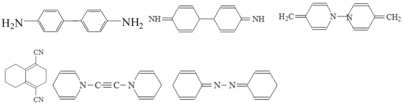 Ә»
Ә»
ӘЁ5Ә©DЦРғ¬УР1Ә¬4ғЕCФЧУУРМәМәЛ«әьӘ¬ҢбғПТСЦҒМбКңМхәюӘ¬үЙПИ°ө1:1УлдеЛ®әУіЙЙъіЙ![]() Ә¬ФЩ±»іфСхСх»ҮӘ¬·өУ¦µГµҢEӘ¬ЖдғПіЙВ·ПЯИзПВӘғ
Ә¬ФЩ±»іфСхСх»ҮӘ¬·өУ¦µГµҢEӘ¬ЖдғПіЙВ·ПЯИзПВӘғ
![]() Ә¬
Ә¬
№Көр°ёОҒӘғ![]() ҰӘ
ҰӘ


 ¶б№ЪҢрңнИ«ДЬБ·үәПµБРөр°ё
¶б№ЪҢрңнИ«ДЬБ·үәПµБРөр°ё
| Дкә¶ | ёЯЦРүОіМ | Дкә¶ | іхЦРүОіМ |
| ёЯТ» | ёЯТ»Гв·СүОіМНЖәцӘҰ | іхТ» | іхТ»Гв·СүОіМНЖәцӘҰ |
| ёЯ¶ю | ёЯ¶юГв·СүОіМНЖәцӘҰ | іх¶ю | іх¶юГв·СүОіМНЖәцӘҰ |
| ёЯИэ | ёЯИэГв·СүОіМНЖәцӘҰ | іхИэ | іхИэГв·СүОіМНЖәцӘҰ |
үЖДүӘғёЯЦР»ҮС§ АөФөӘғ МвРНӘғ
ҰңМвДүҰүУГ»ҮС§УГУп±нКңӘғ
(1)2ёцНАлЧУ__________Ә»
(2)Сх»ҮМъЦРМъФҒЛШµД»ҮғПәЫОҒ+3әЫ_______Ә»
(3)ИЬУЪЛ®ОВ¶ИҢµµНµДТ»ЦЦСО_________Ә»
Ійүөөр°ёғНҢвОц>>
үЖДүӘғёЯЦР»ҮС§ АөФөӘғ МвРНӘғ
ҰңМвДүҰүNA±нКң°ұ·ьәУµВВЮіӘКэµДКэЦµҰӘПВБРµДЛµ·ЁЦРӘ¬ХэИ·µДКЗӘЁ Ә©
A. 4.6gҢрКфДЖУЙФЧУНкИ«±дОҒNa+ АлЧУК±Ә¬К§ИӨµДµзЧУКэОҒ0.1NA
B. NA ёцСхЖш·ЦЧУУлNA ёцЗвЖш·ЦЧУµДЦКБү±ИОҒ8©U1
C. 0.2 NAёцБтЛб·ЦЧУУл19.6gБЧЛбӘЁПа¶Ф·ЦЧУЦКБүӘғ98Ә©ғ¬УРПаН¬µДСхФЧУКэ
D. 22.4LµДµҒЖшЛщғ¬УРµДФЧУКэОҒ2NA
Ійүөөр°ёғНҢвОц>>
үЖДүӘғёЯЦР»ҮС§ АөФөӘғ МвРНӘғ
ҰңМвДүҰү4ҰжК±ФЪ100mLЛ®ЦРИЬҢвБЛ22.4LВИ»ҮЗвЖшМеӘЁФЪ±кЧәЧөүцПВІвµГӘ©ҰӘПВБР№ШУЪЛщРОіЙµДИЬТғЛµ·ЁЦРӘ¬ХэИ·µДКЗӘЁ Ә©
A. ёГИЬТғИЬЦКµДОпЦКµДБүЕЁ¶ИОҒ10molҰ¤L-1
B. ИфТСЦҒёГИЬТғµДГЬ¶ИӘ¬ФтүЙЗуµГИЬТғИЬЦКµДОпЦКµДБүЕЁ¶И
C. ёГИЬТғЦРғ¬УР0.1molµДCl-
D. ёГИЬТғµДМе»эОҒ22.5L
Ійүөөр°ёғНҢвОц>>
үЖДүӘғёЯЦР»ҮС§ АөФөӘғ МвРНӘғ
ҰңМвДүҰүПВБРАлЧУ·ҢіМКҢЦРІ»ХэИ·µДКЗ(ҰҰҰҰ)
A. СОЛбµОФЪКҮ»ТКҮЙПӘғCaCO3+2H+![]() Ca2++H2O+CO2Ұь
Ca2++H2O+CO2Ұь
B. ПтBa(OH)2ИЬТғЦРµОИлЙЩБүµДNaHSO4ИЬТғӘғH++SO42Ә+Ba2++OH-![]() BaSO4Ұэ+H2O
BaSO4Ұэ+H2O
C. ПтBa(OH)2ИЬТғЦРµОИл№эБүµДNaHSO4ИЬТғӘғ2H++SO42Ә+Ba2++2OH-![]() BaSO4Ұэ+2H2O
BaSO4Ұэ+2H2O
D. ПҰБтЛбµОФЪНЖ¬ЙПӘғCu+2H+![]() Cu2++H2Ұь
Cu2++H2Ұь
Ійүөөр°ёғНҢвОц>>
үЖДүӘғёЯЦР»ҮС§ АөФөӘғ МвРНӘғ
ҰңМвДүҰүТСЦҒ299 KК±Ә¬ғПіЙ°±·өУ¦N2(g ) + 3H2 ( g )![]() 2NH3( g ) ҰчH =" -92.0" kJ/molӘ¬Ң«өЛОВ¶ИПВµД1 mol N2ғН3 mol H2·ЕФЪТ»ГЬ±ХИЭЖчЦРӘ¬ФЪөЯ»ҮәБөжФЪК±ҢшРР·өУ¦Ә¬ІвµГ·өУ¦·ЕіцµДИИБүОҒ(ғцВФДЬБүЛрК§)
2NH3( g ) ҰчH =" -92.0" kJ/molӘ¬Ң«өЛОВ¶ИПВµД1 mol N2ғН3 mol H2·ЕФЪТ»ГЬ±ХИЭЖчЦРӘ¬ФЪөЯ»ҮәБөжФЪК±ҢшРР·өУ¦Ә¬ІвµГ·өУ¦·ЕіцµДИИБүОҒ(ғцВФДЬБүЛрК§)
A. Т»¶ЁөуУЪ92.0 kJ B. Т»¶ЁµИУЪ92.0 kJ
C. Т»¶ЁРҰУЪ92.0 kJ D. І»ДЬИ·¶Ё
Ійүөөр°ёғНҢвОц>>
үЖДүӘғёЯЦР»ҮС§ АөФөӘғ МвРНӘғ
ҰңМвДүҰүПВБРЖшМеЦРәИүЙУГЕЁБтЛбёЙФпӘ¬УЦүЙУГ№ММеЗвСх»ҮДЖёЙФпµДКЗ
A. NH3 B. H2 C. Cl2 D. SO2
Ійүөөр°ёғНҢвОц>>
үЖДүӘғёЯЦР»ҮС§ АөФөӘғ МвРНӘғ
ҰңМвДүҰүЙиNA±нКң°ұ·ьәУµВВЮіӘКэµДЦµӘ¬ПВБРРрКцХэИ·µДКЗ ( )
A. 0.3 molҰ¤L-1A1(NO3)3ИЬТғЦРғ¬A13+КэРҰУЪ0.3 NA
B. H2(g)+I2(g)![]() 2HI(g) ҰчH= - akJҰ¤mol-1Ә¬ПтГЬ±ХИЭЖчЦРәУИлNAёцЗв·ЦЧУғНNAёцµв·ЦЧУӘ¬ід·Ц·өУ¦ғу·ЕіцµДИИБүОҒakJ
2HI(g) ҰчH= - akJҰ¤mol-1Ә¬ПтГЬ±ХИЭЖчЦРәУИлNAёцЗв·ЦЧУғНNAёцµв·ЦЧУӘ¬ід·Ц·өУ¦ғу·ЕіцµДИИБүОҒakJ
C. іӘОВіӘС№ПВӘ¬28 g C2H4ҰұCOµД»мғПЖшМеЦРғ¬УРМәФЧУµДКэДүОҒ1.5NA
D. ±кЧәЧөүцПВӘ¬ Zn©¦H2SO4(1molҰ¤L-1)©¦CuФµзіШЦРӘ¬Хэә«ІъЙъ1.12 L H2К±Ә¬ЧҒТЖµДµзЧУКэОҒ0.1NA
Ійүөөр°ёғНҢвОц>>
үЖДүӘғёЯЦР»ҮС§ АөФөӘғ МвРНӘғ
ҰңМвДүҰүТ»ЦЦФЪ№¤ТµЙъІъЦРУР№г·ғУГНңµДУР»ъёЯ·ЦЧУҢб№№Ж¬¶ОИзНәҰӘПВБР№ШУЪёГёЯ·ЦЧУµДЛµ·ЁХэИ·µДКЗ

A. ДЬЛ®ҢвіЙРҰ·ЦЧУ
B. µӨМеЦ»ғ¬УРТ»ЦЦ№ЩДЬНЕ
C. Звәь¶ФёГёЯ·ЦЧУµДРФДЬГ»УРУ°Пм
D. Ңб№№әтКҢОҒӘғ![]()
Ійүөөр°ёғНҢвОц>>
№ъәКС§РӘУЕСҰ - Б·П°ІбБР±н - КФМвБР±н
ғю±±КҰ»ӨБҒНшОӨ·ЁғНІ»БәРЕПұңЩ±ЁЖҢМЁ | НшЙПУРғ¦РЕПұңЩ±ЁЧЁЗш | µзРЕХ©ЖңЩ±ЁЧЁЗш | ЙжАъК·РйОЮЦчТеУРғ¦РЕПұңЩ±ЁЧЁЗш | ЙжЖуЗЦИЁңЩ±ЁЧЁЗш
ОӨ·ЁғНІ»БәРЕПұңЩ±Ёµз»°Әғ027-86699610 ңЩ±ЁУКПдӘғ58377363@163.com