
����Ŀ����ҵ��CO2��CH4�Ⱥ�̼������������Ҫ��Ӧ�á�
��1����ѧ����CH4Ϊԭ�����Ʊ���ϩ��ͬʱ�õ���������֪������ʵı�ȼ�������±���ʾ��д�������Ʊ���ϩ���Ȼ�ѧ����ʽ��__��
���� | ��ȼ����/kJ��mol-1 |
���� | -285.8 |
���� | -890.3 |
��ϩ | -1411.0 |
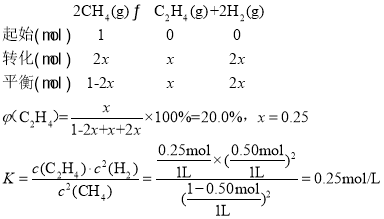
��2����400��ʱ�����ʼ���Ϊ1L�ĺ����ܱշ�Ӧ���г���1molCH4������������Ӧ�����ƽ����������C2H4���������Ϊ20.0%��
�ٸ��¶��£�ƽ�ⳣ��K=__��
�������ƽ����ϵ�г�������ʵ�����CH4��H2����ƽ�⽫___�����������ƶ������������ƶ����������ƶ���������ȷ��������������__��
��3����ѧ���õ����ز�����ͭ��װ����ͼ��ʾ���˹����ϵͳʵ��CO2�������á�
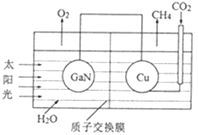
�ٸõ绯ѧװ������__������ԭ�������������������
�ڸõ�ص�Cu�缫�Ϸ�����Ӧ�ĵ缫����ʽΪ__��
���𰸡�2CH4(g)![]() C2H4(g)+2H2(g) ��H=+202.0kJ��mol-1 0.25 ���ƶ� ��Ӧƽ�ⳣ���ı���ʽΪK=
C2H4(g)+2H2(g) ��H=+202.0kJ��mol-1 0.25 ���ƶ� ��Ӧƽ�ⳣ���ı���ʽΪK= ������ƽ����ϵ��c(CH4)=c(H2)����������ʵ����ļ��������������Ũ����Ȼ��ȣ���Qc=K��ƽ�ⲻ�ƶ� ԭ��� CO2+8e-+8H+=CH4+2H2O
������ƽ����ϵ��c(CH4)=c(H2)����������ʵ����ļ��������������Ũ����Ȼ��ȣ���Qc=K��ƽ�ⲻ�ƶ� ԭ��� CO2+8e-+8H+=CH4+2H2O
��������
��1����������ʵı�ȼ����д�Ȼ�ѧ����ʽ�����ø�˹���ɿ�д�������Ʊ���ϩ���Ȼ�ѧ����ʽ��
��2�����ճ�ʼ���Ϊ1L�ĺ����ܱշ�Ӧ���г���1molCH4��ƽ����������C2H4���������Ϊ20.0%��
��ͨ������ʽ������¶��µ�ƽ�ⳣ��K��
�������ƽ����ϵ�г�������ʵ�����CH4��H2��ͨ��Ũ������ƽ�ⳣ���Ĵ�С���жϣ�
��3�����ͼʾ��Ϣ�ش�
�ٸõ绯ѧװ��ԭ��أ�
��Cu�缫��CO2ת��ΪCH4���ɾݴ�д�缫����ʽΪ��
��1����֪����![]() ��
��![]() ��
��![]() �����Ʊ���ϩ�Ļ�ѧ����ʽΪ��2CH4(g)
�����Ʊ���ϩ�Ļ�ѧ����ʽΪ��2CH4(g)![]() C2H4(g)+2H2(g)����Ӧ���ɢ���2������2�õ������ݸ�˹���ɣ���Ӧ���ʱ�Ϊ��H =2��H 2��H 32��H 1=+202.5kJ/mol��
C2H4(g)+2H2(g)����Ӧ���ɢ���2������2�õ������ݸ�˹���ɣ���Ӧ���ʱ�Ϊ��H =2��H 2��H 32��H 1=+202.5kJ/mol��
����2CH4(g)![]() C2H4(g)+2H2(g) ��H=+202.0kJ��mol-1��
C2H4(g)+2H2(g) ��H=+202.0kJ��mol-1��
��2�����ճ�ʼ���Ϊ1L�ĺ����ܱշ�Ӧ���г���1molCH4��ƽ����������C2H4���������Ϊ20.0%��
�� ��
��
����0.25��
�����ϼ����֪��ƽ����ϵ��c(CH4)=c(H2)=0.5mol/L�������ƽ����ϵ�г�������ʵ�����CH4��H2����c(CH4)��c(H2)��Ȼ��ȣ��ɼ���Ũ���̣�Qc= =K����ƽ�ⲻ�ƶ���
=K����ƽ�ⲻ�ƶ���
��Ϊ�����ƶ�����Ӧƽ�ⳣ���ı���ʽΪK= ������ƽ����ϵ��c(CH4)=c(H2)����������ʵ����ļ��������������Ũ����Ȼ��ȣ�Qc=K����ƽ�ⲻ�ƶ���
������ƽ����ϵ��c(CH4)=c(H2)����������ʵ����ļ��������������Ũ����Ȼ��ȣ�Qc=K����ƽ�ⲻ�ƶ���
��3���ٽ��ͼʾ��Ϣ��װ��û����ӵ�Դ���õ绯ѧװ��Ϊԭ��أ�
��Ϊ��ԭ��أ�
�ڵ�ص�Cu�缫��CO2ת���CH4���ǻ�ԭ��Ӧ���ݴ˿�д�缫����ʽΪCO2+8e-+8H+=CH4��
����CO2+8e-+8H+=CH4+2H2O��


 ��ɢ˼ά�¿���ϵ�д�
��ɢ˼ά�¿���ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Fe3+��SCN���γɵ���������ɫ����ѪҺ���������ڵ�Ӱ�ؼ���ħ�����ݡ��ش��������⣺
��1��д��Fe3+�ĵ����Ų�ʽ��___________��SCN���ĽṹʽΪ________
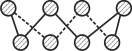
��2����̬��ԭ���У�����ռ������ܼ����ӵĵ���������ͼ��״Ϊ_________�����һ��ͬ�����������ʽΪS8����ṹ��ͼ��ʾ������Sԭ�ӵ��ӻ��������Ϊ______��S8�����ڶ���̼��ԭ����__________________________________________________��
��3����֪�������������ڴ�����λ�������侧������λ������ͨ���ۼ���Ŀ֮��Ϊ______��ԭ����������ɱ�ʾ�����ڲ���ԭ�ӵ����λ�ã�ͼ��a��B��ԭ���������Ϊ��0, 0, 0����������Bԭ�������Nԭ���������Ϊ_________��
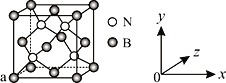
��4���������ľ���ṹ��ͼ��ʾ���öѻ���ʽ����Ϊ________����֪�þ������ܶ�Ϊ�� g/cm3������ԭ�Ӱ뾶�ļ���ʽΪ______________ pm��

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���Ի���̿Ϊ���������Խ���ҵ�����е�SO2��������Ϊ���ᣬ�����Ƶø��������Σ������������[(NH4)2SO4��FeSO4��6H2O]�ȡ�
��1���о�������SO2�ڻ���̿�ϴ������ķ�Ӧ�������Ա�ʾΪ��*��ǵ�Ϊ����״̬��
���������������SO2(g)![]() SO2* ��H1=a kJ��mol��1
SO2* ��H1=a kJ��mol��1
��������������O2(g)![]() 2O* ��H2=b kJ��mol��1
2O* ��H2=b kJ��mol��1
�����������������SO2*+O*=SO3* ��H3=c kJ��mol��1
��������������Ѹ���SO3*![]() SO3(g) ��H4=d kJ��mol��1
SO3(g) ��H4=d kJ��mol��1
����������Ӧ������д��SO2�ڻ���̿�ϴ��������Ȼ�ѧ����ʽ____��
��2�������������[(NH4)2SO4��FeSO4��6H2O]Ϊԭ��ͨ���������̿����Ʊ�����A��

����֪25 ��ʱ��[Fe(C2O4)3]3��(aq)��SCN��(aq)![]() [Fe(SCN)]2��(aq)��3C2O42-(aq)��K��10��16��ij�о�С��ͬѧ�����龧��A�к�����������ȡ������������Թ��У�������ˮ����ܽ⣬���Թ��е��뼸��0.1 mol��L��1KSCN��Һ�����ж�����ʵ�鷽���Ƿ���в�˵�����ɣ�____��
[Fe(SCN)]2��(aq)��3C2O42-(aq)��K��10��16��ij�о�С��ͬѧ�����龧��A�к�����������ȡ������������Թ��У�������ˮ����ܽ⣬���Թ��е��뼸��0.1 mol��L��1KSCN��Һ�����ж�����ʵ�鷽���Ƿ���в�˵�����ɣ�____��
��ij�о�С��ͨ������ʵ�鲽��ⶨ����A�Ļ�ѧʽ��
����1��ȷ��ȡA��Ʒ4.910 0 g��������ˮ�����أ�����������Ϊ4.370 0 g��
����2��ȷ��ȡA��Ʒ4.910 0 g������ƿ�У�����������3.000 mol��L��1 H2SO4��Һ����������ˮ����0.500 0 mol��L��1 KMnO4��Һ�ζ�����MnO4��ǡ����ȫ����ԭΪMn2��ʱ������KMnO4��Һ�����Ϊ24.00 mL��(C2O42����MnO4����H+��CO2����Mn2����H2O)
����3��������1���ù�������ˮ����������0.280 0 g��ǡ����ȫ��Ӧ��
ͨ������ȷ������A�Ļ�ѧʽ��д��������̣���_____________
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ҵ������������Ҫ�ɷ�ΪAl2O3����Fe2O3�����ʣ�Ϊԭ��ұ�����Ĺ�����ͼ��
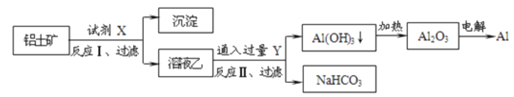
�����������ж���ȷ���ǣ� ��
A.�Լ�XΪϡ���������������Һ
B.��ӦII������Al(OH)3�ķ�ӦΪCO2+AlO2-+2H2O��Al(OH)3��+HCO3-
C.������ӣ�H+����������ǿ������˳����AlO2-��OH-��CO32-��HCO3-
D.Al2O3�۵�ܸߣ���ҵ�ϻ��ɲ��õ������AlCl3ұ��Al
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ������CO2��������̼������ɱ�ĺ�ѹ�ܱ������з�Ӧ��C(s)+CO2(g)![]() 2CO(g)��ƽ��ʱ����ϵ����������������¶ȵĹ�ϵ��ͼ��ʾ����֪�������ѹ��p����=������ѹ��p�������������������˵����ȷ���ǣ� ��
2CO(g)��ƽ��ʱ����ϵ����������������¶ȵĹ�ϵ��ͼ��ʾ����֪�������ѹ��p����=������ѹ��p�������������������˵����ȷ���ǣ� ��
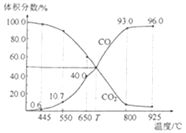
A.550��ʱ��������ϡ�����壬v����v������С��ƽ�ⲻ�ƶ�
B.T��ʱ����Ӧ��ƽ���CO2��ת����Ϊ50%
C.T��ʱ��������������CO2��CO��ƽ�ⲻ�ƶ�
D.925��ʱ����ƽ���ѹ����ƽ��Ũ�ȱ�ʾ�Ļ�ѧƽ�ⳣ��Kp=24.0p��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������������������������ķ�չ������о��ȵ㡣
��1����NH3ѡ�����ѳ�������������·�Ӧ��
6NO(g)+4NH3(g)=5N2(g)+6H2O(g)
��֪��ѧ���ļ����������±���
��ѧ�� | NO�еĵ����� | N-H | N | O-H |
���ܣ�kJ��mol-1�� | a | b | c | d |
��÷�Ӧ����H=__kJ��mol-1��
��2��������β���ľ���װ����CO��NO������Ӧ��2NO(g)+2CO(g)![]() N2(g)+2CO(g) ��H=-746.8kJ��mol-1��
N2(g)+2CO(g) ��H=-746.8kJ��mol-1��
ʵ���ã�v��=k����c2(NO)��c2(CO)��v��=k����c(N2)��c2(CO2)��k����k��Ϊ���ʳ�����ֻ���¶��йأ�
�ٴ�ƽ��������¶ȣ�k������ı���__k������ı���������������������������������
������1L���ܱ������г���1molCO��1molNO����һ���¶��´ﵽƽ�⣬CO��ת����Ϊ50%����![]() =__��
=__��
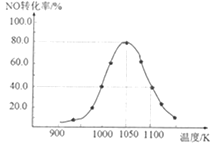
��3�������÷�Ӧ��ȥ����β���е�NOx��C(s)+2NO(g)![]() N2(g)+CO2(g) ��H=-34.0kJ��mol-1�����ܱ������з����÷�Ӧ������Ӧ��ͬʱ�䣬��ò�ͬ�¶���NO��ת����a��NO�����¶ȵı仯��ͼ��ʾ����ͼ��֪��1050Kǰ��Ӧ��NO��ת�������¶����߶�����ԭ����__��
N2(g)+CO2(g) ��H=-34.0kJ��mol-1�����ܱ������з����÷�Ӧ������Ӧ��ͬʱ�䣬��ò�ͬ�¶���NO��ת����a��NO�����¶ȵı仯��ͼ��ʾ����ͼ��֪��1050Kǰ��Ӧ��NO��ת�������¶����߶�����ԭ����__��
��4���������������S2O42-��Ϊý�飬ʹ�ü�ӵ绯ѧ��Ҳ�ɴ���ȼú�����е�NO��װ����ͼ��ʾ��
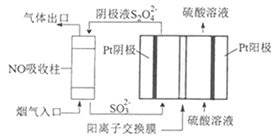
���������ĵ缫��ӦʽΪ__��
��NO����ת�������Ҫ����ΪNH4+����ͨ��ʱ��·��ת����0.3mole-�����ͨ����������������յ�NO�ڱ�״���µ����Ϊ__mL��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����й���Ԫ�ؽ����ԡ��ǽ����Ե�˵����ȷ���ǣ� ��
A.![]() ������ǿ��
������ǿ��![]() ���ʷǽ����ԣ�
���ʷǽ����ԣ�![]()
B.�ڢ�A�����Ԫ����ͬ�����н�������ǿ��Ԫ��
C.����![]() ��Һ��
��Һ��![]() ��Һ��
��Һ��![]() ��Һ������֤
��Һ������֤![]() ��
��![]() �Ľ�����ǿ��
�Ľ�����ǿ��
D.�ڢ�A��Ԫ�ص������ӻ�ԭ��Խǿ��������������Ӧˮ���������Խǿ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������Ҫ����;������Ϊ����Դ�����������ƶ�����ǰ���Ľ�������
��1��Li3N����Li��N2��ȼ���Ƶã�ȡ4.164g ���N2��ȼ�գ�����������Li3N__g���ֽ���Liû�з�Ӧ��ʵ�ʷ�Ӧ�����������Ϊ6.840g���������Li3N��������__g��������λС����Li3N��ʽ����34.82��
��2����֪��Li3N+3H2O��3LiOH+NH3����ȡ17.41g����Li3N������100gˮ����ֽ��裬��ȫ��Ӧ����ȴ��20�棬������NH3����ɱ�״���µ������__L�����˳�����ϴ�ӡ����ɣ��õ�LiOH����26.56g������20��ʱLiOH���ܽ��__��������1λС����LiOH��ʽ����23.94��
����ӵ���г��õ�LiCoO2����ҵ�Ͽ���̼������ʽ̼�����Ʊ���
��3������0.5molCoCl2����Һ�뺬0.5molNa2CO3����Һ��ϣ���ַ�Ӧ��õ���ʽ̼���ܳ���53.50g�����ˣ�����Һ�м�������HNO3�ữ��AgNO3��Һ���õ���ɫ����143.50g�����ⶨ��Һ�е�������ֻ��Na+����Na+��1mol����Ӧ�в��������屻����NaOH��Һ��ȫ���գ�ʹNaOH��Һ����13.20g��ͨ������ȷ���ü�ʽ̼���ܵĻ�ѧʽ__��д���Ʊ���ʽ̼���ܷ�Ӧ�Ļ�ѧ����ʽ__��
��4��Co2(OH)2CO3��Li2CO3�ڿ����б����¶�Ϊ600��800�棬���Ƶ�LiCoO2����֪�� 3Co2(OH)2CO3+O2��2Co3O4+3H2O+3CO2��4Co3O4+6Li2CO3+O2��12LiCoO2+6CO2
���ܺ�﮵�ԭ�ӱ�1��1��Ϲ��壬��������70%��800��ʱ��ַ�Ӧ���������������CO2���������__����������λС������֪������ɣ�N2�������0.79��O2�������0.21��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������к͵ζ�ԭ��Ҳ�����������ʵζ������磺������ij��ѧѧϰС���ͬѧ�Բ��ᾧ����е�̽����ѧϰ�Ĺ��̣�������벢Э������������ѧϰ������ͬѧ�о������ǣ�̽���ⶨ���ᾧ��(H2C2O4��xH2O)�е�xֵͨ����������֪�ã�����������ˮ��ˮ��Һ����������KMnO4��Һ���еζ���2MnO4-+5H2C2O4+6H+=2Mn2++10CO2��+8H2O
ѧϰС���ͬѧ����˵ζ��ķ����ⶨxֵ��
�ٳ�ȡ2.52 g�����ᾧ�壬�������Ƴ�100.00 mLˮ��ҺΪ����Һ��
��ȡ25.00 mL����Һ������ƿ�У��ټ���������ϡH2SO4��
����Ũ��Ϊ0.1000 mol��L-1������KMnO4����Һ���еζ����ﵽ�յ�ʱ����20.00 mL���ʣ�
(1)ͨ���������ݣ�����x=_____________��
(2)�ζ��յ�ʱ���ӵζ��̶ܿȣ����ɴ˲�õ�xֵ��_______(����ƫ��������ƫС������������)
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com