
【题目】水煤气变换[CO(g)+H2O(g)=CO2(g)+H2(g)]是重要的化工过程,主要用于合成氨、制氢以及合成气加工等工业领域中。回答下列问题:
(1)Shibata曾做过下列实验:①使纯H2缓慢地通过处于721 ℃下的过量氧化钴CoO(s),氧化钴部分被还原为金属钴(Co),平衡后气体中H2的物质的量分数为0.0250。
②在同一温度下用CO还原CoO(s),平衡后气体中CO的物质的量分数为0.0192。根据上述实验结果判断,还原CoO(s)为Co(s)的倾向是CO_________H2(填“大于”或“小于”)。
(2)721 ℃时,在密闭容器中将等物质的量的CO(g)和H2O(g)混合,采用适当的催化剂进行反应,则平衡时体系中H2的物质的量分数为_________(填标号)。
A.<0.25 B.0.25 C.0.25~0.50 D.0.50 E.>0.50
(3)我国学者结合实验与计算机模拟结果,研究了在金催化剂表面上水煤气变换的反应历程,如图所示,其中吸附在金催化剂表面上的物种用![]() 标注。
标注。
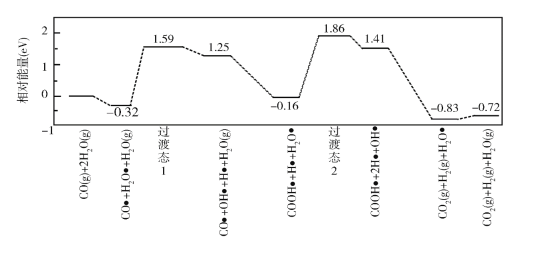
可知水煤气变换的ΔH________0(填“大于”“等于”或“小于”),该历程中最大能垒(活化能)E正=_________eV,写出该步骤的化学方程式_______________________。
【答案】大于 C 小于 2.02 COOH![]() +H
+H![]() +H2O
+H2O![]() =COOH
=COOH![]() +2H
+2H![]() +OH
+OH![]() 或H2O
或H2O![]() =H
=H![]() +OH
+OH![]()
【解析】
(1)通过气体所占物质的量分数结合反应方程式判断;
(2)CO(g)+H2O(g)=CO2(g)+H2(g),等物质的量的一氧化碳和水蒸气反应生成二氧化碳和氢气,反应前后气体物质的量不变,当反应物全部反应氢气所占物质的量的分数50%,但反应为可逆反应不能进行彻底;
(3)图象分析可知水煤气的生成过程经过了过渡态1和过渡态2,最后生成产物的能量低于反应物,正反应进行的方向需要吸收能量,结合图此分析判断,该历程中最大能垒(活化能)E正,得到反应的化学方程式;
:(1)①反应的化学方程式:H2+CoOCo+H2O,②反应的化学方程式:CO+CoOCo+CO2,相同条件下还原反应达到平衡状态后,反应前后气体物质的量都是不变的反应,一氧化碳物质的量分数小于氢气物质的量分数,说明一氧化碳进行的程度大
故答案为:大于;
(2)假设氢气的物质的量为1mol,①H2+CoOCo+H2O中反应后氢气的物质的量分数可求出该温度下反应的平衡常数,方法如下:
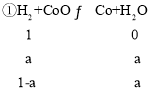
K1=![]() =a/(1-a);其中(1-a)/1=0.025;故K1=39;用同样方法求出反应②反应CO+CoOCo+CO2的平衡常数K2=
=a/(1-a);其中(1-a)/1=0.025;故K1=39;用同样方法求出反应②反应CO+CoOCo+CO2的平衡常数K2=![]() =51;反应CO(g)+H2O(g)=CO2(g)+H2(g)平衡常数K=
=51;反应CO(g)+H2O(g)=CO2(g)+H2(g)平衡常数K=![]() >1;当K=
>1;当K=![]() =1时,
=1时,![]() =
=![]() =
=![]() =
=![]() ,此时氢气的物质的量分数为0.25;当反应物全部反应氢气所占物质的量的分数0.50,但反应为可逆反应不能进行彻底,综上所述氢气的物质的量分数应大于0.25小于0.50,
,此时氢气的物质的量分数为0.25;当反应物全部反应氢气所占物质的量的分数0.50,但反应为可逆反应不能进行彻底,综上所述氢气的物质的量分数应大于0.25小于0.50,
故答案为:C;
(3)图象分析可知水煤气的生成过程经过了过渡态1和过渡态2,最后生成产物的能量低于反应物,反应的焓变小于0,正反应进行的方向需要吸收能量,结合图此分析判断,是发生的过渡反应:COOH![]() +H2O
+H2O![]() =COOH
=COOH![]() +2H
+2H![]() +OH
+OH![]() 或H2O
或H2O![]() =H
=H![]() +OH
+OH![]() ,该历程中最大能垒(活化能)E正=1.86eV-(-0.16eV)=2.02eV,
,该历程中最大能垒(活化能)E正=1.86eV-(-0.16eV)=2.02eV,
故答案为:小于;2.02;COOH![]() +H
+H![]() +H2O
+H2O![]() =COOH
=COOH![]() +2H
+2H![]() +OH
+OH![]() 或H2O
或H2O![]() =H
=H![]() +OH
+OH![]() ;
;


科目:高中化学 来源: 题型:
【题目】青蒿素是高效的抗疟疾药,为无色针状晶体,易溶于丙酮、氯仿和苯中,在甲醇、乙醇、乙醚、石油醚中可溶解,在水中几乎不溶,熔点为156~157℃,热稳定性差。已知:乙醚沸点35℃,提取青蒿素的主要工艺为:

下列有关此工艺操作的说法不正确的是
A.破碎的目的是增大青蒿与乙醚的接触面积,提高青蒿素浸取率
B.操作I需要用到的玻璃仪器有漏斗、玻璃棒、烧杯
C.操作II是蒸馏,利用了乙醚与青蒿素的沸点相差较大
D.操作II的主要过程为加水溶解,蒸发浓缩、冷却结晶、过滤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知2CO(g)+O2(g)=2CO2(g) ΔH= -566 kJmol-1
Na2O2(s)+CO2(g) = Na2CO3(s)+1/2O2(g) ΔH= -226 kJmol-1
下列表述正确的是
A.1molCO燃烧时放出的热量为283kJmol-1
B.Na2O2(s)+CO(g)=Na2CO3(s)ΔH=-509kJmol-1
C.Na2O2(s)与CO2(g)反应放出226kJ热量时电子转移数为2NA
D.Na2O2和Na2CO3中阴阳离子个数比不同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】臭氧在烟气脱硝中的反应为2NO2(g)+O3(g)![]() N2O5(g)+O2(g)。若此反应在恒容密闭容器中进行,下列选项中有关图象对应的分析正确的是( )
N2O5(g)+O2(g)。若此反应在恒容密闭容器中进行,下列选项中有关图象对应的分析正确的是( )
A.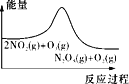 平衡后升温,NO2含量降低
平衡后升温,NO2含量降低
B.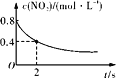 0~2 s内,v(O3)=0.2 mol·L-1·s-1
0~2 s内,v(O3)=0.2 mol·L-1·s-1
C.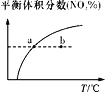 v正:b点>a点,b点:v逆 > v正
v正:b点>a点,b点:v逆 > v正
D.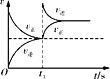 恒温,t1时再充入O3
恒温,t1时再充入O3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃下,向20mL0.1molL-1HA溶液中逐滴加入0.1molL-1NaOH溶液,随滴入NaOH溶液体积的变化混合溶液的pH的变化如图所示。下列说法正确的是( )
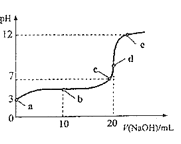
A.A-的水解常数约为10-11
B.水的电离程度:e>d>c>b>a
C.c点和d点溶液中均符合c(Na+)=c(A-)
D.b点溶液中粒子浓度关系:c(A-)>c(HA)>c(H+)>c(OH-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】能表示H2(g)+ I2(g)![]() 2HI(g)已经达到平衡状态的标志是( )
2HI(g)已经达到平衡状态的标志是( )
①c(H2)=c(I2)=c(HI)时
②c(H2):c(I2):c(HI)=1:1:2时
③c(H2)、c(I2)、c(HI)不再随时间而改变
④单位时间内生成nmolH2的同时生成2nmolHI
⑤单位时间内生成nmolH2的同时生成nmolI2
⑥反应速v(H2)=v(I2)=1/2v(HI)
⑦一个H-H键断裂的同时有两个H-I键断裂
⑧温度和体积一定时,容器内压强不再变化
⑨温度和体积一定时,混合气体的颜色不再变化
⑩温度和压强一定时,混合气体的密度不再变化
条件一定,混合气体的平均相对分子质量不再变化
A.③④⑦⑨⑩B.③④⑦⑨C.②③④⑦⑨D.②③④⑥⑦⑨
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】C、N、S的氧化物常会造成一些环境问题,科研工作者正在研究用各种化学方法来消除这些物质对环境的不利影响。
(1)已知:2CO(g)+O2(g)=2CO2(g) ΔH1=-566kJ/molS(l)+O2(g)=SO2(g) ΔH2=-296kJ/mol
一定条件下,可以通过CO与SO2反应生成S(1)和一种无毒的气体,实现燃煤烟气中硫的回收,写出该反应的热化学方程式_______________________________。
(2)在500℃下合成甲醇的反应原理为:
CO2(g)+3H2(g) ![]() CH3OH(g)+H2O(g);在1L的密闭容器中,充入1mol CO2和3mol H2,压强为p0 kpa,测得CO2(g)和CH3OH(g)的浓度随时间变化如图所示。(可逆反应的平衡常数可以用平衡浓度计算,也可以用平衡分压Kp代替平衡浓度,计算分压=总压×物质的量分数)
CH3OH(g)+H2O(g);在1L的密闭容器中,充入1mol CO2和3mol H2,压强为p0 kpa,测得CO2(g)和CH3OH(g)的浓度随时间变化如图所示。(可逆反应的平衡常数可以用平衡浓度计算,也可以用平衡分压Kp代替平衡浓度,计算分压=总压×物质的量分数)

①0~4min,H2的平均反应速率v(H2)=________mol·L1·min1。
②CO2平衡时的体积分数为______________,该温度下Kp为_________kPa-2_(用含有p0的式子表示,小数点后保留1位)。
③下列能说明该反应已达到平衡状态的是______________。
A.v正(CH3OH)=3v逆(H2)
B.CO2、H2、CH3OH和H2O浓度之比为1∶3∶1∶1
C.恒温恒压下,气体的体积不再变化
D.恒温恒容下,气体的密度不再变化
④500℃、在2个容积都是2L的密闭容器中,按不同方式投入反应物,保持恒温、恒容,测得反应达到平衡时的有关数据如下:
容器 | 容器甲 | 容器乙 |
反应物起始投入量 | 1mol CO2,3mol H2 | 0.5mol CO2,1mol H2 1mol CH3OH,1mol H2O |
CH3OH的平衡浓度/mol·L1 | C1 | C2 |
则乙容器中反应起始向________(填“正反应”或“逆反应”)方向进行;c1_________(填“>”“<”或“=”)c2。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】探究Na2O2与水的反应,实验如图:(已知:H2O2 ![]() H+ + HO2-、HO2-
H+ + HO2-、HO2- ![]() H+ + O22-)下列分析不正确的是
H+ + O22-)下列分析不正确的是
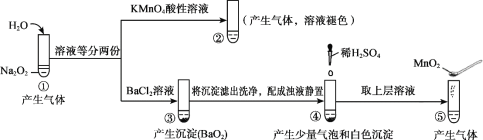
A. ①、⑤中产生的气体能使带火星的木条复燃
B. ①、④中均发生了氧化还原反应和复分解反应
C. ②、⑤中KMnO4与MnO2的作用不同,产生气体的量也不同
D. 通过③能比较酸性:HCl>H2O2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮氧化物与悬浮在大气中海盐粒子的相互反应:4NO2(g)+2NaCl(s) ![]() 2NaNO3(s)+2NO(g)+Cl2(g)
2NaNO3(s)+2NO(g)+Cl2(g) ![]() 在恒温条件下,向2L恒容密闭容器中加入0.4molNO2和0.2molNaCl,10min反应达到平衡时n(NaNO3)=0.1mol,NO2的转化率为
在恒温条件下,向2L恒容密闭容器中加入0.4molNO2和0.2molNaCl,10min反应达到平衡时n(NaNO3)=0.1mol,NO2的转化率为![]() 。下列叙述中正确的是
。下列叙述中正确的是
A. 10min内NO浓度变化表示的速率υ(NO)=0.01mol·L-1·min-1
B. 若升高温度,平衡逆向移动,则该反应的![]()
C. 若起始时向该容器中充入0.1molNO2(g)、0.2molNO(g)和0.1molCl2(g)(固体物质足量),则反应将向逆反应方向进行
D. 若保持其他条件不变,在恒压下进行该反应,则平衡时NO2的转化率小于![]()
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com