
【题目】铅蓄电池是典型的可充电电池,在现代生活中有着广泛的应用,其充电、放电按下式进行:Pb+PbO2+2H2SO4 ![]() 2PbSO4+2H2O,有关该电池的说法正确的( )
2PbSO4+2H2O,有关该电池的说法正确的( )
A.放电时,电解质溶液的pH不断降低且正负极均有PbSO4 生成
B.放电时,每通过1mol电子,蓄电池就要消耗2mol H2SO4
C.充电时,阳极反应:PbSO4+2e﹣=Pb+SO42﹣
D.充电时,铅蓄电池的负极与外接电源的负极相连
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】实验室需要0.10mol/L的硫酸950mL,某同学欲用密度为![]() 、溶质的质量分数为98%的浓硫酸进行配制。试回答:
、溶质的质量分数为98%的浓硫酸进行配制。试回答:
(1)需选用________容量瓶(填序号)。
A. 50 mL B. 100 mL C. 250 mL D. 1000 mL
(2)需量取98%浓硫酸的体积为_______mL。
(3)若提供如下仪器:
A. 量筒 B. 托盘天平 C. 玻璃棒 D. 容量瓶 E. 胶头滴管 F. 烧杯
完成该实验需选用哪些仪器?请按使用的先后顺序将仪器标号填在横线上:__________________。
(4)下列操作会使所配制的溶液物质的量浓度一定偏低的是_________。
A. 容量瓶洗净后未经干燥处理
B. 向容量瓶转移溶液时,有少量液体溅出
C. 量取浓硫酸时,仰视刻度线
D. 未洗涤烧杯玻璃棒
(5)下列关于容量瓶的使用方法中,正确的是_________(填序号)。
A. 使用前要检验是否漏水 B. 在容量瓶中直接溶解固体或稀释液体
C. 溶液未经冷却即注入容量瓶中 D. 向容量瓶中转移溶液要用玻璃棒引流
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在CuC12和FeC12的混合溶液中,加入一定量的锌粉,充分反应后过滤,向滤渣中加稀盐酸,有气体生成,则滤渣中一定含有
A. Cu、Fe和ZnB. Cu和FeC. Zn和CuD. Fe和Zn
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列条件下,两瓶气体所含原子数一定相等的是( )
A. 同压强、同体积的N2O和CO2 B. 同温度、同体积的H2和N2
C. 同体积、同密度的CH4和C3H6 D. 同质量、不同密度的N2和CO
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下,H2O2在水溶液中发生分解反应:2H2O2![]() 2H2O+O2↑反应过程中,测得不同时间H2O2的物质的量浓度如下表:
2H2O+O2↑反应过程中,测得不同时间H2O2的物质的量浓度如下表:
t/min | 0 | 20 | 40 | 60 | 80 |
c(H2O2)/molL﹣1 | 0.80 | 0.40 | 0.20 | 0.10 | 0.05 |
① H2O2的分解反应氧化还原反应(填“是”或“不是”).
②该分解反应0─20min的平均反应速率v(H2O2)为molL﹣1 min﹣1 .
③如果反应所用的H2O2溶液为100mL,则共产生O2g.
A.0.08 B.0.16 C.1.28 D.2.4.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室制备氯气(Cl2)的化学方程式如下:
4HCl(浓) + MnO2 ![]() MnCl2 + Cl2↑ +2 H2O
MnCl2 + Cl2↑ +2 H2O
(1)用单线桥表示出电子转移的方向和数目________________________,
(2)将题干中反应改写成离子方程式是___________________________。
(3)在上述过程中,被氧化的元素是_________,还原产物是___________,氧化剂和还原剂的物质的量之比为:__________;该反应中盐酸体现的性质为:__________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)按如图所示操作,充分反应后:
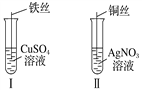
①Ⅰ中铁丝上观察到的现象是______________________;
②Ⅱ中发生反应的离子方程式为_______________________;
③结合Ⅰ、Ⅱ实验现象可知Fe2+、Cu2+、Ag+的氧化性由强到弱的顺序为_____________。
(2)在小烧杯中加入20 mL蒸馏水,加热至沸腾后,向沸水中滴入几滴FeCl3溶液,继续煮沸至溶液呈红褐色,停止加热。
①写出制备氢氧化铁胶体的化学方程式____________________.
②向氢氧化铁胶体中逐滴滴入过量盐酸,出现的实验现象为:___________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将足量CO2通入KOH和Ca(OH)2的混合稀溶液100mL中,生成沉淀的质量(m)与通入(STP)状况下CO2的体积(V)之间关系如图所示:
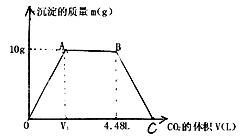
(1)写同下列各段发生的离子方程式
①OA_____________________ ;
②AB_____________________;
③BC_____________________;
(2)C点对应溶液中溶质离子有:_____________________;
(3)V1=_________________L;
(4)KOH物质的量浓度c=____________________mol·L-1。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有关浓硫酸的性质或作用,叙述错误的是
A.浓硫酸的脱水性是化学性质
B.使铁、铝钝化表现了强氧化性
C.制备乙酸乙酯的反应中起催化脱水作用
D.与氯化钠固体共热制氯化氢气体时,表现强酸性
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com