
【题目】已知最外层电子数相等的元素的原子具有相似的化学性质。下列原子中,与氯元素原子的化学性质相似的是( )
A.NeB.MgC.OD.Br
 长江作业本同步练习册系列答案
长江作业本同步练习册系列答案科目:高中化学 来源: 题型:
【题目】铜及其化合物在生产生活中用途广泛。回答下列问题:
(1)目前,低压甲醇铜基催化剂的主要组分是CuO、ZnO和Al2O3,下列氧原子电子排布图表示的状态中,能量最高的是______(填序号)。
A.
B.
C.
D.
(2)铜离子是人体内多种酶的辅因子,某化合物与Cu+结合形成如下图所示的离子。

①该离子中含有化学键的类型有______(填序号)。
A.极性键 B.离子键 C.非极性键 D.配位键
②该离子中碳原子的杂化方式有______。
③H、N、Cu三种元素的电负性由大到小的顺序是______。
(3)甲醇(CH3OH)在Cu催化作用下被氧化成甲醛(HCHO)。甲醛分子内σ键与π键个数之比为______。甲醇分子内的O-C-H键角______(填“大于”“等于”或“小于”)甲醛分子内的O-C-H键角。
(4)某磷青铜晶胞结构如下图所示:

①其中原子坐标参数A为(0,0,0);B为(0,![]() ,
,![]() )。则P原子的坐标参数为______。
)。则P原子的坐标参数为______。
②该晶体中距离Cu原子最近的Sn原子有______个,这些Sn原子所呈现的构型为______。
③若晶体密度为agcm3,最近的Cu原子核间距为______pm(用含NA和a的代数式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】COCl2(g)![]() CO(g)+Cl2(g) ΔH>0,当反应达到平衡时,下列措施:①升温 ②恒容通入稀有气体 ③增加CO浓度 ④减压 ⑤加催化剂 ⑥恒压通入稀有气体,能提高COCl2转化率的是( )
CO(g)+Cl2(g) ΔH>0,当反应达到平衡时,下列措施:①升温 ②恒容通入稀有气体 ③增加CO浓度 ④减压 ⑤加催化剂 ⑥恒压通入稀有气体,能提高COCl2转化率的是( )
A. ①②④ B. ①④⑥ C. ②③⑤ D. ③⑤⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上利用N2和H2可以实现合成氨气,而氨又可以进一步制备硝酸,在工业上一般可进行连续生产。请回答下列有关问题:
(1)已知N2(g)+O2(g)=2NO(g) △H=+180.5kJ·mol-1
N2(g)+3H2(g)![]() 2NH3(g) △H=-92.4kJ.mol-1
2NH3(g) △H=-92.4kJ.mol-1
2H2(g)+O2(g)=2H2O(g) △H=-483.6kJ·mol-1
写出氨气经催化氧化完全生成一氧化氮和水蒸气的热化学方程式为___________。
(2)在一定体积的密闭容器中,进行如下化学反应:N2(g)+3H2(g)![]() 2NH3(g),其化学平衡常数K与温度t的关系如下表:
2NH3(g),其化学平衡常数K与温度t的关系如下表:
t/K | 298 | 398 | 498 | ...... |
K/(mol/L)2 | 4.1×106 | K1 | K2 | ...... |
完成下列问题:
①比较K1、K2的大小:K1___________K2(填“>”、“=”或“<”);
②在同温同压下判断该反应达到化学平衡状态的依据是___________(填序号);
A.2v(H2)(正)=3v(NH3)(逆) B.2v(N2) (正)=v(H2) (逆)
C.容器内压强保持不变 D.混合气体的密度保持不变
(3)硝酸工业的尾气NO可用于制备NH4NO3,其工作原理如图。

①其阴极的电极反应式为___________。
②常温下,1LpH=6的NH4NO3溶液中c(NH3·H2O)+c(OH-)=___________mol·L-1。
(4)工业上生产尿素的化学方程式为:
2NH3(g)+CO2(g)![]() CO(NH2)2(s)+H2O(l)
CO(NH2)2(s)+H2O(l)
在T℃,体积为4L的密闭容器中,通入6molNH3和3 mol CO2,反应达到平衡时,c(NH3)=0.5mol·L-1,e(CO2)=0.25mol·L-1。若此时保持T℃和平衡时容器的压强不变,再向体积可变的容器中充入3molNH3,则此时反应的V正___________V逆(填“>”“<”或“=”)。再次平衡后,平衡常数为___________。
(5)已知Ksp(AgCl)=1.8×10-10,若向50mL0.09mo1·L-1的AgNO3溶液中加入50mL0.10mol·L-1的盐酸,混合后溶液中的Ag+的浓度为___________mol·L-1。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物F(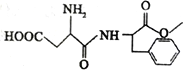 )是一种应用广泛可食用的甜味剂,俗称蛋白糖,它的一种合成路线如图所示
)是一种应用广泛可食用的甜味剂,俗称蛋白糖,它的一种合成路线如图所示

已知:①A能发生银镜反应
②
③R-CN![]() R-COOH
R-COOH
请回答下列问题:
(1)D中官能团的名称为___________,F的分子式为___________。
(2)A的名称为___________,反应③的反应类型为___________。
(3)反应④的化学方程式为___________。
(4)反应⑤中的另一种生成物是水,则X的结构简式为___________。
(5)D有多种同分异构体,请写出一种符合下列条件的有机物的结构简式___________;
①苯环上有2个取代基
②与D具有相同的官能团
③核破共振氢谱为6组峰且峰面积比为2:2:2:2:2:1
(6)丙烯酸是重要的有机合成原料及合成树脂单体,请写出以CH3CHO为原料合成丙烯酸的合成路线___________(其它试剂任选)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氢元素与其他元素形成的二元化合物称为氢化物,有关氢化物的叙述正确的是
A. HF的电子式为![]() B. H2O的空间构型为直线型
B. H2O的空间构型为直线型
C. NH3的结构式为![]() D. CH4的比例模型为
D. CH4的比例模型为![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上用_______和_______作为原料来制取漂粉精,反应的化学方程式为_______;粉精长期暴露在空气中,会使其失效,主要化学方程式__________;______________________,故其应_______保存。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】1993年8月,国际原子量委员会确认我国张青莲教授测定的锑的相对原子质量(121.760)为标准原子量,已知锑有两种以上天然同位素,则121.760是( )
A.锑元素的质量与12C原子质量1/12的比值
B.一个锑原子的质量与12C原子质量1/12的比值
C.按各种锑的天然同位素的相对原子质量与这些同位素所占的一定百分比计算出的平均值
D.按各种锑的天然同位素质量数与这些同位素所占的一定百分比计算出的平均值
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究化学反应的速率、限度及能量变化具有重要意义。
⑴实验室用锌粒和稀硫酸反应制氢气,能加快反应速率的方法有:______、______。
⑵工业上合成氨反应(N2+3H2![]() 2NH3)中物质的能量随时间的变化如下图所示。
2NH3)中物质的能量随时间的变化如下图所示。

①该反应为______(填“放热”或“放热”)反应。
②若起始N2和H2的体积比为1∶3,控制一定的条件,___(填“能”或“不能”)使反应物的转化率达到100%。
③下列过程放出热量的是______。(填字母)
A.甲烷燃烧
B.碳酸钙分解
C.液氨汽化
D.化学键断裂
⑶图为铜锌原电池示意图。

①原电池工作时的能量转化方式为______。
②原电池工作时,导线中电子的流向为______。
③Cu电极表面的现象为______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com