
【题目】铜镁合金2.14 g完全溶于一定浓度的硝酸,硝酸被还原成NO2、NO、N2O三种气体且标准况下它们体积均为0.224 L。反应后的溶液中加入足量氢氧化钠溶液,生成的沉淀经过滤、洗涤、干燥后称量,质量为
A.3.12 gB.4.68 gC.5.08 gD.4.18 g
【答案】D
【解析】
铜镁合金溶于一定浓度的硝酸,反应生成Mg(NO3)2、Cu(NO3)2、NO2、NO、N2O和H2O,反应后的溶液中加入足量NaOH溶液所得沉淀为Mg(OH)2和Cu(OH)2,沉淀的质量等于原铜镁合金的质量与OH-的质量之和;而n(NO2)=n(NO)=n(N2O)= ![]() =0.01mol;铜镁合金溶于一定浓度的硝酸发生氧化还原反应,反应中铜、镁失去的电子总物质的量等于HNO3得到的电子总物质的量,HNO3得到电子被还原成NO2、NO、N2O,则2n(Mg)+2n(Cu)=0.01mol×[(+5)-(+4)]+ 0.01mol×[(+5)-(+2)]+ 0.01mol×2×[(+5)-(+1)]=0.12mol;根据沉淀的组成Mg(OH)2和Cu(OH)2,沉淀中n(OH-)=2n(Mg2+)+2n(Cu2+)=2n(Mg)+2n(Cu)=0.12mol,m(OH-)=0.12mol×17g/mol=2.04g;沉淀的质量为2.14g+2.04g=4.18g,答案选D。
=0.01mol;铜镁合金溶于一定浓度的硝酸发生氧化还原反应,反应中铜、镁失去的电子总物质的量等于HNO3得到的电子总物质的量,HNO3得到电子被还原成NO2、NO、N2O,则2n(Mg)+2n(Cu)=0.01mol×[(+5)-(+4)]+ 0.01mol×[(+5)-(+2)]+ 0.01mol×2×[(+5)-(+1)]=0.12mol;根据沉淀的组成Mg(OH)2和Cu(OH)2,沉淀中n(OH-)=2n(Mg2+)+2n(Cu2+)=2n(Mg)+2n(Cu)=0.12mol,m(OH-)=0.12mol×17g/mol=2.04g;沉淀的质量为2.14g+2.04g=4.18g,答案选D。


 直通贵州名校周测月考直通名校系列答案
直通贵州名校周测月考直通名校系列答案科目:高中化学 来源: 题型:
【题目】桶烯(Barrelene)结构简式如图所示,有关说法不正确的是
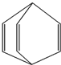
A.桶烯分子中所有的碳原子杂化类型均为sp2杂化
B.桶烯在一定条件下能发生加聚反应
C.桶烯与苯乙烯(C6H5CH=CH2)互为同分异构体
D.桶烯中的一个氢原子被氯原子取代,所得产物只有两种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质的性质比较,结论错误的是
A.硬度:金刚石>碳化硅>晶体硅
B.离子半径:S2->Cl->Na+>O2-
C.熔点:NaF>NaCl>NaBr>NaI
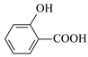
D.沸点:![]() >
>
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国化学侯德榜改革国外的纯碱生产工艺,生产流程可简要表示如下:
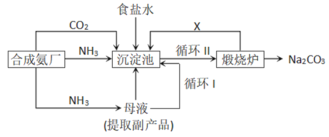
(1)实验室制取氨气的反应方程式为______
(2)上述生产纯碱过程副产品是______。
(3)沉淀池中发生的化学反应方程式是______。
(4)写出上述流程中X物质的电子式______。
(5)使原料氯化钠的利用率从70%提高到90%以上,主要是设计了______(选填循环Ⅰ或循环Ⅱ)的循环。从沉淀池中取出沉淀的操作是_________。
(6)为检验产品碳酸钠中是否含有氯化钠,可取少量试样溶于水后,再滴加________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E都是短周期元素,原子序数依次增大,B、C同周期,A、D同主族。A、B能形成两种常温下的液态化合物甲和乙,原子个数比分别为2∶1和1∶1。根据以上信息回答下列问题:
(1)甲、乙两分子中含有非极性共价键的物质的电子式是________,C元素在周期表中的位置是_____。
(2)C和D的离子中,半径较小的是____(离子符号),以上元素中电负性最大的是____(元素符号)
(3)常温下将D的单质投入甲中,待D消失后再向上述溶液中加入E的固体单质,此时发生反应的化学方程式是______________。
(4)C、D、E可组成离子化合物DxEC6,其晶胞(晶胞是在晶体中具有代表性的最小重复单元)结构如下图所示,阳离子D+(用○表示)位于正方体的棱的中点和正方体内部;阴离子EC6x-(用●表示)位于该正方体的顶点和面心。该化合物的化学式是_________。
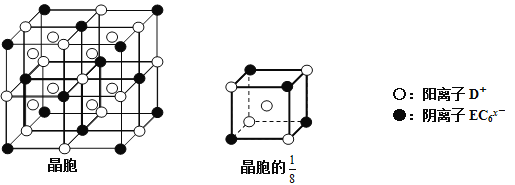
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】三氯化硼(BCl3)是一种重要的化工原料。实验室制备BCl3的原理:
B2O3+3C+3Cl2 =2BCl3+3CO,某实验小组利用干燥的氯气和下列装置(装置可重复使用)制备BCl3并验证反应中有CO生成。(已知:BCl3的熔点为-107.3℃,沸点为12.5℃;硝基苯的密度比水大。)请回答下列问题:
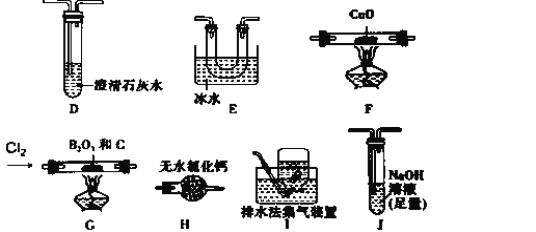
实验Ⅰ:制备BCl3并验证产物CO
(1)BCl3接触潮湿空气时会形成白雾,请写出该反应的化学方程式_______。
(2)该实验装置中合理的连接顺序为G→___→___→__→__→F→D→I;其中装置E的作用是____。
(3)能证明反应中有CO生成的现象是____。
实验Ⅱ:产品中氯含量的测定
①准确称取少许m克产品,置于蒸馏水中完全水解,并配成100mL溶液。
②取10.00mL溶液于锥形瓶中
③加入V1mL浓度为C1 mol/LAgNO3溶液使氯离子完全沉淀;向其中加入少许硝基苯用力摇动。
④以硝酸铁为指示剂,用C2 mol/L KSCN标准溶液滴定过量的AgNO3溶液。重复步骤②~④二次,达到滴定终点时用去KSCN溶液的平均体积为V2mL。
已知:Ksp(AgCl)>Ksp(AgSCN)。
(4)步骤②移取溶液时所需仪器名称为____,步骤④中达到滴定终点的现象为_____。
(5)产品中氯元素的质量分数为_______。
(6)下列操作,可能引起测得产品中氯含量偏高是_____。
A.步骤③中未加硝基苯
B.步骤①中配制100mL溶液时,定容时俯视刻度线
C.用KSCN溶液滴定剩余AgNO3溶液时,滴定前有气泡,滴定后无气泡
D.滴定剩余AgNO3溶液时,KSCN溶液滴到锥形瓶外面一滴
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知短周期元素的离子:aA2+、bB+、cC3-、dD-都具有相同的电子层结构,则下列叙述正确的是( )
A. 原子半径:A>B>D>CB. 原子序数:d>c>b>a
C. 离子半径:C>D>B>AD. 单质的还原性:A>B>D>C
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】锰锌铁氧体是应用广泛的高性能磁性材料。现以akg废旧碱性锌锰电池为原料(含锰元素的物质:MnO2占b%,MnOOH占c%)制备锰锌铁氧体,主要流程如下:
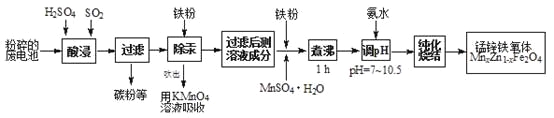
(1)酸浸废电池时,被溶解生成Zn2+的物质有______,SO2的作用是_____(填字母编号)。
A.漂白剂 | B.沉淀剂 | C.氧化剂 | D.还原剂 |
(2)除汞是以氮气为载体吹入滤液带出汞蒸汽,经KMnO4溶液吸收而实现的。如图是KMnO4溶液处于不同pH时对应的单位时间Hg去除率变化图,图中物质为Hg与MnO4-在该pH范围反应的主要产物。
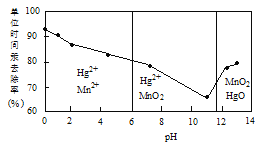
①pH<6时反应的离子方程式为___________。
②汞的去除速率随pH变化的规律是_________。
(3)锌锰干电池中MnO2可以用碳酸锰在空气中煅烧制得。
已知25℃,101 kPa时:2MnO(s)+O2(g)=2MnO2(s) H=-272.0 kJ/mol
MnCO3(s)=MnO(s)+CO2(g) H=+116.6 kJ/mol
碳酸锰在空气中煅烧反应生成MnO2的热化学方程式是_______________。
(4)x=0.2的锰锌铁氧体具有较高的饱和磁场强度,该锰锌铁氧体的组成用氧化物形式(最简整数比)表示为____________。若制得这种锰锌铁氧体的质量为100 kg,在制取过程中不考虑损耗,需补充硫酸锰晶体(MnSO4·H2O)_________kg。(只列出计算式)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】五种短周期元素X、Y、Z、M、W的原子序数与其常见化合价的关系如图所示,下列关系不正确的是( )
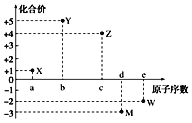
A.元素X可能为锂
B.原子半径大小:r(M)>r(W)
C.X2W中各原子均达到8电子稳定结构
D.元素气态氢化物的稳定性:Y>M
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com