
 考前必练系列答案
考前必练系列答案科目:高中化学 来源: 题型:
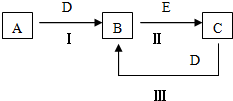 A、B、C、D、E为中学化学常见的单质或化合物,相互转化关系如图所示.
A、B、C、D、E为中学化学常见的单质或化合物,相互转化关系如图所示.查看答案和解析>>
科目:高中化学 来源: 题型:
| A、10 mL |
| B、5 mL |
| C、大于5 mL |
| D、小于5 mL |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、2A+3B=2C |
| B、A+3B=2C |
| C、3A+B=2C |
| D、A+B=C |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、② | B、③④ | C、②④ | D、①④ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、反应NH3(g)+HCl(g)═NH4Cl(s)在室温下可自发进行,则该反应的△H<0 |
| B、当镀锡铁和镀锌铁镀层破损时,后者更易被腐蚀 |
| C、CH3COOH溶液加水稀释后,电离平衡正向移动,溶液中的c(CH3COO-)增大 |
| D、Na2CO3溶液中加入少量Ca(OH)2固体,CO32-水解程度减小,溶液的pH减小 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com