
【题目】已知反应A2(g)+3B2(g)![]() 2AB3(g) ΔH<0,下列说法正确的是
2AB3(g) ΔH<0,下列说法正确的是
A. 升高温度,正、逆反应速率都加快,且正反应速率加快更明显
B. 升高温度能缩短达到平衡所需的时间且提高A2的转化率
C. 达到平衡后,同时升高温度和增大压强,n(AB3)有可能不变
D. 达到平衡后,降低温度或减小压强都有利于该平衡向正反应方向移动
 优秀生应用题卡口算天天练系列答案
优秀生应用题卡口算天天练系列答案 浙江之星课时优化作业系列答案
浙江之星课时优化作业系列答案 激活思维优加课堂系列答案
激活思维优加课堂系列答案科目:高中化学 来源: 题型:
【题目】ClO2是一种强氧化性气体(高浓度时呈红黄色,低浓度时呈黄色),在消毒和果蔬保鲜等方面应用广泛。某兴趣小组通过下图所示装置(夹持装置略)对其进行制备、收集、吸收并制取NaClO2。
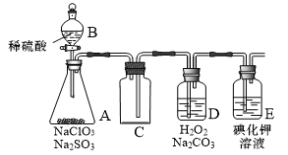
(1)仪器A的名称是______。
(2)图中装置有一明显错误,请指出:______。
(3)打开B的活塞,A中有ClO2生成,D中吸收ClO2后生成NaClO2和NaHCO3,写出D中所发生反应的离子方程式:______。
(4)E中溶液出现黄色能否说明ClO2未被H2O2和Na2CO3的混合溶液充分吸收,判断并说明理由:______。
(5)写出一种提高ClO2吸收率的方法:______。
(6)E装置吸收逸出的少量ClO2气体后所得溶液(pH为5.5~6.5)中存在少量ClO2—,当pH≤2.0时,ClO2—能被I—还原。请补充完整检验E装置溶液中存在少量ClO2—的实验方案:取一定体积E装置中的溶液于分液漏斗中,______,则溶液中存在ClO2—。(实验中须使用的试剂有:CCl4、稀硫酸、淀粉溶液)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向10 mL0.1 mol·L-1NH4Al(SO4)2溶液中,滴加等浓度Ba(OH)2溶液x mL。下列叙述正确的是
A. x=10时, 溶液中有NH4+、AlO2-、SO42-, 且c(NH4+)>c(SO42-)
B. x=10时, 溶液中有NH4+、Al3+、SO42-, 且c(NH4+)>c(Al3+)
C. x=30时, 溶液中有Ba2+、AlO2-、OH-, 且c(OH-)<c(AlO2-)
D. x=30时, 溶液中有Ba2+、Al3+、OH-, 且c(OH-)=c(Ba2+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】不属于有机物的特点是( )
A.大多数有机物难溶于水,易溶于有机溶剂
B.有机反应比较复杂,一般反应速率较慢
C.绝大多数有机物受热不易分解,且不易燃烧
D.绝大多数有机物是非电解质,不易导电,熔点较低
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】[化学—选修5:有机化学基础]我国首架国产大飞机C919采用具有自主知识产权的国产芳砜纶纤维,合成芳砜纶纤维的一种单体M的合成路线如下:
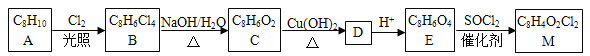
已知:①化合物B的核磁共振氢谱有2组峰
②一个碳原子上连两个羟基不稳定,会自动脱水,即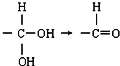
③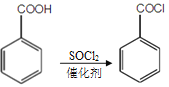
(1)A为芳香烃,请写出A的结构简式____________。
(2)B、C中所含官能团的名称分别为______________、____________。
(3)写出C与新制Cu(OH)2悬浊液反应生成D的化学方程式____________。
(4)E的化学名称为_____________,由E生成M的反应类型为____________。请写出E生成M的化学方程式____________。
(5)工业上用E与乙二醇反应来制涤纶,若涤纶的平均相对分子质量为10000,则其平均聚合度约为____________。
(6)B的同分异构体中能同时满足下列条件的共有_______种(不含立体异构)。
①属于芳香族化合物 ②Cl-不与苯环直接相连
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二氧化铈(CeO2)是一种重要的稀土氧化物。平板电脑显示屏生产过程中有大量的废玻璃粉末(含SiO2、Fe2O3、CeO2以及其他少量可溶于稀酸的物质)产生。某课题组以此粉末为原料回收铈,设计实验流程如下:
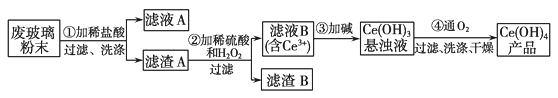
(1)滤渣A的主要成分是_____________;洗涤滤渣A除去的阳离子主要是________(填离子符号),检验该离子是否洗净的操作是________________________;
(2)步骤②中反应的离子方程式是_____________________;
(3)萃取是分离稀土元素的常用方法。已知化合物TBP作为萃取剂能将铈离子从水溶液中萃取出来,TBP________(填“能”或“不能”)与水互溶。实验室进行萃取操作时用到的主要玻璃仪器有________、烧杯、玻璃棒、量筒等;
(4)步骤④中反应化学方程式为______________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为了除去KC1固体中少量MgSO4和CaCl2杂质,需进行下列六项操作: ①加水溶解;②加热蒸发得到晶体;③加入过量BaCl2溶液;④加入过量盐酸;⑤加入过量K2CO3溶液;⑥过滤; 正确的顺序是
A. ①⑤③⑥④② B. ①⑤③④⑥② C. ①③④⑥⑤② D. ①③⑤⑥④②
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】环之间共用一个碳原子的化合物称为螺环化合物,螺[2,2]戊烷(![]() )是最简单的一种。下列关于该化合物的说法错误的是
)是最简单的一种。下列关于该化合物的说法错误的是
A. 与环戊烯互为同分异构体
B. 二氯代物超过两种
C. 所有碳原子均处同一平面
D. 生成1 molC5H12至少需要2 molH2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com