
【题目】反应Fe(s)+CO2(g)FeO(s)+CO(g),700℃时平衡常数为1.47,900℃时平衡常数为2.15.下列说法正确的是( )
A.升高温度该反应的正反应速率增大,逆反应速率减小
B.该反应的化学平衡常数表达式为K= ![]()
C.该反应的正反应是吸热反应
D.增大CO2浓度,平衡常数增大
【答案】C
【解析】解:A.升温,正、逆反应速率均增大,故A错误;B.固体浓度视为常数,不列入平衡常数的表达式,故该化学平衡常数表达式为 ![]() ,故B错误;
,故B错误;
C.升温,平衡常数增大,表明平衡向正反应方向移动,即正反应为吸热反应,故C正确;
D.平衡常数只与温度有关,与浓度无关;故增大反应物浓度,平衡常数不变,故D错误.
故选C.
【考点精析】解答此题的关键在于理解化学平衡状态本质及特征的相关知识,掌握化学平衡状态的特征:“等”即 V正=V逆>0;“动”即是动态平衡,平衡时反应仍在进行;“定”即反应混合物中各组分百分含量不变;“变”即条件改变,平衡被打破,并在新的条件下建立新的化学平衡;与途径无关,外界条件不变,可逆反应无论是从正反应开始,还是从逆反应开始,都可建立同一平衡状态(等效).


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A.氧化还原反应的实质是电子的转移
B.置换反应不一定是氧化还原反应
C.氧化剂发生氧化反应
D.有单质参加或者生成的反应一定属于氧化还原反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】六种短周期元素a、b、c、d、e、f其原子序数与其最高正价或最低负价的关系如下图所示。

(1)上述六种元素,其中属于金属元素的有________种。
(2)元素f在周期表中的位置是____________。
(3)由a、b、c三种元素组成既含离子键又含共价键的化合物,该化合物的化学式为________,该化合物的水溶液显_________性,该化合物在水中的电离方程式为____________。
(4)b元素的气态氢化物与f元素的气态氢化物熔沸点高低顺序为_________(用氢化物的化学式表示)。
(5)a与b、c两元素分别可形成18电子的分子M和N,其中M的电子式为_______。化合物M是一种环保的液体燃料,常温下8g液态M与足量的液态N反应可放出204.5kJ的热量,则该反应的热化学反应方程式为___________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列热化学方程式表达正确的是(![]() 的绝对值均正确)
的绝对值均正确)
A. C2H5OH(1)+3O2(g)=2CO2(g)+3H2O(g) △H=–1367.0 kJ/mol(燃烧热)
B. NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(1) △H= +57.3kJ/mol(中和热)
C. S(s)+O2(g)=SO2(g) △H=–269.8kJ/mol (反应热)
D. 2NO2=O2+2NO △H= +116.2kJ/mol (反应热)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2A(g)+B(g)3C(g)+4D(g)的反应,在不同条件下的反应的速率最快的是( )
A.v(A)=0.7molL﹣1min﹣1
B.v (B)=0.3molL﹣1min﹣1
C.v (C)=0.9molL﹣1min﹣1
D.v (D)=0.8molL﹣1s﹣1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有Al、C12、Al2O3、HCl(aq)、Al(OH)3、NaOH(aq)六种物质,它们之间有如图所示转化关系,图中每条线两端的物质之间都可以发生反应,下列推断不合理的是( )
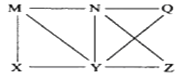
A. N一定是HCl(aq) B. X可能为Al或C12
C. Y一定为NaOH(aq) D. Q、Z中的一种必定为Al2O3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫酸亚铁铵(NH4)aFeb(SO4)cdH2O又称莫尔盐,是浅绿色晶体。用硫铁矿(主要含FeS2、SiO2等)制备莫尔盐的流程如下:

已知:“还原”时,FeS2与H2SO4不反应,Fe3+通过反应Ⅰ、Ⅱ被还原,反应Ⅰ如下:FeS2 + 14Fe3+ + 8H2O =15Fe2+ + 2SO42— + 16H+
(1)写出“还原”时Fe3+与FeS2发生还原反应Ⅱ的离子方程式:______。实验室检验“还原”已完全的方法是_______________。
(2) “还原”前后溶液中部分离子的浓度见下表(溶液体积变化忽略不计):
离子 | 离子浓度(mol·L-1) | |
还原前 | 还原后 | |
SO42- | 3.20 | 3.40 |
Fe2+ | 0.05 | 2.15 |
请计算反应Ⅰ、Ⅱ中被还原的Fe3+的物质的量之比______。
(3)称取11.76g新制莫尔盐,溶于水配成250mL溶液。取25.00 mL该溶液加入足量的BaCl2溶液,得到白色沉淀1.398 g;另取25.00 mL该溶液用0.0200 mol/L KMnO4酸性溶液滴定,当MnO4-恰好完全被还原为Mn2+时,消耗溶液的体积为30.00mL。试确定莫尔盐的化学式_________________(请写出计算过程)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com