
【题目】某工厂在山坡坑道的仓库里贮有氯气钢瓶。某天,有一只贮有氯气的钢瓶损坏,造成氯气泄漏。
(1)处理钢瓶的方法正确的是________。
A.钢瓶推到坡下的小河里
B.把钢瓶丢到深坑里,用石灰填埋
C.把钢瓶扔到农田中
(2)钢瓶处理后,工人应立即________。
A.转移到坡下 B.转移到坡上
科目:高中化学 来源: 题型:
【题目】图为周期表的一部分,已知A,B,C,D,E五种元素原子核外共有85个电子,E原子核外有四个电子层,B元素是( )
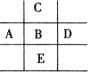
A. PB. MgC. ClD. S
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二氯化二硫(S2Cl2)在工业上用于橡胶的硫化。为在实验室合成S2Cl2,某化学研究性学习小组查阅了有关资料,得到如下信息:
①将干燥纯净的氯气在110℃~140℃与硫反应,即可得S2Cl2粗品。
②有关物质的部分性质如下表:
物质 | 熔点/℃ | 沸点/℃ | 化学性质 |
S | 112.8 | 444.6 | 略 |
S2Cl2 | -77 | 137 | 与过量氯气发生S2Cl2+Cl2 |
设计实验装置图如下:

(1)仪器A的名称是______________。
B中反应的离子方程式为_________________________________。
(2) S2Cl2遇水会生成黄色单质、一种能使品红溶液褪色的气体化合物及酸雾,D中的试剂应是________,写出该反应的化学方程式__________________ 。
(3)装置H的作用是_______________ ,其中发生反应的化学方程式为 ______________________。
(4)S2Cl2粗品中可能混有的杂质是SCl2、Cl2、S,为了提高S2Cl2的纯度,关键的操作是控制好温度和_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某抗癌新药H的一种合成路线如下:
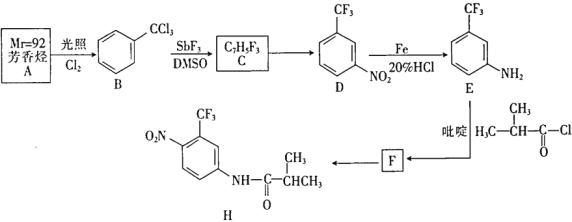
回答下列问题:
(1)A的名称是____________。
(2)B→C的反应类型是__________________。
(3)吡啶的结构简式为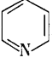 具有碱性,在E→F中吡啶的作用是_________________。
具有碱性,在E→F中吡啶的作用是_________________。
(4)写出E→F的化学方程式_____________。
(5)T(C7H7NO2)是E在碱性条件下的水解产物,同时符合下列条件的T的同分异构体有______种。
①-NH2直接连在苯环上;②能与新制氢氧化铜悬浊液共热产生红色固体
其中,在核磁共振氢谱上有4个峰且峰的面积比为1:2:2:2的结构简式为_________________。
(6)以CH3CH2COCl和![]() 为原料,经三步合成某化工产品(
为原料,经三步合成某化工产品(![]() )路线为(无机试剂任选):___________________。
)路线为(无机试剂任选):___________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在a L Al2(SO4)3和(NH4)2SO4的混合溶液中加入b mol BaCl2,恰好使溶液中的SO42-完全沉淀;如加入足量强碱并加热可得到c mol NH3,则原溶液中Al3+的浓度(mol/L)为
A. ![]() B.
B. ![]() C.
C. ![]() D.
D. ![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质的制备能够成功的是
A. 电解饱和食盐水制备金属钠 B. MnO2和稀盐酸反应制备氯气
C. 铁和盐酸反应制备氯化铁 D. 石灰乳和氯气制备漂白粉
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值,下列说法正确的是
A. 标准状况下,22.4L乙烷中所含的极性共价键数目为NA
B. 500C、101KPa时3.2gSO2和足量的O2充分反应后生成SO3的数目为0.05NA
C. 100mL12mol/L的浓硝酸与过量铜反应,转移的电子数介于0.6NA~0.9NA之间
D. 1L0.1mol/LNH4Cl溶液中,NH4+的数量为0.1NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在进行中和热的测定时,下列操作错误的是( )
A.反应前酸、碱溶液的温度要相同
B.为了使反应均匀进行,可向酸(碱)中分次加入碱(酸)
C.测量溶液的温度计要一直插在溶液中
D.为了使反应更完全,可以使酸或碱适当过量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(化学一选修3:物质结构与性质)1735年瑞典化学家布兰特(G·Brands)制出金属钴。钴的矿物或钴的化合物一直用作陶瓷、玻璃、珐琅的釉料。到20世纪,钴及其合金在电机、机械、化工、航空和航天等工业部门得到广泛的应用,并成为一种重要的战略金属。所以钴及其化合物具有重要作用,回答下列问题:
(1)基态Co原子的电子排布式为___________。
(2)[Co(NH3)5H2O]Cl3是一种砖红色的晶体,可通过CoCl2、NH4Cl、浓氨水、H2O2制得。
①Co、N、0原子的第一电离能由大到小的顺序是__________。
②[Co(NH3)5H2O]Cl3中Co元素化合价为____,其配位原子为_____;1mol该晶体中含有____molσ键。
③H2O2中O原子的杂化轨道类型是______,H2O2能与水互溶,除都是极性分子外,还因为____。
④NH3、NF3的空间构型都相同,但Co3+易与NH3形成配离子,而NF3不能。原因是________。
(3)CoO晶胞如图,已知Co原子半径为apm,O原子半径为bpm,则等距最近的所有O原子围成的空间形状为_____;该晶胞中原子的空间利用率为__________(用含a、b的计算式表示)。
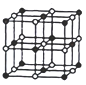
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com