
����Ŀ�����Ȼ�����(S2Cl2)�ڹ�ҵ����������Ϊ��ʵ���Һϳ�S2Cl2��ij��ѧ�о���ѧϰС��������й����ϣ��õ�������Ϣ��
�ٽ����﴿����������110�桫140������Ӧ�����ɵ�S2Cl2��Ʒ��
���й����ʵIJ����������±���
���� | �۵�/�� | �е�/�� | ��ѧ���� |
S | 112.8 | 444.6 | �� |
S2Cl2 | ��77 | 137 | �������������S2Cl2��Cl2 |
���ʵ��װ��ͼ���£�

(1)����A��������______________��
B�з�Ӧ�����ӷ���ʽΪ_________________________________��
(2) S2Cl2��ˮ�����ɻ�ɫ���ʡ�һ����ʹƷ����Һ��ɫ�����廯���P������D�е��Լ�Ӧ��________��д���÷�Ӧ�Ļ�ѧ����ʽ__________________ ��
(3)װ��H��������_______________ �����з�����Ӧ�Ļ�ѧ����ʽΪ ______________________��
(4)S2Cl2��Ʒ�п��ܻ��е�������SCl2��Cl2��S,Ϊ�����S2Cl2�Ĵ��ȣ��ؼ��IJ����ǿ��ƺ��¶Ⱥ�_______��
���𰸡���Һ©�� MnO2��4H����2Cl��![]() Mn2����Cl2����2H2O Ũ���� 2 S2Cl2+2H2O=4HCl+SO2��+3S�� ����β������ֹ��Ⱦ���� Cl2+2NaOH=NaCl+NaClO+H2O �μ�Ũ������ٶȲ�Ҫ����
Mn2����Cl2����2H2O Ũ���� 2 S2Cl2+2H2O=4HCl+SO2��+3S�� ����β������ֹ��Ⱦ���� Cl2+2NaOH=NaCl+NaClO+H2O �μ�Ũ������ٶȲ�Ҫ����
��������
(1)��װ��ͼ��֪B�з�Ӧ���ù�Һ���ȵķ�����Cl2������Ũ����Ͷ������̷�Ӧ��ȡ��(2)������ȡ�����еij������⣬���ñ���ʳ��ˮ��ȥ�����е�HCl������Ũ������и��T�ɵô��������������S2Cl2����ˮ��Ӧ��(3)�������ж����壬����Ⱦ������(4) ����Ϣ��֪�������¶ȡ�ˮ�������������������ػ���ɲ�Ʒ���������ʣ��ݴ˷������
(1)����������״��֪AΪ��Һ©�����ù�Һ���ȵķ�����Cl2������Ũ����Ͷ������̷�Ӧ��ȡ����Ӧ�����ӷ���ʽΪMnO2+4H++2Cl- ![]() Mn2++Cl2��+2H2O���ʴ�Ϊ����Һ©����MnO2+4H++2Cl-
Mn2++Cl2��+2H2O���ʴ�Ϊ����Һ©����MnO2+4H++2Cl- ![]() Mn2++Cl2��+2H2O��
Mn2++Cl2��+2H2O��
(2) ������ȡ�����еIJ�������HCl��H2O��������ñ���ʳ��ˮ��ȥ�����е�HCl������Ũ������и��T�ɵô������������������C��Ϊ����ʳ��ˮ��D��ΪŨ���S2Cl2��ˮ�����ɻ�ɫ������һ����ʹƷ����Һ��ɫ�����廯����Ϊ������������(HCl)����Ӧ�Ļ�ѧ����ʽΪ��2S2Cl2+2H2O=3S��+SO2��+4HCl���ʴ�Ϊ��Ũ���2S2Cl2+2H2O=3S��+SO2��+4HCl��
(3) ��Ӧ�������漰�ж��к����壬������β������Ⱦ���������װ��H�е�����������Һ��������δ��Ӧ������(��������)����ֹ��Ⱦ��������Ӧ�Ļ�ѧ����ʽΪCl2+2NaOH=NaCl+NaClO+H2O���ʴ�Ϊ������β������ֹ��Ⱦ������Cl2+2NaOH=NaCl+NaClO+H2O��
(4) ����Ϣ��֪���������¶ȡ�ˮ������������SCl2��Cl2��S�����ʣ�Ϊ�����S2Cl2�Ĵ��ȣ��ؼ��IJ����ǿ��ƺ��¶ȣ�����S2Cl2�ֽ�Ϊ������������μ�������죬��ɷ�Ӧ�������������������¸���ӦS2Cl2��Cl2![]() 2SCl2�ķ�������˻�Ӧ����Ũ����ĵ��ٲ�Ҫ���죬�ʴ�Ϊ������Ũ����ĵ��ٲ�Ҫ���졣
2SCl2�ķ�������˻�Ӧ����Ũ����ĵ��ٲ�Ҫ���죬�ʴ�Ϊ������Ũ����ĵ��ٲ�Ҫ���졣


 ��Ǭ����������ҵ���ּ����ӱ����������ϵ�д�
��Ǭ����������ҵ���ּ����ӱ����������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���л���A�Ľṹ��ʽΪ��![]()
��1��A�ķ���ʽΪ_____��
��2��A��NaOHˮ��Һ�м��ȣ����ữ�õ��л���B��D��D�Ƿ����廯�������1mol A������Ӧʱ���������_____mol NaOH��
��3��B��һ�������·���������Ӧ������ij��Ԫ����������Ԫ�����Ľṹ��ʽΪ_____��
��4��д��������ֻ��һ��ȡ���������������D������ͬ���칹�壮_____��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪:�����¼װ���CH3NH2���ĵ��볣��kb��pkb=-lgkb=3.4��CH3NH2+H2O![]() CH3NH3++OH-������˵������ȷ���ǣ� ��
CH3NH3++OH-������˵������ȷ���ǣ� ��
A. (CH3NH3)2SO4��Һ������Ũ��:c(CH3NH3+)>c(SO42-)>c(H+)>c(OH-)
B. �����£�pH=3��������Һ��pH=11��CH3NH2��Һ�������ϣ������Һ������
C. �ñ�Ũ�ȵ�����ζ�δ֪Ũ�ȵ�CH3NH2��Һ��ʵ���У�ѡ�������ָʾ��
D. ��������CH3NH2��Һ�μ�ϡ������c(CH3NH2)=c(CH3NH3+)ʱ����ҺpH=10.6
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪:pNi=-lgc(Ni2+)�������£�K(NiCO3)=1.4��10-7��H2S�ĵ���ƽ�ⳣ����Ka1=1.3��10-7��Ka2=7.1��10-15�������£���10mL0.1mol��L-1Ni(NO3)2��Һ�еμ�0.1mol��L-1Na2S��Һ���μӹ�����pNi��Na2S��Һ����Ĺ�ϵ��ͼ��ʾ������˵������ȷ���ǣ� ����
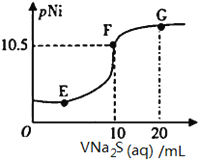
A. E��F��G�����У�F���Ӧ��Һ��ˮ����̶���С
B. �����£�Ksp(NiS)=1��10-21
C. ��NiS��NiCO3����Һ��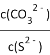 =1.4��1014
=1.4��1014
D. Na2S��Һ�У�S2-��һ��ˮ�ⳣ��Kh1=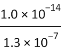
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��LED(Light EmittingDiode)����������ܣ���һ���ܹ�������ת��Ϊ���ܵĹ�̬�뵼����������ͼ��ij����С����Ƶ��û�ѧ��ԴʹLED�Ʒ����װ�á�����˵������ȷ���ǣ� ��

A. ��Һ��SO42-��ͭƬ�����ƶ�
B. ͭƬ�Ϸ����ķ�ӦΪ2H++2e-=H2��
C. �����е�����пƬ����ͭƬ
D. �����пƬ������Ƭ�����·�еĵ�������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ����������ijŨ��Fe2+ΪFe3+���̵�ʵ�����������й�˵����ȷ����
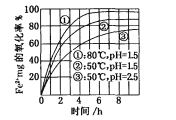
A. pH=1.5ʱ������һ����pH=2.5ʱ��
B. ����������ͬʱ��80��������ʱ�50���
C. Fe2+�������ʽ�����Һ��pH���¶��й�
D. ���������̵����ӷ���ʽΪ��Fe2++O2+4H+=Fe3++2H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��(1)ʪ���Ƹ��������(K2FeO4)�ķ�Ӧ��ϵ�����������ӣ�Fe(OH)3��ClO����OH����FeO42����Cl����H2O��
��д������ƽʪ���Ƹ�����ط�Ӧ�����ӷ���ʽ��______________________________
��ÿ����l mol FeO42-ת��__________mol���ӣ�����Ӧ������ת����0.3 mol���ӣ���ԭ��������ʵ���Ϊ____mol��
�۵����£��ڸ���������Һ�м���KOH�����Ϳ������������(K2FeO4)ԭ����__��
(2)��ҵ�ϴӺ�ˮ����ȡ������ɲ������·�����
����ˮ��ͨ��Cl2����ˮ���廯�������������ӷ���ʽΪ____��
�����������Һ�д����ȿ����������ɵ��崵�����ô�����Һ���գ��仯ѧ����ʽΪ__��
�۽���������Һ��H2SO4�ữ��ʹNaBr��NaBrO3�е���ת��Ϊ�����壬�����л��ܼ���ȡ����ɵõ�����ƷNa2SO4����һ���̿��û�ѧ����ʽ��ʾΪ____��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij������ɽ�¿ӵ��IJֿ�������������ƿ��ij�죬��һֻ���������ĸ�ƿ���������й©��
��1��������ƿ�ķ�����ȷ����________��
A����ƿ�Ƶ����µ�С����
B���Ѹ�ƿ����������ʯ������
C���Ѹ�ƿ�ӵ�ũ����
��2����ƿ��������Ӧ����________��
A��ת�Ƶ����� B��ת�Ƶ�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪��2SO2 (g)+ O2(g) ![]() 2SO3(g) ��H���й��������£�
2SO3(g) ��H���й��������£�
T������ | 527 | 627 | 727 | 827 | 927 |
ƽ�ⳣ��K | 910 | 42 | 3.2 | 0.39 | 0.12 |
����˵������ȷ����
A. ����ƽ�ⳣ�����¶ȵı仯��ϵ���жϳ���H��0
B. ���������������䣬SO2��ƽ��ת������(727��)����(927��)
C. ����ѹǿ�������¶������SO2��ת����
D. SO3���ȶ������¶ȵ����߶�����
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com