
【题目】有机物A的结构简式为:![]()
(1)A的分子式为_____.
(2)A在NaOH水溶液中加热,经酸化得到有机物B和D,D是芳香族化合物.当有1mol A发生反应时,最多消耗_____mol NaOH.
(3)B在一定条件下发生酯化反应可生成某五元环酯,该五元环酯的结构简式为_____.
(4)写出苯环上只有一个取代基且属于酯类的D的所有同分异构体._____.
科目:高中化学 来源: 题型:
【题目】微型纽扣电池在现代生活中有广泛应用。有一种银锌电池,其电极材料分别是Ag2O和Zn,电解质溶液为KOH溶液,电极反应式为Zn+2OH2e===Zn(OH)2,Ag2O+H2O+2e===2Ag+2OH。下列叙述中正确的是( )
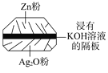
A. 在使用过程中,电解质KOH不断被消耗
B. 使用过程中,电子由Ag2O极经外电路流向Zn极
C. Zn电极发生还原反应,Ag2O电极发生氧化反应
D. Zn是负极,Ag2O是正极
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组离子在溶液中能大量共存的是( )
A.Cu2+、K+、SO42-、NO3-B.Na+、H+、Cl-、HCO3-
C.Na+、NH4+、OH-、Cl-D.H+、K+、SO42-、CO32-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在反应3S+6KOH=K2SO3+2K2S+3H2O中,被还原与被氧化的硫原子数之比为
A. 1:2 B. 2:1 C. 1:1 D. 3:2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某有机物A是农药生产中的一种中间体,其结构简式如图所示,下列叙述正确的是( )
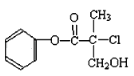
A. 有机物A属于芳香烃
B. 有机物A可以和Br2的CCl4溶液发生加成反应
C. 有机物A和浓硫酸混合加热,可以发生消去反应
D. 1molA和足量的NaOH溶液反应,可以消耗3mol NaOH
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示是用石墨和铁作电极电解饱和食盐水的装置,请填空:
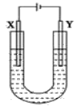
(1)X的电极名称是________极,发生的电极反应式为:_______________________。Y极的电极材料是__________,检验X极产物的方法是___________________________________________。
(2)写出该电极总反应的离子方程式:___________________________________。
(3)若食盐水为100mL 两极共放出2.24L气体(标准状况),则电路中通过电子的物质的量为___________。(假定电解后仍为100mL)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某校的化学兴趣小组利用下列实验装置探究二氧化硫的性质,E中装有常见气体,与E装置相连的玻璃导管可根据需要变换长短。
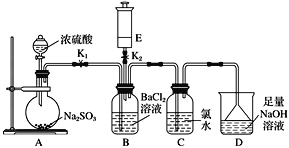
实验开始时关闭K2打开K1,从分液漏斗中向烧瓶内加入浓硫酸。
(1)A中发生反应的化学方程式是:________________________________________,B中的现象是_____________________________________。
(2)C中的现象是______________写出C中反应的化学方程式:___________________________________。
(3)D的作用是________________________,反应的离子方程式为__________________________________。
(4)A中反应完成后,关闭K1,打开K2,将E中的无色气体缓缓注入B中,有白色沉淀产生:
①若E是无色有刺激性气味气体,它的分子式为________,产生的白色沉淀是_______________(填化学式)
②若E是无色无味气体,它的分子式为________, 产生的白色沉淀是_______________(填化学式)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】图为周期表的一部分,已知A,B,C,D,E五种元素原子核外共有85个电子,E原子核外有四个电子层,B元素是( )
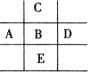
A. PB. MgC. ClD. S
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二氯化二硫(S2Cl2)在工业上用于橡胶的硫化。为在实验室合成S2Cl2,某化学研究性学习小组查阅了有关资料,得到如下信息:
①将干燥纯净的氯气在110℃~140℃与硫反应,即可得S2Cl2粗品。
②有关物质的部分性质如下表:
物质 | 熔点/℃ | 沸点/℃ | 化学性质 |
S | 112.8 | 444.6 | 略 |
S2Cl2 | -77 | 137 | 与过量氯气发生S2Cl2+Cl2 |
设计实验装置图如下:

(1)仪器A的名称是______________。
B中反应的离子方程式为_________________________________。
(2) S2Cl2遇水会生成黄色单质、一种能使品红溶液褪色的气体化合物及酸雾,D中的试剂应是________,写出该反应的化学方程式__________________ 。
(3)装置H的作用是_______________ ,其中发生反应的化学方程式为 ______________________。
(4)S2Cl2粗品中可能混有的杂质是SCl2、Cl2、S,为了提高S2Cl2的纯度,关键的操作是控制好温度和_______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com