
【题目】下列无色透明溶液,能大量共存的是( )
A. K+、Na+、Ba2+、OH— B. Cl—、MnO4—、K+、Na+
C. Ag+、K+、Cl—、NO3— D. H+、NO3—、CO32—、Fe2+
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】(1)微粒1123Na+中质子数是 ,中子数是 ,核外电子数是 .
(2)下列3种不同粒子 11H、12H、13H表示 种元素, 种核素,11H、12H、13H互称为 , 它们的化学性质 . (填“相似”或“不同”)
(3)1124Mg表示Mg原子核外电子所占据的电子层中,能量最高的是 层(填符号).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有一种活跃在中学化学题中的物质叫氢化铵(NH5),有人认为它的结构与氯化铵相似,所有的原子最外层都符合相应稀有气体原子的最外层电子层结构。与水反应有气体生成事实上,目前为止尚未有人能够成功制取氢化铵,所以此物质是否存在仍有争议,但想法还是要有的,万一发现了呢?假设它真的存在,上述观点也正确,则下列有关说法正确的是
A. NH5中N元素的化合价是+5价
B. 1mol NH5中含有5NA个N-H键
C. NH5的电子式为![]()
D. NH5只由两种非金属元素组成,所以它是共价化合物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“忽闻海上有仙山,山在虚无缥缈间。”海市蜃楼是一种自然现象,发生这种现象的本质原因是( )
A. 人产生的视幻觉,无法解释
B. 空气中的小液滴颗粒直径为100纳米以上
C. 此时空气是胶体,产生了丁达尔效应
D. 光本身是一种胶体,在空气中被反射到了观察者的眼内
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】磷化铝、磷化锌、磷化钙是我国目前最常见的熏蒸杀虫剂,都能与水或酸反应产生有毒气体膦(PH3)PH3具有较强的还原性,能在空气中自燃.我国粮食卫生标准规定,粮食中磷化物(以PH3计)含量≤0.05mg/kg. 某化学兴趣小组的同学通过下列方法对粮食中残留磷化物含量进行研究:
【实验课题】
【实验原理】
5PH3+8KMnO4+12H2SO4=5H3PO4+8MnSO4+4K2SO4+12H2O
2KMnO4+5Na2SO3+3H2SO4=2MnSO4+K2SO4+5Na2SO4+3H2O
【操作流程】
安装蒸馏吸收装置→PH3的产生与吸收→转移褪色→亚硫酸钠标准溶液滴定
【实验装置】
A、D、E、F各装1.00mL浓度为5.00×10﹣4 mol/L的酸性KMnO4溶液,B中装碱性焦性没食子酸(1,2,3﹣三羟基苯),C中装200g原粮.
(1)实验课题的名称是 .
(2)以磷化铝为例,写出磷化物与水反应的化学方程式 .
(3)检查上述装置气密性的方法是 .
(4)A中盛装KMnO4溶液是为除去空气中可能含有的(填“氧化性”、“还原性”) 气体;B中盛装碱性焦性没食子酸溶液的作用是;如去除B装置,则实验中测得的PH3含量将(填偏大、偏小或不变).
(5)将D、E、F三装置中的吸收液、洗涤液一并置于锥形瓶中,加水稀释至25mL,用浓度为2.5×10﹣4 mol/LNa2SO3标准溶液滴定剩余的KMnO4溶液,消耗Na2SO3标准溶液11.00mL,则该原粮中磷化物(以PH3计)的含量为mg/kg.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用如图装置制取、提纯并收集下表中的四种气体(a、b、c、d表示相应仪器中加入的试剂,收集装置略去).其中可行的是( )
气体 | a | b | c | d | |
A | CO2 | 稀硫酸 | 石灰石 | 饱和Na2CO3溶液 | 浓H2SO4 |
B | Cl2 | 浓盐酸 | KMnO4固体 | 饱和NaCl溶液 | 浓H2SO4 |
C | NH3 | 饱和NH4Cl溶液 | 消石灰 | H2O | 碱石灰 |
D | H2 | 硝酸 | 锌粒 | H2O | P2O5 |

A.A
B.B
C.C
D.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】图1是元素周期表的一部分,A、B、C、D、E、X 是元素周期表给出元素组成的常见单质或化合物.已知 A、B、C、D、E、X 存在如图2所示转化关系(部分生成物和反应条件略去). 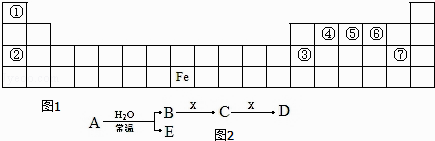
(1)若 E 为氧化物,则 A 与水反应的方程式为 , 该反应中氧化剂和还原剂物的量之比为 . ①当 X 为碱性盐溶液,C分子中有 22 个电子时,D 是(写化学式).
②当 X 为金属单质时,X 与足量 B 的稀溶液反应生成 C 的离子方程式为 , 写出检验生成物 C 的阳离子所用试剂的电子式 .
(2)若 E 为单质气体,D 为白色沉淀,A 可能是(写化学式),X是(写化学式).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ti、Fe、Cr、Mn等均为过渡元素,在生产生活中起着不可替代的重要作用,对其单质和化合物的应用研究是目前科学研究的前沿之一.请回答下列问题: 
(1)Cr元素的基态原子电子排布式为 , 比较Fe和 Mn的各级电离能后发现,气态Mn2+再失去一个电子比气态Fe2+再失去一个电子(填“难”或“易”).
(2)Cu元素处于周期表区,向盛有硫酸铜的试管里加入氨水,首先形成蓝色沉淀,继续加入氨水,沉淀溶解,此时的离子方程式为 , 若加入乙醇将析出色的晶体,其配离子的离子构型为
(3)某钙钛型复合氧化物(如图1),以A原子为晶胞的顶点,A位可以是Ca、Sr、Ba或Pb,当B位是V、Cr、Mn、Fe时,这种化合物具有CMR效应(巨磁电阻效应).用A、B、O表示这类特殊晶体的化学式: .
(4)有一种蓝色晶体可表示为:[KxFey(CN)z],研究表明它的结构特性是Fe2+、Fe3+分别占据立方体的顶点,自身互不相邻,而CN﹣位于立方体的棱上,K+位于上述晶胞体心,且K+空缺率为50%(体心中没有K+的占总体心的百分比),其晶体中的阴离子晶胞结构如图2所示,该晶体的化学式可表示为 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com