
【题目】下列说法正确的是( )
A. 1个丙烯分子中有6个![]() 键,1个
键,1个![]() 键
键
B. 在晶体中,1个Si原子和2个O原子形成2个共价键![]()
C. 12g石墨中含有的C-C键数目为2NA
D. 124gP4分子中含有P-P键的数目为6NA
 星级口算天天练系列答案
星级口算天天练系列答案 芒果教辅达标测试卷系列答案
芒果教辅达标测试卷系列答案科目:高中化学 来源: 题型:
【题目】LED系列产品是一类新型节能产品。图甲是NaBH4/H2O2燃料电池,图乙是LED发光二极管的装置示意图。下列叙述错误的是

A.电池A极区的电极反应式为:H2O2+2e-=2OH-
B.电池放电过程中,Na+从负极区向正极区移动
C.每有1mol NaBH4参加反应转移电子数为4NA
D.要使LED发光二极管正常发光,图乙中的导线a应与图甲中的B极相连
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】300mL Al2(SO4)3溶液中,含Al3+为1.62g,在该溶液中加入0.1mol·L-1Ba(OH)2溶液300mL,反应后溶液中SO42﹣的物质的量浓度为( )
A. 0.4mol·L-1 B. 0.3mol·L-1 C. 0.2mol·L-1 D. 0.1mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】胶体是一种常见的分散系,回答下列问题。
(1)向大量沸腾的蒸馏水中逐滴加入___________溶液,继续煮沸至________________________________,停止加热,可制得Fe(OH)3胶体;
(2)向Fe(OH)3胶体中滴加氢碘酸(HI水溶液)至过量,观察到的现象为________________________________________,该反应的离子方程式为________________________________________________________;
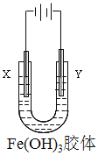
(3)如由图所示,通电后,Fe(OH)3胶体粒子向_________电极移动(填“X”或“Y”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学用密度为1.84g/cm3、质量分数为 98%的浓硫酸配制500mL0.22 mol/L的稀硫酸。
(1)操作过程中使用到的玻璃仪器有_____________________________________________________;
(2)实验过程中涉及的操作如下:
①将容量瓶中的溶液倒入试剂瓶中并贴上标签;
②将浓硫酸沿烧杯内壁缓慢注入盛有约160mL蒸馏水的烧杯中并小心搅拌;
③用规格为 的量筒量取 mL的浓硫酸;
④将已冷却的硫酸溶液转移到容量瓶中,并用少量蒸馏水洗涤烧杯和玻璃棒2~3次,洗涤液全部转移到容量瓶中,轻轻摇动容量瓶,使溶液混合均匀;
⑤改用胶头滴管滴加蒸馏水,使溶液凹液面最低处恰好与刻度线相切;
⑥塞好玻璃塞,反复颠倒摇匀;
⑦继续向容量瓶中加蒸馏水直到距离刻度线 处;
将步骤③、⑦补充完整:_____________,_____________,_______________;
实验操作顺序为__________________________________________(填序号)。
(3)配制该溶液的过程中,下列操作使得所配得的溶液浓度偏小的是______________(填字母) 。
A.稀释密度为1.84g/cm3、质量分数为 98%的浓硫酸时,不小心溅出少量硫酸溶液
B.用蒸馏水洗涤烧杯、量筒及玻璃棒,并将洗涤液注入容量瓶中
C.定容时反复上下倒转容量瓶后,发现凹液面最低处低于刻度线,再补加水到刻度线
D.量取密度为1.84g/cm3、质量分数为 98%的浓硫酸时,仰视量筒的刻度线
E.洗涤容量瓶后,立即用来配制溶液
F.稀释浓硫酸结束后立即将溶液转移到容量瓶中
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述表示可逆反应N2 + 3H2 ![]() 2NH3一定处于平衡状态的是
2NH3一定处于平衡状态的是
A. N2、H2、NH3的百分含量相等
B. 单位时间,消耗a mol N2的同时消耗3a mol H2
C. 单位时间,消耗a molN2的同时生成3a mol H2
D. 反应若在定容的密器中进行,温度一定时,压强不随时间改变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组化合物中,不论二者以任何比例混合,只要总质量一定,则完全燃烧时消耗O2的质量和生成水的质量不变的是( )
A、CH4、C2H6 B、C2H6、C3H6 C、C2H4、C3H6 D、C2H4、C3H4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】金属钛(22Ti)、铁(26Fe)及其相关化合物在化工、医药、材料等领域有着广泛的应用。回答下列问题:
(1)基态Ti原子中,最高能层电子的电子云轮廓形状为_____________,与Ti同周期的所有过渡元素的基态原子中,最外层电子数与钛不同的元素有_________种。
(2)琥珀酸亚铁片是用于缺铁性贫血的预防和治疗的常见药物,临床建议服用维生素C促进“亚铁”的吸收,避免生成Fe3+,从结构角度来看,Fe2+易被氧化成Fe3+的原因是_____________。
(3)SCN-离子可用于Fe3+的检验,其对应的酸有两种,分别为硫氰酸(H-S-C![]() N)和异硫氰酸(H-N=C=S)。
N)和异硫氰酸(H-N=C=S)。
①写出与SCN-互为等电子体的一种微粒______________(分子或离子);
②硫氰酸分子中π键和σ键的个数之比为______________;
③异硫氰酸的沸点比硫氰酸沸点高的原因是__________________________________。
(4)TiCl3可用作烯烃定向聚合的催化剂,如:nCH3CH=CH2![]() 。该反应涉及的物质中碳原子的杂化轨道类型有_______________________;反应涉及的元素中电负性最大的是_____________________________。
。该反应涉及的物质中碳原子的杂化轨道类型有_______________________;反应涉及的元素中电负性最大的是_____________________________。
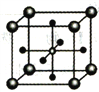
(5)Ti的某氧化物和CaO相互作用能形成钛酸盐的晶胞结构如图所示(Ti4+位于立方体的顶点,Ca2+处于立方体的中心)。该晶体中,Ti4+和周围________个O2-紧邻;若该晶胞的密度为dg/cm3则钛氧键的键长为________cm(用含NA的代数式表示)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com