
【题目】按照要求回答下列问题
(1)硫酸铁溶液显酸性的原因_____(用离子方程式表示).
(2)物质的量浓度相同的醋酸和氢氧化钠溶液混合溶液中c(CH3COO﹣)=c(Na+),则混合后溶液显_____性.
(3)浓度均为0.1mol/L①氯化铵②醋酸铵③硫酸氢铵④氨水四种溶液中,c(NH4+)由大到小的顺序_____(填序号).
(4)将化合物A的蒸气1mol充入0.5L容器中加热分解:2A(g)B(g)+nC(g),反应到3min时,容器内A的浓度为0.8mol/L,测得这段时间内,平均速率ν(C)=0.6mol/(Lmin),则化学方程式中的n值为_____,ν(B)=_____,此时A的分解率为_____.
【答案】Fe3++3H2O ![]() Fe(OH)3+3H+ 中 ③①②④ 3 0.2 mol/(L·min) 60%
Fe(OH)3+3H+ 中 ③①②④ 3 0.2 mol/(L·min) 60%
【解析】
(1)硫酸铁溶液中,Fe3+发生水解,溶液显酸性;
(2)根据电荷守恒进行分析;
(3)从盐类的水解和弱电解质的电离程度微弱进行分析;
(4)根据化学反应速率以及物质的量在反应方程式的应用进行分析;
(1)硫酸铁属于强酸弱碱盐,Fe3+发生水解:Fe3++3H2O ![]() Fe(OH)3+3H+,使溶液中c(H+)>c(OH-),溶液显酸性;
Fe(OH)3+3H+,使溶液中c(H+)>c(OH-),溶液显酸性;
(2)根据电荷守恒,c(Na+)+c(H+)=c(OH-)+c(CH3COO-),因为c(Na+)=c(CH3COO-),因此有c(H+)=c(OH-),溶液显中性;
(3)盐类水解程度和弱电解质的电离程度都是微弱,因此四种溶液中NH3·H2O中的c(NH4+)最小,硫酸氢铵溶液中存在大量H+,抑制NH4+的水解,醋酸铵为弱酸弱碱盐,相互促进水解,盐中c(NH4+)最小,因此c(NH4+)由大到小的顺序是③①②④;
(4)根据化学反应速率的数学表达式,这段时间内生成C的物质的量浓度为0.6mol/(L·min)×3min=1.8mol/L,根据反应方程式,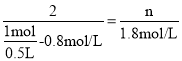 ,解得n=3,根据反应速率之比等于化学计量数之比,因此有v(B)=
,解得n=3,根据反应速率之比等于化学计量数之比,因此有v(B)=![]() v(C)=
v(C)=![]() ×0.6 mol/(L·min)=0.2 mol/(L·min),0-3min消耗A的物质的量为(1mol-0.8mol/L×0.5L)=0.6mol,则A的分解率=
×0.6 mol/(L·min)=0.2 mol/(L·min),0-3min消耗A的物质的量为(1mol-0.8mol/L×0.5L)=0.6mol,则A的分解率=![]() ×100%=60%。
×100%=60%。


科目:高中化学 来源: 题型:
【题目】元素Ni用途广泛,工业上以硫化镍矿(含少量杂质硫化铜、硫化亚铁)为原料制备并精制镍的基本流程如下:
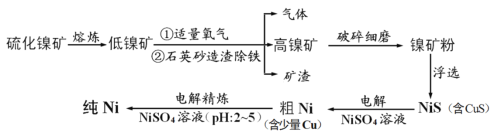
已知:①电极电位(E)能体现微粒的氧化还原能力强弱,如:
H2 -2e-= 2H+ E=0.00V; Cu-2e- =Cu2+ E=0.34V;
Fe -2e-= Fe2+ E=-0.44V; Ni-2e-=Ni2+ E=-0.25V
②常温下溶度积常数 Ksp(NiS)=1.07×10-21; Ksp(CuS)=1.27×10-36
(1)可用光洁的镍丝代替铂丝蘸取化学试剂在焰色反应实验中灼烧,原因是_________。
(2)就制备高镍矿的相关问题请回答:
①通入氧气时控制适量的目的是________________。
②已知矿渣能使酸性高锰酸钾溶液褪色,原因是__________________。
(3)电解制粗镍时阳极发生的主要电极反应式___________________。
(4)电解精炼镍的过程需控制pH为2~5,试分析原因__________________。
(5)工业生产中常用加NiS的方法除去溶液中的Cu2+,若过滤后溶液中c(Ni2+) 为0.107 mol/L,则滤液中残留的c(Cu2+)为________ mol/L。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下,一定体积pH=12的Ba(OH)2溶液中,逐滴加入一定物质的量浓度的Na2SO4溶液,当溶液中的Ba2+恰好完全沉淀时,溶液的pH=11(忽略反应前后的体积变化),则Ba(OH)2溶液与Na2SO4溶液的体积比是( )
A.1:9B.1:1C.1:2D.1:4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:H2(g)+F2(g)=2HF(g);ΔH= -270 kJ/mol,下列说法正确的是( )
A.氟化氢气体分解生成氢气和氟气的反应是放热反应
B.1mol H2与1mol F2反应生成2mol液态HF放出的热量小于270kJ
C.在相同条件下,1mol H2与1mol F2的能量总和大于2mol HF气体的能量
D.该反应中的能量变化可用如图来表示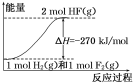
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NH4Al(SO4)2是食品加工中最为快捷的食品添加剂,用于焙烤食品中;NH4HSO4在分析试剂、医药、电子工业中用途广泛。请回答下列问题:
(1)NH4Al(SO4)2可作净水剂,其理由是_______________(用必要的化学用语和相关文字说明)。
(2)相同条件下,0.1 mol/L NH4Al(SO4)2中的c(NH![]() )________(填“等于”“大于”或“小于”)0.1 mol/L NH4HSO4中的c(NH
)________(填“等于”“大于”或“小于”)0.1 mol/L NH4HSO4中的c(NH![]() )。
)。
(3)如图是0.1 mol/L电解质溶液的pH随温度变化的图像。

①其中符合0.1 mol/L NH4Al(SO4)2的pH随温度变化的曲线是________(填写字母),导致pH随温度变化的原因是___________________;
②20℃时,0.1 mol/L NH4Al(SO4)2中2c(SO![]() )-c(NH
)-c(NH![]() )-3c(Al3+)=________。
)-3c(Al3+)=________。
(4)室温时,向100 mL 0.1 mol/L NH4HSO4溶液中滴加0.1 mol/L NaOH溶液,得到溶液pH与NaOH溶液体积的关系曲线如图所示:
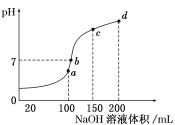
试分析图中a、b、c、d四个点,水的电离程度最大的是________;在b点,溶液中各离子浓度由大到小的排列顺序是_______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】阅读下列实验内容,根据题目要求回答问题。
某学生为测定未知浓度的硫酸溶液,实验如下:用1.00mL待测硫酸配制100mL稀H2SO4溶液;以0.14mol·L-1的NaOH溶液滴定上述稀H2SO4溶液25.00mL,滴定终止时消耗NaOH溶液15.00mL。
(1)该学生用标准0.14mol·L-1 NaOH溶液滴定硫酸的实验操作如下:
A.用酸式滴定管取稀H2SO4 25.00mL,注入锥形瓶中,加入几滴酚酞做指示剂
B.用待测定的溶液润洗酸式滴定管
C.用蒸馏水洗干净滴定管
D.取下碱式滴定管用标准的NaOH溶液润洗后,将标准液注入碱式滴定管,调整液面,记下开始读数
E.检查滴定管是否漏水
F.另取锥形瓶,再重复操作一次
G.把锥形瓶放在滴定管下面,瓶下垫一张白纸,边滴边摇动锥形瓶直至滴定终点,记下滴定管液面所在刻度
滴定操作的正确顺序是(用序号填写)_______________。
(2)在D操作中应该调整液面到_________________,并使尖嘴处_____________。
(3)配制准确浓度的稀H2SO4溶液,必须使用的主要容器是__________________。
(4)滴定到终点时锥形瓶内溶液的pH约为________;终点时颜色变化是____________。
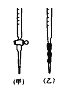
(5)用标准NaOH溶液滴定时,应将标准NaOH溶液注入____(选填“甲”或“乙”)中。
(6)观察碱式滴定管读数时,若滴定前仰视,滴定后俯视,则结果会导致测得的稀H2SO4溶液浓度测定值___________(选填“偏大”“偏小”或“无影响”)。
(7)计算待测硫酸(稀释前的硫酸)溶液的物质的量浓度(计算结果到小数点后二位)____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】咖啡鞣酸具有较广泛的抗菌作用,其结构简式如下图所示:

关于咖啡鞣酸的下列叙述正确的是( )
A.分子式为C16H13O9
B.1 mol咖啡鞣酸可与含8 mol NaOH的溶液反应
C.能使酸性KMnO4溶液褪色,说明分子结构中含有碳碳双键
D.与浓溴水能发生两种类型的反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国科研团队发现苯乙烯与开链醚可实现如下的转化反应,关于该反应,下列说法不正确的是

A.M属于芳香烃
B.N的同分异构中可能有醛类化合物
C.P分子中只含有两种含氧官能团
D.若R1、R2均为甲基,则P的分子式为C12H16O2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】把1 mol X气体和0.5 mol Y气体混合于2 L密闭容器中,发生如下反应:3X(g)+Y(g)![]() nZ(g)+2W(g),2 min末生成0.2 mol W,若测得以Z的物质的量浓度变化表示的平均反应速率为0.1mol/(L·min),试计算:
nZ(g)+2W(g),2 min末生成0.2 mol W,若测得以Z的物质的量浓度变化表示的平均反应速率为0.1mol/(L·min),试计算:
(1)前2 min内,用X表示的平均反应速率________;
(2)2 min末时Y的转化率________;
(3)化学方程式中Z的化学计量数n________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com