
【题目】下列叙述不正确的是 ( )
A. 氢氧化铝可以用于治疗胃酸过多 B. Fe3O4可用作红色油漆和涂料
C. 金属钠有强还原性,能和硫酸铜溶液反应,但不能置换出金属铜 D. 为使面包松软可口可用碳酸氢钠做发泡剂
科目:高中化学 来源: 题型:
【题目】X元素原子的L层比Y元素原子的L层少3个电子,X元素原子的核外电子总数比Y原子核外电子总数少5个,则X、Y可形成的化合物是
A. 离子化合物Y(XO4)2 B. 离子化合物Y2X3
C. 共价化合物XY2 D. 离子化合物Y3X2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】分别处于第二、第三周期的主族元素A和B,它们的离子电子层结构相差两层,已知A处于第m族,B处于第n族,A只有正化合价,则A、B的原子序数分别是( )
A. m、n B. 3、7 C. m-2、10-n D. m+2、n+10
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列哪一个反应表示二氧化硫被还原 ( )
A. SO2+2H2O+Cl2===H2SO4+2HCl B. SO2+2H2S===2H2O+3S
C. SO2+2NaOH===Na2SO3+H2O D. SO2+Na2CO3===Na2SO3+CO2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】姜黄素具有搞突变和预防肿瘤的作用,其合成路线如下:
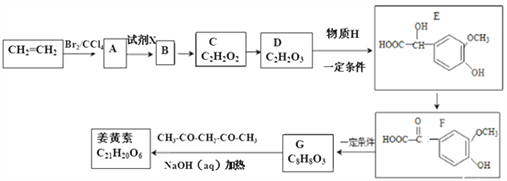
已知:①![]()
②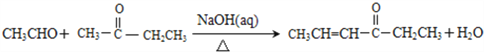
请回答下列问题:
(1)D中含有的官能团名称是___________。
(2)反应A→B的反应条件为________;已知D→E转化中原子利用率100%,则H的结构简式为______________。
(3)姜黄素的结构简式为_________________。
(4)D的催化氧化产物与B可以反应生成一种高分子化合物,其化学方程式为_________________________________________。
(5)下列有关E的叙述不正确的是___________(填正确答案编号)。
a.1molE与浓溴水反应最多消耗3mol的Br2
b.E能发生氧化、加成、取代和缩聚反应
c.1molE最多能与3molNaOH发生反应
d. E能与FeCl3溶液发生显色反应
(6)G(C8H8O3)的同分异构体中,符合下列条件的共有__________种。
①苯环上的一取代物只有2种;②1mol该物质与烧碱溶液反应,最多消耗3molNaOH.
其中核磁共振氢谱中有4组吸收峰的同分异构体的结构简式为_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表是元素周期表的一部分,其中每个数字序号代表一种短周期元素。

请按要求回答下列问题:
(1) 写出②的元素名称____________;
(2) 将①、②和③三种元素相比较,非金属性最强的是____________(填元素符号);
(3) 元素⑥的氢化物的化学式为________________________;
(4) 元素④和元素⑤的最高价氧化物对应的水化物在溶液中相互反应的离子方程式是_________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对外加电流的保护法中,下列叙述正确的是
A.电子从被保护金属流向电源的负极
B.被保护的金属与电源的负极相连
C.在被保护的金属表面上发生氧化反应
D.被保护的金属表面上不发生氧化反应,也不发生还原反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】[2016新课标Ⅱ节选]联氨(又称肼,N2H4,无色液体)是一种应用广泛的化工原料,可用作火箭燃料,回答下列问题:
(1)联氨分子的电子式为_____________,其中氮的化合价为____________。
(2)实验室可用次氯酸钠溶液与氨反应制备联氨,反应的化学方程式为_____________________。
(3)①2O2(g)+N2(g)=N2O4(l) ΔH1
②N2(g)+2H2(g)=N2H4(l) ΔH2
③O2(g)+2H2(g)=2H2O(g) ΔH3
④2 N2H4(l) + N2O4(l)= 3N2(g)+ 4H2O(g) ΔH 4=-1048.9kJ/mol
上述反应热效应之间的关系式为ΔH4=________________,联氨和N2O4可作为火箭推进剂的主要原因为_________________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com