
【题目】设NA为阿伏加德罗常数。下列说法正确的是( )
A. 常温常压下,20 g D2O分子中所含中子数为10 NA
B. 0.1 mol FeCl3水解生成的Fe(OH)3胶粒数为0.1 NA
C. 将lmol Cl2通入水中,HC1O、Cl-、C1O-粒子数之和为2 NA
D. 常温常压下,11.2 L CO2 与足量Na2O2反应转移的电子数为0.5 NA
 亮点激活精编提优100分大试卷系列答案
亮点激活精编提优100分大试卷系列答案科目:高中化学 来源: 题型:
【题目】现有甲、乙、丙三名同学分别进行Fe(OH)3胶体的制备实验:
甲同学向1 mol·L1氯化铁溶液中加入少量的NaOH溶液;
乙同学直接加热饱和FeCl3溶液;
丙同学向25 mL沸水中逐滴加入5~6滴FeCl3饱和溶液;继续煮沸至溶液呈红褐色,停止加热。
试回答下列问题:
(1)其中能得到Fe(OH)3胶体的同学是 。
(2)证明有Fe(OH)3胶体生成的实验操作是 。
(3)丁同学利用所制得的Fe(OH)3胶体进行下列实验:
①将其装入U形管内,用石墨作电极,接通直流电,通电一段时间后发现阴极附近的颜色逐渐变深,这表明Fe(OH)3胶粒带 电荷(填“正”或“负”)。
②向其中加入饱和Na2SO4溶液,产生的现象是 。
(4)Fe(OH)3胶体能稳定存在的主要原因是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A. N和As属于第ⅤA族元素,氮原子得电子能力比砷原子强
B. 族序数等于其周期序数的元素一定是金属元素
C. 元素周期表中,位于金属和非金属交界线附近的元素属于过渡元素
D. Si、S、Cl的最高价氧化物都能与水反应生成相应的酸,且酸性依次增强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】煤的工业加工过程中,可利用CO和H2合成用途广泛的化工原料甲醇,能量变化如图所示。下列说法正确的是

A. 该反应是吸热反应
B. 1molCH3OH所具有的能量为90.lkJ·mol-1
C. CO(g)+2H2(g) ![]() CH3OH(l) △H=-90.1kJ·mol-1
CH3OH(l) △H=-90.1kJ·mol-1
D. 1mol CO和2mol H2断键所需能量小于1mol CH3OH断键所需能量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、W四种短周期元素在元素周期表中的相对位置如图所示。下列说法正确的是
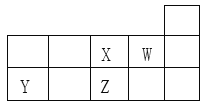
A. Y、Z、X三种元素的原子半径依次增大
B. X、Z都是第2周期VIA族元素,单质的氧化性X>Z
C. Y的气态氢化物的热稳定性比Z的高
D. R元素与W同族且相邻周期,则R元素最高价氧化物的水化物的酸性比Z的强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将等物质的量的甲烷和氯气混合后,在漫射光的照射下充分反应,生成物中物质的量最大的是
A、CH3Cl B、CH2Cl2 C、HCl D、CCl4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是在一定温度下,冰醋酸加水稀释的过程中,溶液的导电能力与加水量的关系。回答下列问题:

(1)0”点导电能力为0的理由__________________________________;
(2)a、b、c三点溶液中氢离子浓度由小到大的顺序为________________________;
(3)a、b、c三点中,醋酸的电离程度最大的一点是_____________;
(4)若使c点溶液中的c(CH3COO-)提高,在如下措施中,可选择__________;
A.加热 B.加水 C.加CH3COONa固体 D.加很稀的NaOH溶液
(5)在稀释过程中,随着醋酸浓度的降低,下列始终保持增大趋势的量是____________。
A.c(H+) B.H+个数 C.CH3COOH分子数 D.c(H+)/c(CH3COOH)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com