
【题目】X、Y、Z、W四种短周期元素在元素周期表中的相对位置如图所示。下列说法正确的是
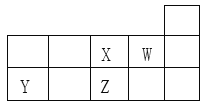
A. Y、Z、X三种元素的原子半径依次增大
B. X、Z都是第2周期VIA族元素,单质的氧化性X>Z
C. Y的气态氢化物的热稳定性比Z的高
D. R元素与W同族且相邻周期,则R元素最高价氧化物的水化物的酸性比Z的强
 目标测试系列答案
目标测试系列答案科目:高中化学 来源: 题型:
【题目】铁及其化合物在日常生产生活中用途广泛。利用FeSO4制备还原铁粉的工业流程如下:

实验室中可用FeSO4(用铁粉和稀硫酸反应制得)和NH4HCO3在如下装置模拟上述流程中的“转化”环节。
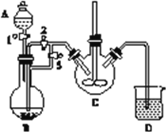
(1)装置A的名称是________,装置B中盛放的试剂是________,NH4HCO3盛放在装置________中。
(2)实验过程中,欲将生成的FeSO4溶液和NH4HCO3溶液混合制FeCO3沉淀,操作方法是________________,发生主要反应的离子方程式为_____________________。FeSO4溶液要现用现配制的原因是____________,检验久置的FeSO4是否变质的方法是______________。
(3)干燥过程主要目的是脱去游离水,过程中会有少量FeCO3在空气中被氧化为FeOOH,该反应的化学方程式为____________________________,取干燥后的FeCO3样品12.49 g,与碳混合后焙烧,最终得到还原铁粉6.16 g,计算样品中杂质FeOOH的质量:________g。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温时,用0.1000mol/L NaOH溶液滴定25.00mL 0.1000mol/L某一元酸HX溶液,滴定过程中pH变化曲线如下图所示。下列说法不正确的是( )

A. 在A点:c(HX)>c(Na+)>c(X-)
B. 在B点,溶液中c(H+)=c(OH-)
C. C点溶液中存在的主要平衡是X- + H2O![]() HX+OH-
HX+OH-
D. 0.05mol/L NaX溶液的pH ≈ 9
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数。下列说法正确的是( )
A. 常温常压下,20 g D2O分子中所含中子数为10 NA
B. 0.1 mol FeCl3水解生成的Fe(OH)3胶粒数为0.1 NA
C. 将lmol Cl2通入水中,HC1O、Cl-、C1O-粒子数之和为2 NA
D. 常温常压下,11.2 L CO2 与足量Na2O2反应转移的电子数为0.5 NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】烟气中SO2和NOx(NO及NO2)的脱除对于环境保护意义重大。
(1)湿式氨法烟气脱硫脱氮是通过氨水吸收烟气,得到含NH4+、SO32-、SO42-、HSO3-、和NO2-的吸收液。
① 用离子方程式解释吸收液中含有SO32-的原因:_______________。
② 吸收液中的SO32-、HSO3-均对NO2具有吸收作用,但HSO3-对NO2的吸收能力比SO32-弱。
a. SO32-与NO2反应生成NO2-的离子方程式是_______________________。
b. 经测定,在烟气的吸收过程中,吸收液对NO2的吸收率随烟气通入量变化的曲线如下图所示。

结合化学用语解释产生上述结果的原因:_____________。
(2)二氧化氯(ClO2)具有很强的氧化性,可用于烟气中SO2和NO的脱除。
① 酸性条件下,电解NaClO3溶液,生成ClO2的电极反应式是__________。
② 研究表明:ClO2氧化SO2和NO的反应历程与下列反应有关。
i.NO + ClO2 === NO2+ ClO
ii.NO + ClO === NO2 + Cl
iii.SO2 + ClO2 === SO3+ ClO
iv.SO2 + ClO === SO3 + Cl
实验测得:ClO2分别氧化纯SO2和纯NO的氧化率以及ClO2氧化SO2和NO混合气中的SO2氧化率随时间的变化情况如下图所示。

a. 结合上述信息,下列推论合理的是________(填字母序号)。
A. NO的存在会影响ClO2氧化SO2的反应速率
B. ClO2氧化SO2的反应速率慢于ClO2氧化NO的反应速率
C. 反应i中生成的NO2可以加快ClO2氧化SO2的反应速率
b. 结合反应历程,分析混合气中SO2氧化速率较纯SO2氧化速率快的可能原因是_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为探究某矿石(仅含两种元素)的组成和性质,设计并完成如下实验:
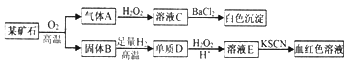
请回答:(1)某矿石的组成元素为__________(用元素符号表示)。
(2)气体A与H2O2溶液反应的化学方程式是________________。
(3)写出D→E的离子方程式____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氢能的存储是氢能应用的主要瓶颈,配位氢化物、富氢载体化合物是目前所采用的主要储氢材料。
(1)Ti(BH4)2是一种过渡元素硼氢化物储氢材料。基态Ti原子电子占据的最高能层符号________,基态Ti2+的价电子的电子排布式_____________。
(2)液氨是富氢物质,是氢能的理想载体,利用N2+3H2![]() 2NH3实现储氢和输氢。下列说法正确的是______(填字母)。
2NH3实现储氢和输氢。下列说法正确的是______(填字母)。
a.NH3分子中氮原子的轨道杂化方式为sp2杂化
b.NH4+与ClO4-、PH4+、CH4、BH4-互为等电子体
c.相同压强时,NH3的沸点比PH3的沸点高
d.电负性C<N<O , 第一电离能C<O<N
(3)Se与O同族,则 SeO2分子的空间构型为_______________。
(4)富勒烯(C60)的结构如图甲,分子中碳原子轨道的杂化类型为__________;1 mol C60分子中σ键的数目为________个。
(5)图乙为一个金属铜的晶胞,此晶胞立方体的边长为a pm,Cu的相对原子质量为64,金属铜的密度为ρ g·cm-3,则阿伏加德罗常数可表示为__________ mol-1(用含a、ρ的代数式表示)。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室现有一瓶标签右半部分已被腐蚀的固体M,剩余部分只看到“Na2S”字样(如图所示)。已知固体M只可能是Na2SO3、Na2SiO3、Na2SO4中的一种。若取少量固体M配成稀溶液进行下列有关实验,其中说法正确的是( )

A. 往溶液中通入二氧化碳,若有白色沉淀,则固体M为Na2SiO3
B. 往溶液中加入稀盐酸酸化的BaCl2,若有白色沉淀,则固体M为Na2SO4
C. 用pH试纸检验,若pH=7,则固体M不一定是Na2SO4
D. 只用盐酸一种试剂不能确定该固体M的具体成分
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com