
【题目】水热法制备Fe3O4纳米颗粒的总反应:3Fe2++2S2O32﹣+O2+xOH﹣→Fe3O4+S4O62﹣+2H2O,有关说法正确的是( )
A.每转移1.5mol电子,有1.125mol Fe2+被氧化
B.x=2
C.Fe2+、S2O32﹣都是还原剂
D.每生成1mol Fe3O4 , 转移电子2mol
【答案】C
【解析】解:在3Fe2++2 S2O32﹣+O2+xOH﹣=Fe3O4+S4O62﹣+2H2O中,化合物中铁元素、硫元素用平均化合价,铁元素的化合价变化:+2→+ ![]() ; 硫元素的化合价变化为:+2→+
; 硫元素的化合价变化为:+2→+ ![]() ;氧元素的化合价变化:0→﹣2,
;氧元素的化合价变化:0→﹣2,
A.由方程式3Fe2++2S2O32﹣+O2+4OH﹣═Fe3O4+S4O62﹣+2H2O可知,当转移4mol电子时,有2molFe2+被氧化,则每转移1.5mol电子,有0.75mol Fe2+被氧化,故A错误;
B.反应的离子方程式为3Fe2++2S2O32﹣+O2+4OH﹣═Fe3O4+S4O62﹣+2H2O,则x=4,故B错误;
C.反应3Fe2++2S2O32﹣+O2+4OH﹣═Fe3O4+S4O62﹣+2H2O中,Fe和S元素的化合价升高,被氧化,Fe2+和S2O32﹣都是还原剂,故C正确;
D.反应3Fe2++2S2O32﹣+O2+4OH﹣═Fe3O4+S4O62﹣+2H2O中,Fe和S元素的化合价升高,被氧化,O2为氧化剂,每生成1molFe3O4 , 需要氧气1mol,反应转移的电子总数为4mol,故D错误.
故选C.


 培优三好生系列答案
培优三好生系列答案科目:高中化学 来源: 题型:
【题目】“一碳化学”是指以含一个碳原子的化合物(如:CO2、CO、CH4、CH3OH等)为初始反应物,合成一系列重要的化工原料和燃料的化学。
(1)以CO2和NH3为原料合成尿素是利用CO2的成功范例。在尿素合成塔中的主要反应可表示如下:
反应I:2NH3(g)+CO2(g)=NH2COONH4(s)△H1
反应II:NH2COONH4(s)=CO(NH2)2(s)+H2O(g) △H2=+72.49kJ/mol
总反应:2NH3(g)+CO2(g)==CO(NH2)2(s)+H2O(g) △H3=-86.98kJ/mol
请回答下列问题:
①反应I的△H1=______ kJ/mol
②反应II一般在_________(填“高温”或“低温”)情况下有利于该反应的进行。
③一定温度下,在体积为固定的密闭容器中按计量比进行反应I,下列能说明反应达到了平衡状态的是__________(填序号)。
A.混合气体的平均相对分子质量不再变化 B.容器内气体总压强不再变化
C.2V正(NH3)=V逆(CO2) D.容器内混合气体的密度不再变化
④环境为真空时,在一敞开容器(非密闭容器)中加入NH2COONH4固体,足够长时间后,反应是否建立平衡状态? ___________(填“是”或“否”)
(2)将CO2和H2充入一定体积的密闭容器中,在两种温度下发生反应:CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g)。测得CH3OH的物质的量随时间的变化如下图。
CH3OH(g)+H2O(g)。测得CH3OH的物质的量随时间的变化如下图。

①曲线I.II对应的平衡常数大小关系为KI_______KII(填“ >”、“<”或“=”)。
②一定温度下,在容积相同且固定的两个密闭容器中,按如下方式加入反应物,一段时间后达到平衡。
容器 | 甲 | 乙 |
反应物投入量 | 1molCO2、3molH2 | amolCO2、bmolH2 cmol CH3OH(g)、cmolH2O(g)(a、b、c均不为零) |
若甲容器平衡后气体的压强为开始的0.8倍,则甲容器平衡混合气体中CH3OH(g)的体积分数为_______,要使平衡后乙容器与甲容器中相同组分的体积分数相等,且起始时维持化学反应向逆反应方向进行,乙容器中c的取值范围为________。
(3)以TiO2/Cu2Al2O4为催化剂,可以将CO2和CH4直接转化成乙酸。在不同温度下催化剂的催化效率与乙酸的生成速率的关系如下图,乙酸的生成速率主要取决于温度影响的范围是________________。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某溶液中加入铝粉能产生H2,在该溶液中一定能大量共存的离子组是
A. Cl-、K+、SO42-、Na+ B. Na+、SO32-、Cl-、NO3-
C. NH4+、Mg2+、SO42-、Cl- D. K+、Na+、NO3-、HCO3-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某离子反应中涉及H2O、ClO-、NH4+、H+、N2、Cl-六种微粒,其中N2的物质的量随时间变化的曲线如图所示,下列判断正确的是( )

A. 该反应的还原剂是Cl-
B. 反应后溶液的酸性明显增强
C. 消耗1mol还原剂,转移6mol电子
D. 氧化剂与还原剂的物质的量之比为2∶3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲、乙、丙、丁、戊是中学常见的无机物,其中甲、乙均为单质,它们的转化关系如图所示(某些条件和部分产物已略去)。下列说法不正确的是:
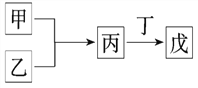
A. 若甲既能与盐酸反应又能与NaOH溶液反应,则丙可能属于两性氧化物
B. 若丙、丁混合产生白烟,且丙为18电子分子,丁为10电子分子,则乙的水溶液可能具有漂白作用
C. 若甲为短周期中原子半径最大的主族元素的单质,且戊为碱,则丙只能为Na2O2
D. 若甲、丙、戊含有同一种元素,则三种物质中,该元素的化合价由低到高的顺序可能为甲<丙<戊
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ:用序号回答:①HCl ②NaOH ③Cl2 ④H2O ⑤NH4Cl ⑥MgCl2
⑦NH3H2O ⑧Na2O2 ⑨HClO ⑩CaO
(1)只存在离子键的是:_______________
(2)既存在离子键又存在共价键的是:__________________
(3)试写出⑨的电子式:_________________________________________________________
Ⅱ: (4)氢氧燃料电池,是一种高效无污染的清洁电池它分碱性(用KOH做电解质)和酸性(用硫酸做电解质)燃料电池。如果是酸性燃料电池则正极反应方程式是:_____________
(5)科研人员设想用如图原电池装置生产硫酸:则负极的电极反应式为:______________________________________________________

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某有机物A的分子式为C4H8O2 , 已知A~E有下列转化关系:试回答下列问题: 
(1)C中的官能团名称是
(2)E的结构简式是 .
(3)在图中①~④的反应中,属于氧化反应的有
(4)写出反应②的化学方程式 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】汉黄芩素是传统中草药黄芩的有效成分之一,对肿瘤细胞的杀伤有独特作用。下列有关汉黄芩素的叙述不正确的是( )

A. 汉黄芩素的分子式为C16H12O5
B. 该物质遇FeCl3溶液显色
C. 1mol该物质与溴水反应,最多消耗2mol Br2
D. 与足量H2发生加成反应后,该分子中官能团的种类减少1种
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com