
| A、不断分离出液氨 |
| B、使用催化剂 |
| C、采用500℃的高温 |
| D、采用20-50Mp的压强 |


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
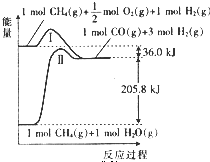 合成气(CO和H2为主的混合气体)不但是重要的燃料,也是重要的化工原料,图中曲线Ⅰ和Ⅱ是两种合成CO和H2反应的能量变化图.
合成气(CO和H2为主的混合气体)不但是重要的燃料,也是重要的化工原料,图中曲线Ⅰ和Ⅱ是两种合成CO和H2反应的能量变化图.查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Na2CO3→NaHCO3 |
| B、SiO2→H2SiO3 |
| C、Fe(OH)2→Fe(OH)3 |
| D、NH4Cl→NH3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、[H2S]+[HS-]+[S2-]=0.1 |
| B、[Na+]+[H+]=2[S2-]+[HS-]+[OH-] |
| C、[OH-]=[H+]+[HS-]+2[H2S] |
| D、[Na+]+[H+]=[S2-]+[HS-]+[OH-] |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、稀盐酸 |
| B、Ba(OH)2溶液 |
| C、NaOH溶液 |
| D、Na2SO4溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、已知氢元素有1H、2H、3H三种同位素,氧元素有16O、18O两种同位素,则它们之间形成的化合物有30种 | ||||||||
| B、能够使pH试纸显红色的溶液pH一定大于7 | ||||||||
| C、已知反应:2(CaO?MgO)(s)+Si(s)?CaSiO4(l)+2Mg(g),在密闭的还原炉内达到平衡后,若其他条件均不改变,将还原炉体积缩小一半,则达到新平衡是Mg(g)的浓度将升高 | ||||||||
D、
|
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、53g碳酸钠中含NA个CO32- |
| B、标准状况下11.2L臭氧中含NA个氧原子 |
| C、1.8g水中含NA个中子 |
| D、0.1molOH-含NA个电子 |
查看答案和解析>>
科目:高中化学 来源: 题型:

| A、由图甲可以判断:T1>T2,且反应的△H<0 |
| B、图乙表示压强对可逆反应2A(g)+2 B(g)?3C(g)+D(s)的影响,乙的压强比甲的压强大 |
| C、根据图丙,若除去CuSO4溶液中的Fe2+,可先向溶液中加入适量双氧水,再调节pH≈4 |
| D、图丁表示用0.1mol/L的盐酸滴定20mL 0.1mol/LNaOH溶液,溶液pH随加入盐酸体积的变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、B单质可能是金属,也可能是非金属 |
| B、B与A形成的化合物一定是离子化合物 |
| C、C单质只有氧化性 |
| D、原子半径:C>B>A |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com