
【题目】有机物R是金银花的一种成分,具有广谱抗病毒功效,键线式为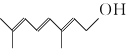 (已知CH2=CHCH2OH的键线式为
(已知CH2=CHCH2OH的键线式为![]() )。下列说法错误的是( )
)。下列说法错误的是( )
A.R能发生加成、氧化、取代反应
B.用酸性高锰酸钾溶液可以确认R含碳碳双键
C.R分子中所有碳原子可能共平面
D.![]() CHO与R互为同分异构体
CHO与R互为同分异构体
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】硫是一种自然界分布较广的元素,在很多化合物中都含有该元素,回答下列问题:
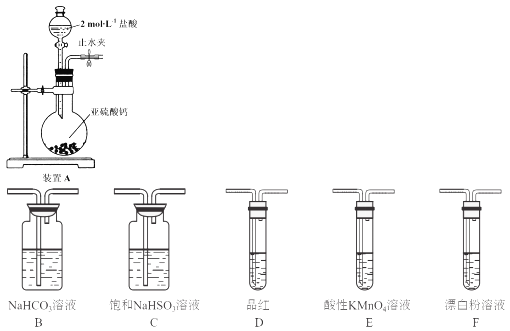
(1)装置A中反应的化学方程式为___________。
(2)使分液漏斗中液体顺利流下的操作是___________。
(3)选用上面的装置和药品探究亚硫酸与次氯酸的酸性强弱:
①甲同学认为按照A→C→F的顺序连接装置即可证明,乙同学认为该方案不合理,其理由是___________。
②丙同学设计的合理实验方案为:A→C→_____→___→D→F,其中装置C的作用是_____,证明亚硫酸的酸性强于次氯酸的实验现象是____。
(4)K2S2O3具有强氧化性,可通过电解H2SO4和K2SO4的混合溶液制得,其阳极反应式为_____。称取0.2500g产品于碘量瓶中,加100mL水溶解,再加入8.000g KI固体(稍过量),振荡使其充分反应;加入适量醋酸溶液酸化,以淀粉为指示剂,用cmol/L的Na2S2O3标准液滴定至终点,消耗Na2S2O3标准液VmL,则样品中K2S2O8的纯度为______%(用含c、V的代数式表示,已知:S2O82-+2I-=2SO42-+I2;2S2O32-+I2=S4O62-+2I-)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)下列几组物质中,互为同位素的有__________,互为同素异形体的有__________,互为同系物的有__________,互为同分异构体的有__________,属于同种物质的__________。
①O2和O3 ②35Cl和37Cl③CH3CH3和CH3CH2CH3④CH3CH2CH(CH3)CH2CH3和CH3CH2CH(CH3)CH(CH3)CH3
⑤H2、D2和T2⑥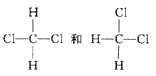 ⑦CH3(CH2)2CH3和(CH3)2CHCH3 ⑧CH3CH(CH3)CH和CH(CH3)3
⑦CH3(CH2)2CH3和(CH3)2CHCH3 ⑧CH3CH(CH3)CH和CH(CH3)3
(2)含有10个及10个以下碳原子的烷烃,其一氯代物只有一种的共有4种,请写出这4种烷烃的结构简式和名称:_______、_______、______、______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铈及其化合物在工业生产中应用广泛。以某玻璃废料(主要成分为CeO2、SiO2、Fe2O3、FeO等)为原料制备CeO2和NH4Fe(SO4)2·12H2O(硫酸铁铵晶体),其流程如下(已知CeO2既不溶于稀硫酸,也不溶于氢氧化钠溶液):
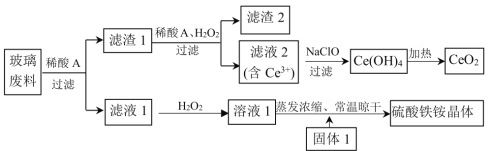
回答下列问题:
(1)浸取玻璃废料选用的“稀酸A”为____________(填“稀硫酸”或“稀盐酸”)。
(2)向滤渣1加入H2O2的目的是_________(用离子方程式表示)。为了提高溶解“滤渣1”的速率,常釆用加热措施,但温度高于60℃时溶解速率减慢,其主要原因是____________。
(3)为了不引入杂质,所选用固体1的化学式为_______________。
(4)制备2mol CeO2需要NaClO的质量为____________。
(5)锌铈液流电池放电时的工作原理如图所示。
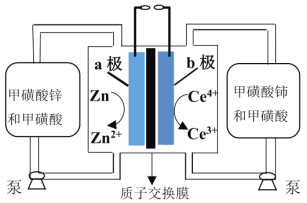
①放电时电池的总离子反应方程式为____________________。
②充电时,当a极增重6.5g时,有_________mol离子通过交换膜以平衡电荷。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知热化学方程式:则下列说法正确的是
①CO(g)+![]() O2(g)=CO2(g) ΔH=-283.0kJ·mol-1
O2(g)=CO2(g) ΔH=-283.0kJ·mol-1
②H2(g)+![]() O2(g)=H2O(g) ΔH=-241.8kJ·mol-1
O2(g)=H2O(g) ΔH=-241.8kJ·mol-1

A. H2的燃烧热为241.8kJ·mol-1
B. 由反应①、②可知如图所示的热化学方程式为CO(g)+H2O(g)=CO2(g)+H2(g) ΔH =-41.2kJ·mol-1
C. H2(g)转变成H2O(g)的化学反应一定要释放能量
D. 根据②推知反应H2(g) +1/2O2(g)=H2O(l):ΔH>-241.8 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为确定HCl、H2CO3、H2SiO3的酸性强弱,某同学设计了如图所示的装置,下列有关叙述正确的是( )
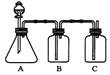
A.HCl、H2CO3、H2SiO3的酸性依次增强
B.A中锥形瓶中生成CO2气体
C.B中装饱和Na2CO3溶液,用于除去A中挥发出的HCl气体
D.C中装Na2SiO3溶液,预期现象是先出现白色沉淀后又逐渐溶解
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与人类生产、生活密切相关,下列叙述中正确的是( )
A.石英是制造光导纤维的原料,也是常用的半导体材料
B.刚玉![]() 硬度仅次于金刚石,可做机械轴承,属于无机非金属材料
硬度仅次于金刚石,可做机械轴承,属于无机非金属材料
C.泰国银饰和土耳其彩瓷,其主要成分均为金属材料
D.手机外壳上贴的碳纤维外膜是一种新型的有机高分子材料
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据元素周期表和元素周期律,判断下列叙述不正确的是
A. 气态氢化物的稳定性:H2O>NH3
B. 钠元素的金属性比镁元素的强
C. 图所示实验可证明元素的非金属性:Cl>C>Si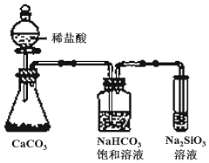
D. 在元素周期表中金属和非金属的分界处可以找到半导体材料
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图的实验装置可用于研究SO2转化为SO3的转化率。已知:SO3的熔点是16.8℃,沸点是44.8℃处为SO2气体发生装置,C处为SO2与O2反应的装置。
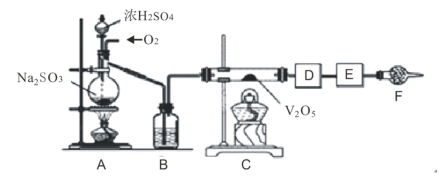
完成下列填空:
(1)A处的化学反应方程式为___,所用的硫酸一般为___(此处填98%的硫酸溶液、70%的硫酸溶液或30%的硫酸溶液)。
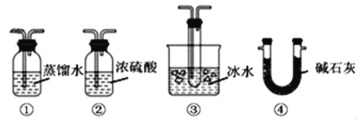
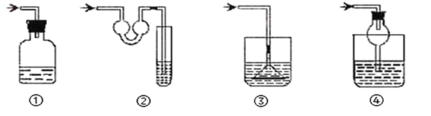
(2)根据实验需要,应该在D、E处连接合适的装置。请从图中选择,将所选装置的序号填入相应的空格,D:___,E:____。
(3)用12.6gNa2SO3粉末与足量浓硫酸进行此实验,当A处反应结束时,再继续通入一段时间![]() ,最后测得E处装置增重1.28gSO2,则此时SO2的转化率为____%。
,最后测得E处装置增重1.28gSO2,则此时SO2的转化率为____%。
(4)若Na2SO3变质,会影响到SO2的转化。现欲检验某Na2SO3样品是否变质,你的方法是___。
(5)以下各种尾气吸收装置中,适合于吸收该尾气,而且能防止倒吸的是___。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com