
【题目】分析下表中的四个热化学方程式,判断氢气和丙烷的标准燃烧热分别是
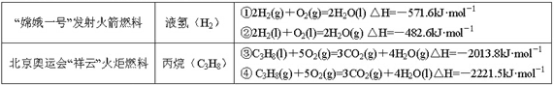
A.-571.6 kJ·mol-1,-2221.5 kJ·mol-1B.-285.5 kJ·mol-1,-2013.8 kJ·mol-1
C.-285.8 kJ·mol-1,-2221.5 kJ·mol-1D.-241.3 kJ·mol-1,-2013.8 kJ·mol-1
【答案】C
【解析】
①2H2(g)+O2(g)=2H2O(l) △H=-571.6kJmol-1,热化学方程式是2mol氢气燃烧生成稳定氧化物的反应放出的热量,而燃烧热为1mol氢气完全燃烧产生稳定的氧化物所放出的热量,是571.6÷2=285.8kJmol-1; ②2H2(l)+O2(l)=2H2O(g) △H=-482.6kJmol-1,热化学方程式生成的是气体水,不是稳定氧化物,不能据此计算;③C3H8(l)+5O2(g)=3CO2(g)+4H2O(g) △H=-2013.8kJmol-1,反应生成的水是气体,不是稳定氧化物,不能据此计算;④C3H8(g)+5O2(g)=3CO2(g)+4H2O(l) △H=-2221.5kJmol-1,是1mol丙烷完全燃烧生成稳定氧化物放出的热量,所以丙烷的燃烧热即为2221.5kJmol-1;
故选C。


科目:高中化学 来源: 题型:
【题目】一定温度下,对可逆反应A(g)+2B(g)3C(g)的下列叙述中,能说明反应已达到平衡的是( )
A.单位时间内消耗a molA,同时生成3a molCB.容器内B的浓度不再变化
C.混合气体的物质的量不再变化D.A的消耗速率等于C的生成速率的![]() 倍
倍
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】SiC纤维单向增强的TixAly基复合材料可作为高超音速飞行器表面的放热材料。回答下列问题:
(1)C元素所在周期中,第一电离能最大的元素是__(填元素符号),电负性最大的是__(填元素符号)。
(2)基态Ti原子的价电子排布式为__,能量最高的能级有__个空轨道。
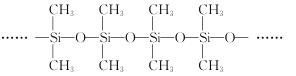
(3)甲基硅油结构如图所示,其中Si原子的杂化方式为__。以甲基硅油为主要成分的硅橡胶能够耐高温的原因是__。
(4)Li2CO3、Li2TiO3是锂离子电池中的常用材料,其中CO32-的空间构型为__,其含有的共价键类型有__。
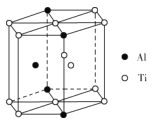
(5)TixAly合金的一种结构单元如图所示(Al、Ti原子各有一个原子在结构单元内部),该合金的化学式为__。其结构单元棱长为apm,底面边长为bpm,该合金的密度为___g·cm-3。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硝酸钙晶体[Ca(NO3)2·4H2O]常用于电子、仪表及冶金工业。一种利用CaO制备Ca(NO3)2·4H2O的流程如下:

(1)“制浆”过程中发生反应的化学方程式是__。
(2)“气体X”的化学式是___。
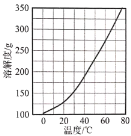
(3)Ca(NO3)2·4H2O的溶解度随温度变化的曲线如图所示。“酸化”后制取Ca(NO3)2·4H2O的操作主要包括加热浓缩、__、过滤、洗涤、干燥。实验室过滤操作必须用到的玻璃仪器有烧杯、玻璃棒和__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙醇(CH3CH2OH)既是生活中常见的有机物,又是重要的化工原料。
(1)工业上可用乙烯制备乙醇,其反应的化学方程式为:CH2 = CH2+H2O![]() CH3CH2OH,该反应属于__反应(填“加成”或“取代”)。
CH3CH2OH,该反应属于__反应(填“加成”或“取代”)。
(2)官能团决定有机物的性质。乙醇中含有的官能团名称是__。
(3)为探究乙醇的性质,某学生向试管中加入3mL乙醇,将下端绕成螺旋状的铜丝在酒精灯火焰上灼烧至红热后,迅速插入乙醇中,可观察到铜丝表面由黑色变成红色,说明乙醇具有__性。
(4)萃取是物质分离的一种方法。某学生拟用乙醇萃取溴水中的Br2,判断该方法是否可行:__(填“是”或“否”),判断的理由是__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯化铅(PbCl2)常用于焊接和制备铅黄等染料。利用从废旧铅蓄电池中得到的铅膏获取氯化铅的流程如图。试回答下列问题:
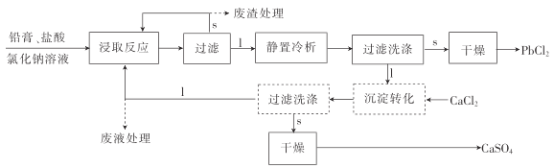
已知:①铅膏主要由PbSO4、PbO、PbO2和Pb等组成。
②流程图中的"1”表示液体,“s”表示固体。
③硫酸铅,氯化铅微溶于水,但氯化铅能溶于NaCl溶液中,主要发生反应:PbCl2+C1-=[PbCl3]-。
(1)铅蓄电池的正极材料是__(填化学式),放电时负极的电极反应式为__。
(2)“浸取反应”是在加热条件下,用盐酸和氯化钠溶液浸取铅膏的过程,主要发生反应的方程式有PbO2+Pb+4HC1=2PbCl2+2H2O,PbO+2HCl=PbCl2+H2O,PbSO4+2NaCl=PbCl2+Na2SO4,PbCl2+Cl-=[PbCl3]-,除此之外,PbO2还能与HCl反应产生一种黄绿色气体,该反应的化学方程式是__,该浸取过程中操作不慎可能会造成意外,原因是___。
(3)PbCl2在氯化钠溶液中的溶解度随温度的升高而增大,适当地升高温度有利于提高铅的浸取率,当温度高于70℃时,浸取率提高不明显,可能的原因是__;为了提高浸取率,还可以采取的措施是___。
(4)在室温下静置冷却3h后,过滤得到的氯化铅的回收率可达到85%,过滤后得到的滤液进行循环使用可提高铅的利用率。在循环使用之前需加入氯化钙进行沉淀转化,若无此步骤,直接循环使用,则会导致的结果是__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫酸钡是一种比碳酸钡更难溶的物质。常温下-lg c(Ba2+)随-lg c(CO32-)或-lg c(SO42-)的变化趋势如图,下列说法正确的是( )
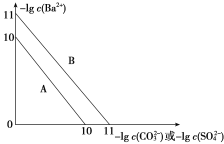
A.趋势线A表示硫酸钡
B.常温下,Ksp(BaCO3)=1×10-11
C.将碳酸钡和硫酸钡固体置于水中,此时溶液中的![]() =10
=10
D.在硫酸钡悬浊液中,若要使0.1 mol的硫酸钡完全转化成碳酸钡,则需要加入碳酸钠的物质的量至少为0.1 mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】水系锂电池具有安全、环保和价格低廉等优点成为当前电池研究领域的热点。以钒酸钠(NaV3O8)为正极材料的电极反应式为:NaV3O8+xLi++xe-=NaLixV3O8,则下列说法不正确的是( )
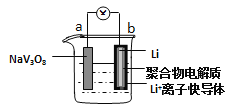
A.充电过程中阳极的电极反应式为NaLixV3O8-xe-=NaV3O8+xLi+,NaLixV3O8中钒的化合价发生变化
B.充电过程中Li+从阳极向阴极迁移
C.放电时,负极的电极反应式:Li-e-=Li+
D.该电池可以用硫酸锂溶液作电解质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铝试剂的结构简式如图所示,下列有关铝试剂的说法错误的是
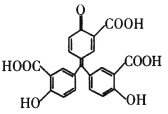
A.铝试剂分子中氢原子数目为16
B.1 mol铝试剂最多消耗3 mo1NaHCO3
C.铝试剂分子中所有碳原子可能在同一平面上
D.铝试剂能与FeCl3溶液发生显色反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com