
| A、水壶中水垢用食醋除去:2H++CaCO3=Ca2++CO2↑+H2O 2H++Mg(OH)2=Mg2++2H2O |
| B、向NaHSO4溶液中滴入Ba(OH)2溶液至中性H++SO42-+Ba2++OH-=BaSO4↓+H2O |
| C、向FeI2溶液中通入少量Cl2 2I-+Cl2=I2+2Cl- |
| D、等体积等浓度的Ba(OH)2稀溶液与NH4HCO3稀溶液混合:Ba2++2OH-+NH4++HCO3-=BaCO3↓+NH3↑+2H2O |


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
| 物质编号 | 物质转化关系 | a | b | c | d |
| ① | 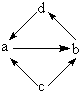 |
FeCl2 | FeCl3 | Fe | CuCl2 |
| ② | Mg | MgO | MgCl2 | Mg(OH)2 | |
| ③ | NaOH | Na2CO3 | NaHCO3 | NaCl | |
| ④ | Al2O3 | NaAlO2 | Al | Al(OH)3 |
| A、①④ | B、②④ |
| C、①③④ | D、①②③ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、用甲醛溶液浸泡的海鲜品 |
| B、牛奶经工业发酵后得到的酸奶 |
| C、加有苏丹红Ⅰ号调色剂的鲜辣酱 |
| D、二氧化硫熏制后的白面粉? |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、铝热反应是炼铁最常用的方法 |
| B、Na2O2用作呼吸面具的供氧剂 |
| C、Na2FeO4有强氧化性,可用作自来水的消毒剂 |
| D、小苏打和氢氧化铝均可用来作治疗胃酸过多的药物 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、向NaAlO2溶液中通入过量CO2:AlO2-+CO2+2H2O═Al(OH)3↓+HCO3- |
| B、Cl2与水的反应:Cl2+H2O═2H++Cl-+ClO- |
| C、醋酸溶液与水垢中的CaCO3反应:CaCO3+2H+═Ca2++H2O+CO2↑ |
| D、FeCl3溶液与Cu的反应:Cu+Fe3+═Cu2++Fe2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| N |
| NA |
| m |
| M |
| V |
| 22.4 |
| nB(mol) |
| V(L) |
| 1000?ρ?wB |
| M |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
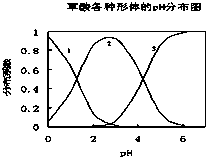 草酸(H2C2O4)是一种易溶于水的二元中强酸,在水中它的存在形态有H2C2O4、HC2O4-、C2O42-,各形态的分布系数(浓度分数)α随溶液pH变化的关系如图所示:
草酸(H2C2O4)是一种易溶于水的二元中强酸,在水中它的存在形态有H2C2O4、HC2O4-、C2O42-,各形态的分布系数(浓度分数)α随溶液pH变化的关系如图所示:| c(Na+) |
| c(C2O42-) |
| c(Na+) | ||
c(C2
|
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com