
【题目】某学生设计了一个“黑笔红字”的趣味实验。滤纸先用氯化钠、无色酚酞的混合液浸湿,然后平铺在一块铂片上,接通电源后,用铅笔在滤纸上写字,会出现红色字迹。据此,下列叙述正确的是( )
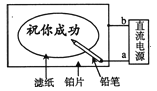
A. 铅笔芯作阳极,发生还原反应
B. 铂片端作阴极,发生氧化反应
C. 铅笔端附近有少量的氯气产生
D. 红字是H+放电,c(OH-)增大造成
【答案】D
【解析】此为电解氯化钠溶液的实验装置,电解时的阴极反应为:2H++2e-═H2↑或2H2O+2e-═H2↑+2OH-,阳极发生的反应为:2Cl--2e-═Cl2↑,总反应为:2NaCl+2H2O![]() 2NaOH+Cl2↑+H2↑,阴极溶液呈碱性,滴加酚酞溶液呈红色。A、用铅笔在滤纸上写字,会出现红色字迹,说明铅笔做阴极,反应为:2H++2e-═H2↑或2H2O+2e-═H2↑+2OH-,溶液呈碱性,滴加酚酞溶液呈红色,所以铅笔芯作阴极,发生还原反应,故A错误;B、阴极发生还原反应,阳极发生氧化反应,在该电解池中,铅笔做阴极,铂片做阳极,故B错误;C、铅笔做阴极,反应为:2H++2e-═H2↑,或2H2O+2e-═H2↑+2OH-,有氢气产生,故C错误;D、用铅笔在滤纸上写字,会出现红色字迹,说明铅笔做阴极,反应为:2H++2e-═H2↑或2H2O+2e-═H2↑+2OH-,溶液呈碱性,滴加酚酞溶液呈红色,故D正确;故选D。
2NaOH+Cl2↑+H2↑,阴极溶液呈碱性,滴加酚酞溶液呈红色。A、用铅笔在滤纸上写字,会出现红色字迹,说明铅笔做阴极,反应为:2H++2e-═H2↑或2H2O+2e-═H2↑+2OH-,溶液呈碱性,滴加酚酞溶液呈红色,所以铅笔芯作阴极,发生还原反应,故A错误;B、阴极发生还原反应,阳极发生氧化反应,在该电解池中,铅笔做阴极,铂片做阳极,故B错误;C、铅笔做阴极,反应为:2H++2e-═H2↑,或2H2O+2e-═H2↑+2OH-,有氢气产生,故C错误;D、用铅笔在滤纸上写字,会出现红色字迹,说明铅笔做阴极,反应为:2H++2e-═H2↑或2H2O+2e-═H2↑+2OH-,溶液呈碱性,滴加酚酞溶液呈红色,故D正确;故选D。


科目:高中化学 来源: 题型:
【题目】已知:25℃时,0.1mol·L-lCH3COOH的电离度(已电离的CH3COOH分子数/原CH3COOH分子总数)约为1%。该温度下,用0.1000mol·L-l氨水滴定10.00 mL0.1000mol·L-lCH3COOH溶液,溶液的pH与溶液的导电能力(I)的关系如图所示。下列说法正确的是

A. M点→N点,水的电离程度逐渐增大
B. 25℃时,CH3COOH 的电离常数约为1.0×10-2
C. N点溶液中,c(CH3COO-) =c(NH4+)=0.05 mol·L-l
D. 当滴入20 mL氨水时,溶液中c(CH3COO-)>c(NH4+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.A、B、C、D四种短周期元素,原子序数依次增大,A原子的最外层上有4个电子;B的阴离子和C的阳离子具有相同的电子层结构,两元素的单质反应,生成一种淡黄色的固体E,D的L层电子数等于K、M两个电子层上的电子数之和。A为 ,B为 ,C为 ,D的最高价氧化物的水化物是 。 (用化学式填空)
Ⅱ.一定温度下,在1L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如下图所示: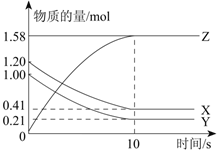
(1)反应开始到10 s,用Z表示的反应速率为 mol/(Ls)。
(2)反应开始到10 s,X的物质的量浓度减少了 mol/L。
(3)反应的化学方程式为: 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验中需2mol/L的Na2CO3溶液950mL,配制时应选用的容量瓶的规格和称取Na2CO3质量是
A.1000mL,212gB.950mL,543.4gC.950mL,572gD.500mL,286g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列电离方程式的书写错误的是 ( )。
A.BaCl2=Ba2++Cl-B.Na2CO3=2Na++CO32-
C.MgCl2=Mg2++2Cl-D.Ba(OH)2=Ba2++2OH-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】中华文化源远流长、博大精深。从化学的视角看,下列理解错误的是( )
A | B | C | D | |
中华 文化 | “千淘万漉虽辛苦,吹尽狂沙始到金”--刘禹锡《浪涛沙》 | 《天工开物》锤锻篇(冶铁)记载:“谚云,‘万器以钳为祖。’非无稽之说也。” | 成语“刀耕火耨(nòu)” |
侯德榜 |
从化学 的视角 理解 | 诗句中的“淘、漉”相当于分离提纯操作中的“过滤” | “钳”是指作为熔铁炉、加热炉的坩埚 | 古人播种前先伐去树木烧掉野草,用余灰可以肥田,还可以降低土壤碱性 | 我国化学工业的奠基人,主要成就: 侯氏制碱法,该碱指的是纯碱 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学课外小组查阅资料知:苯和液溴在有溴化铁(FeBr3)存在的条件下可发生反应生成溴苯和溴化氢,此反应为放热反应。他们设计了下图装置制取溴苯。先向分液漏斗中加入苯和液溴,再将混合液慢慢滴入反应器A中。
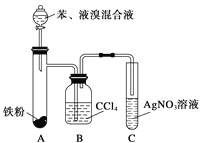
请回答下列问题:
(1)装置A中发生反应的化学方程式是______________________________。
(2)装置C中看到的现象是__________________,证明_________。
(3)装置B内盛有四氯化碳,实验中观察到的现象是_____________,原因是____。
(4)如果没有B装置,将A、C直接相连,你认为是否妥当(填“是”或“否”)________,理由是_________________________________。
(5)实验完毕后将A试管中的液体倒在装有冷水的烧杯中,烧杯____层(填“上”或“下”)为溴苯,这说明溴苯____________且____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】尿素[CO(NH2)2]是首个由无机物人工合成的有机物。
(1)工业上尿素由CO2和NH3在一定条件下合成,其反应方程式为_______________。
(2)当氨碳比 ![]() =4,时CO2的转化率随时间的变化关系如图1所示。
=4,时CO2的转化率随时间的变化关系如图1所示。
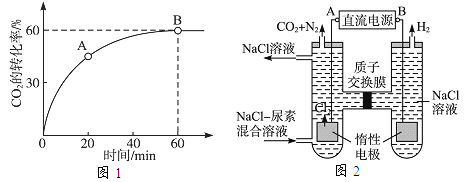
①A点的逆反应速率v逆(CO2)_______B点的正反应速率v正(CO2)(填“<”、“>”或“=”)。
②反应达到平衡后,NH3的转化率为_____________。
(3)人工肾脏可采用间接电化学方法除去代谢产物中的尿素,原理如图2。
①电源的负极为_____(填“A”或“B”)。
②阳极室中发生的电极反应为_________,_________________。
③若两极共收集到气体13.44L(标准状况),则除去的尿素为________g(忽略气体的溶解)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲醚(CH3OCH3)被称为21世纪的新型燃料,它清洁、高效、具有优良的环保性能,甲醚是一种无色气体,具有轻微的醚香味,其燃烧热为1455 kJ·mol﹣1,甲醚可作燃料电池的燃料.
(1)写出甲醚燃烧的热化学方程式 ;已知H2(g)和C(s)的燃烧热分别是285.8kJ·mol﹣1、393.5kJ·mol﹣1;计算反应4C(s)+6H2(g)+O2(g)═2CH3OCH3(g)的反应热△H= kJ·mol﹣1;
(2)工业上利用H2和CO2合成二甲醚的反应如下:6H2(g)+2CO2(g)![]() CH3OCH3(g)+3H2O(g)△H<0
CH3OCH3(g)+3H2O(g)△H<0
①一定温度下,在一个固定体积的密闭容器中进行该反应.下列能判断反应达到化学平衡状态的是 (选填编号,注意大小写)。
a.c(H2)与c(H2O)的比值保持不变
b.单位时间内有2mol H2消耗时,有1mol H2O生成
c.容器中气体密度不再改变
d.容器中气体压强不再改变
②温度升高,该化学平衡移动后,达到新的平衡,CH3OCH3的产率将 (填“变大”、“变小”或“不变”,下同)。
(3)以甲醚、空气、氢氧化钾溶液为原料,石墨为电极可构成燃料电池.该电池的负极反应式的其中一个产物是CO32﹣,请写出该反应的负极反应式 ;
(4)用(3)中的燃料电池为电源,以石墨为电极电解500mL NaCl溶液,装置如图所示,请写出电解过程中Y电极附近观察到的现象是 ;当燃料电池消耗2.8LO2(标准状况下)时,计算此时:NaCl溶液中C(OH-)= mol/L(假设溶液的体积不变,气体全部从溶液中逸出).

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com