
【题目】下列微粒在所给条件下,一定可以大量共存的是
A. 酸性溶液中:![]() 、
、![]() 、
、![]() 、
、![]()
B. 遇酚酞显红色的溶液中:![]() 、
、![]() 、
、![]() 、
、![]()
C. 与铝反应能产生大量氢气的溶液中:![]() 、
、![]() 、
、![]() 、
、![]()
D. 透明溶液中:![]() 、
、![]() 、
、![]() 、
、![]()
【答案】A
【解析】
A.Fe2+、Al3+、SO42、NH4+之间不反应,且都不与氢离子反应,在酸性溶液中能够大量共存,故A符合题意;
B.该溶液中存在大量氢氧根离子,Cl2、I之间发生氧化还原反应,Mg2+与氢氧根离子反应,Cl2与氢氧根离子之间发生氧化还原反应,在溶液中不能大量共存,故B不符合题意;
C.该溶液呈酸性或强碱性,HCO3能与氢离子或氢氧根离子反应,CH3COO与氢离子发生反应生成弱电解质醋酸,在溶液中一定不能大量共存,故C不符合题意;
D.铁离子和氢氧根反应生成难溶物氢氧化铁,铁离子和碳酸氢根会发生相互促进的双水解而生成难溶物氢氧化铁和二氧化碳,氢氧根和碳酸氢根会发生离子反应,在溶液中一定不能大量共存,故D不符合题意,答案选A。


科目:高中化学 来源: 题型:
【题目】将a g由CO和H2组成的混合气体在足量的O2中充分燃烧后,将生成的所有产物通过足量的Na2O2固体,Na2O2固体增加的质量为
A. a g B. ![]() g
g
C. ![]() g D.
g D. ![]() g
g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为进行某些实验的探究,某兴趣小组设计了如下装置。

(1)为探究浓硫酸与木炭反应的全部产物,分液漏斗中盛浓硫酸,圆底烧瓶中放木炭。
①装置B中试剂的名称是________。
②装置C、D、E中所盛放的试剂分别是品红、酸性KMnO4溶液和澄清的石灰水。C装置的作用是________,确认产物中含有CO2的实验现象是________。
(2)为了制取无水氯化铜,上述装置中的分液漏斗中盛浓盐酸,圆底烧瓶中放MnO2,B中放铜粉并在玻璃管下添加酒精灯,且将B装置平移至D与E之间。
①此时C、D中依次加入的试剂分别是________。
②若E中为NaOH溶液用于尾气吸收,常温下发生反应的离子方程式为________。
③实验结束时,应首先熄灭装置B下面的酒精灯,其目的是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】植物在冬季来临过程中,随着气温的逐渐降低,体内发生了一系列适应低温的生理生化变化,抗寒力逐渐增强。下图为冬小麦在不同时期含水量和呼吸速率变化关系图。请根据图推断以下有关说法中,错误的是( )
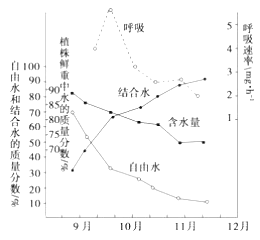
A. 冬季来临过程中,自由水明显减少是呼吸速率下降的主要原因
B. 结合水与自由水含量的比值,与植物的抗寒性呈现明显的正相关
C. 随着气温和土壤温度的下降,根系的吸水量减少,组织的含水量下降
D. 随温度的缓慢降低,植物的呼吸作用逐渐减弱,有利于减少有机物的消耗
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下、1L密闭容器中,3种气体起始状态和平衡状态时的物质的量(n)如下表所示,下列有关说法正确的是
x | y | w | |
n(起始)/mol | 2 | l | 0 |
n(平衡)/mol | l | 0.5 | 1.5 |
A. 该温度下,此反应的平衡常数表达式是![]()
B. 升高温度,若w的体积分数减小,则此反应ΔH>0
C. 增大压强,正、逆反应速率均增大,平衡向正反应方向移动
D. 该温度下,再向容器中通入3molw,达到平衡时,n(x)=2mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室有一份含有杂质MgCl2和KCl的AlCl3溶液M,某小组用下图所示过程对其进行除杂并尽可能的减少AlCl3的损失。请回答下列问题:

(1)沉淀A的化学式为__________,过程①中Al3+发生反应的离子方程式为__________________。
(2)氢氧化钠溶液_____(填“能”或“不能”)用氨水代替,原因是_____________________。
(3)溶液B中大量存在的阳离子是______________,过程②中生成沉淀C的离子方程式为_____________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下,向KOH溶液中通入11.2L(已换算成标准状况下)氯气恰好完全反应生成二种含氯盐:0.7molKC1、0.2mnolKClO和X。则X是
A. 0.1molKClO3 B. 0.2molKClO3 C. 0.1molKClO4 D. 0.2molKClO4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氨作为重要化工原料,被大量应用于工业生产。氨在不同催化剂条件下可发生下列两个反应:
反应I:4NH3(g) +5O2(g)![]() 4NO(g) +6H2O(g) △H=-905.0 kJ·molˉ1
4NO(g) +6H2O(g) △H=-905.0 kJ·molˉ1
反应 II:4NH3(g)+3O2(g)![]() 2N2(g) +6H2O(g) △H=-1266.6kJ·molˉ1
2N2(g) +6H2O(g) △H=-1266.6kJ·molˉ1
(1)写出NO分解生成N2与O2的热化学方程式:___________________________。
(2)反应I在容积固定的密闭容器中进行,容器内部分物质的物质的量浓度如下表:
时间 浓度 | c(NH3)/mol/Ll | c((O2)/mol/L | c(NO)/ mol/L |
第 0 min | 0.8 | 1.6 | 0 |
第 2 min | 0.3 | 0.975 | 0.5 |
第 3 niin | 0.3 | 0.975 | 0.5 |
第4 min | 0.7 | 1.475 | 0.1 |
①反应从开始到第2min时,v(H2O)=__________________。
②在第3min时,改变的反应条件可能是_________(填选项字母)。
A.使用催化剂 B.臧小压强 C.升高温度 D.增加O2的浓度
③该反应达到平衡状态的标志是___________(填选项字母)。
A.在恒温恒容的容器中,混合气体的密度不再变化
B.单位时间内消耗nmolNO的同时消耗nmolNH3
C.百分含量w(NH3)=w(NO)
D.反应速率v(NH3):v(O2):v(NO):v(H2O)=4:5:4:6
(3)①若在容积为2L的密闭容器中充入8molNH3(g)和6molO2(g),发生反应II。保持其他条件不变,在相同时间内测得c(N2)与温度的关系如图所示。则T1℃下,NH3的平衡转化率为___。
②图中a、c两点对应的容器内部压强Pa____Pc(填“>”、“<”或“=”)

(4)氨气可用于生成硝酸铵化肥。25℃时,已知NH3·H2O的电离常数Kb=1.8×10-5,则硝酸铵在此温度下发生水解反应的平衡常数Kh=___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一次有机化学课堂小组讨论中,某同学设计了下列合成路线,你认为不可行的是( )
A. 用氯苯合成环己烯:![]()
B. 用甲苯合成苯甲醇:![]()
C. 用乙烯合成乙酸:![]()
D. 用乙烯合成乙二醇:![]()
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com