
【题目】反应X(g)+3Y(g)![]() 2Z(g);ΔH<0 在不同温度、不同压强(P1>P2)下,达到平衡时,混合气体中Z的体积分数φ(Z)随温度变化的曲线为 ( )
2Z(g);ΔH<0 在不同温度、不同压强(P1>P2)下,达到平衡时,混合气体中Z的体积分数φ(Z)随温度变化的曲线为 ( )

A. A B. B C. C D. D
【答案】C
【解析】对于反应X(g)+3Y(g)2Z(g)△H<0,正反应是体积减小的放热反应,升高温度平衡向逆反应移动,Z的体积φ(Z)减小;增大压强平衡向正反应移动,Z的体积φ(Z)增大,A.由图象可知,压强一定时,温度越高,Z的体积φ(Z)越大,与实际不符合,故A错误;B.由图象可知,压强一定时,温度越高,Z的体积φ(Z)越大,与实际不符合,故B错误;C.由图象可知,压强一定时,温度越高,Z的体积φ(Z)减小;温度一定时,压强越高,Z的体积φ(Z)增大,与实际相符,故C正确;D.由图象可知,压强一定时,温度越高,Z的体积φ(Z)越小;温度一定时,压强越高,Z的体积φ(Z)减小,与实际不符合,故D错误;故选C。


 口算小状元口算速算天天练系列答案
口算小状元口算速算天天练系列答案科目:高中化学 来源: 题型:
【题目】25 ℃时,水的电离达到平衡:H2O![]() H++OH―;ΔH>0 。则下列叙述正确的是
H++OH―;ΔH>0 。则下列叙述正确的是
A. 向水中加入稀氨水,水的电离程度增大
B. 向水中加入少量固体醋酸钠,平衡逆向移动,c(H+)降低
C. 向水中加入少量固体硫酸氢钠,c(H+)增大,KW不变
D. 将水加热,平衡逆向移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】能正确表示下列反应的离子方程式的是( )
A. Fe2O3溶于过量氢碘酸溶液中:Fe2O3+6H++2I-===2Fe2++I2+3H2O
B. 0.1 mol·L-1 NH4Al(SO4)2溶液与0.2 mol·L-1 Ba(OH)2溶液等体积混合:Al3++2SO![]() +2Ba2++4OH-===2BaSO4↓+AlO
+2Ba2++4OH-===2BaSO4↓+AlO![]() +2H2O
+2H2O
C. 向0.1 mol·L-1、pH=1的NaHA溶液中加入NaOH溶液:HA-+OH-===A2-+H2O
D. 向次氯酸钠溶液中通入足量SO2气体:ClO-+SO2+H2O===HClO+HSO![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海水综合利用要符合可持续发展的原则,其联合工业体系(部分)如图所示,下列说法错误的是( )

A. ①中可采用蒸馏法
B. ②制镁过程中用到的沉淀剂是石灰乳
C. ③中提溴涉及到复分解反应
D. ④的产品可生产盐酸、漂白液等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.苯酚沾在皮肤上用大量的水冲洗
B.氯乙烷与NaOH水溶液共热可制乙烯
C.为了鉴别己烯、甲苯和丙醛,可以使用新制Cu(OH)2悬浊液与溴水
D.CH3Cl可发生水解反应和消去反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】H2O2分解速率受多种因素影响。实验测得70℃时不同条件下H2O2浓度随时间的变化如图所示。下列说法正确的是( )

A. 图甲表明,其他条件相同时,H2O2浓度越小,其分解速率越快
B. 图乙表明,其他条件相同时,溶液PH 越小,H2O2分解速率越快
C. 图丙表明,少量Mn2+存在时,溶液碱性越强,H2O2分解速率越快
D. 图丙和图丁表明,碱性溶液中,Mn2+对H2O2分解速率的影响大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知下列十种物质:
①H2O ②Cu ③NO ④SiO2 ⑤稀硫酸 ⑥氢氧化钡 ⑦饱和FeCl3溶液 ⑧氨水 ⑨稀硝酸 ⑩硫酸铝
根据上述提供的物质,回答下列问题:
(1)属于纯净物的是__________,属于电解质的是__________。(填数字序号)
(2)发生中和反应的离子方程式为H++OH-===H2O,该离子反应对应的化学方程式有__________________________________。
(3)实验室制备少量Fe(OH)3胶体所用到的物质有________(填数字序号),发生反应的离子方程式为_________________________。
(4)实验室配制0.5 mol·L-1 245 mL⑩的溶液,需要用到的玻璃仪器有玻璃棒、烧杯、胶头滴管、________,需要用托盘天平称取溶质的质量为________g,从配制好的溶液中取出100 mL,其中含有的SO42—数目为________(设NA为阿伏加德罗常数的值)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列是几种原子的基态电子排布,电负性最大的原子是
A. 1s22s22p63s23p2 B. 1s22s22p63s23p3 C. 1s22s22p63s23p64s2 D. 1s22s22p4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上有一种方法是用CO2来生产燃料甲醇。为探究反应原理,现进行如下实验,在体积为l L的密闭容器中,充入lmol CO2和3mol H2,一定条件下发生反应:CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g) △H = —49.0 kJ·mol-1。
CH3OH(g)+H2O(g) △H = —49.0 kJ·mol-1。
测得CO2和CH3OH(g)的浓度随时间变化如图所示。
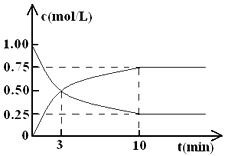
(1)从反应开始到平衡,氢气的平均反应速率v( H2 )= ________ ,CO2的转化率=________。
(2)该反应的平衡常数表达式k=__________ 。
(3)下列措施中能使n(CH3OH)/n(CO2)增大的是_________________ (填编号)。
A.将H2O(g)从体系中分离B.充入He(g),使体系压强增大
C.升高温度 D.再充入lmolCO2和3molH2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com