
| A、原子半径:C1>S>P |
| B、热稳定性:HC1>H2S>H2O |
| C、还原性:I->Br->C1- |
| D、碱性:NaOH>Mg(OH)2>Ca(OH)2 |


 优等生题库系列答案
优等生题库系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、苯、溴水、铁粉混合制成溴苯 |
| B、加浓溴水,然后过滤可除去苯中少量苯酚 |
| C、用高锰酸钾酸性溶液来区别甲烷和乙烯 |
| D、可用水来鉴别苯跟四氯化碳 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、S2-1s22s22p63s23p4 |
| B、F1s22s22p5 |
| C、K+1s22s22p63s23p6 |
| D、Ar1s22s22p63s23p6 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、0.25mol/L |
| B、18.4mol/L |
| C、1.84mol/L |
| D、1.0mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:
 已知常温时CH3COOH的电离平衡常数为K.该温度下向20mL 0.1mol?L-1CH3COOH溶液中逐滴加入0.1mol?L-1NaOH溶液,其pH变化曲线如图所示(忽略温度变化).下列说法中错误的是( )
已知常温时CH3COOH的电离平衡常数为K.该温度下向20mL 0.1mol?L-1CH3COOH溶液中逐滴加入0.1mol?L-1NaOH溶液,其pH变化曲线如图所示(忽略温度变化).下列说法中错误的是( )| A、b点表示的溶液中c(CH3COO-)>c(Na+) | ||
| B、c点表示CH3COOH和NaOH恰好反应完全 | ||
| C、a、b点间一定存在c(CH3COO-)>c(Na+)>c(H+)>c(OH-) | ||
D、b、d点表示的溶液中
|
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①③⑤ | B、①②④ |
| C、③④⑤ | D、①④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:
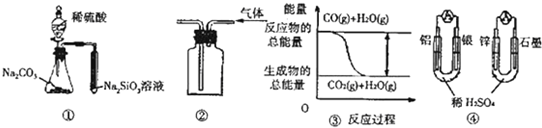
| A、用图 ①所示实验可比较硫、碳、硅三种元素的非金属性强弱 |
| B、用图 ②所示实验装置排空气法收集CO2气体 |
| C、图 ③表示CO(g)+H2O(g)?CO2(g)+H2(g)为吸热反应 |
| D、图 ④两个装置中通过导线的电子数相同时,消耗负极材料的物质的量也相同 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com