
| ||
| 2min |
(
| ||||
(
|
| 1 |
| 27 |
| 1 |
| 27 |


科目:高中化学 来源: 题型:
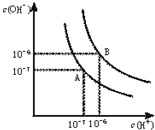 (1)水的电离平衡曲线如图所示.若以A点表示25℃时水在电离平衡时的离子浓度,当温度升到100℃时,水的电离平衡状态到B点,则此时水的离子积从
(1)水的电离平衡曲线如图所示.若以A点表示25℃时水在电离平衡时的离子浓度,当温度升到100℃时,水的电离平衡状态到B点,则此时水的离子积从查看答案和解析>>
科目:高中化学 来源: 题型:
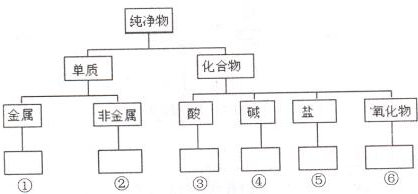 在化学研究中,化学家常常先对物质进行分类,以便对同类物质的组成和性能进行深入的研究,请你将下列物质N2、HClO、CuO、KOH、NaHCO3、Fe3O4、Mg、S的正确分类填入相应的方框内:
在化学研究中,化学家常常先对物质进行分类,以便对同类物质的组成和性能进行深入的研究,请你将下列物质N2、HClO、CuO、KOH、NaHCO3、Fe3O4、Mg、S的正确分类填入相应的方框内:查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
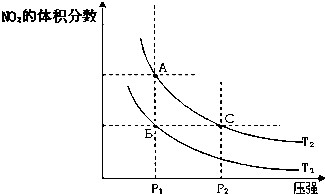
| 时间(s) | 0 | 20 | 40 | 60 | 80 |
| n(NO2)/mol | 0.40 | n1 | 0.26 | n3 | n4 |
| n(N2O4)/mol | 0.00 | 0.05 | n2 | 0.08 | 0.08 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 1 |
| 2 |
| 1 |
| 2 |
| A、9.1% | B、10.0% |
| C、28.6% | D、71.5% |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、乙醇分子中含有羟基,能发生氧化反应、取代反应、加成反应 |
| B、乙酸分子中含有羧基,可与NaHCO3溶液反应生成CO2 |
| C、甲烷和氯气反应生成一氯甲烷,与苯和硝酸反应生成硝基苯的反应类型相同 |
| D、乙烯和苯都能发生加成反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、HCl=H++Cl- | ||
B、Al(NO3)3=Al3++3NO
| ||
C、Na2CO3=2Na++CO
| ||
D、MgCl2=Mg2++Cl
|
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、原子半径:C1>S>P |
| B、热稳定性:HC1>H2S>H2O |
| C、还原性:I->Br->C1- |
| D、碱性:NaOH>Mg(OH)2>Ca(OH)2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com