
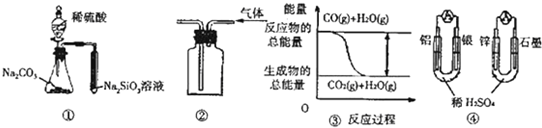
| A、用图 ①所示实验可比较硫、碳、硅三种元素的非金属性强弱 |
| B、用图 ②所示实验装置排空气法收集CO2气体 |
| C、图 ③表示CO(g)+H2O(g)?CO2(g)+H2(g)为吸热反应 |
| D、图 ④两个装置中通过导线的电子数相同时,消耗负极材料的物质的量也相同 |


科目:高中化学 来源: 题型:
| A、原子半径:C1>S>P |
| B、热稳定性:HC1>H2S>H2O |
| C、还原性:I->Br->C1- |
| D、碱性:NaOH>Mg(OH)2>Ca(OH)2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、114号元素的质量数为114 |
| B、114号元素是过渡元素 |
| C、114号元素是非金属元素 |
| D、114号元素原子最外层有4个电子 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①②⑤ | B、②④ | C、①③⑤ | D、② |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Na+ H+ HCO3- Cl- |
| B、K+ Ca2+ HCO3- OH- |
| C、Na+ K+ CO32- Cl- |
| D、Na+ K+ HCO3-CO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:
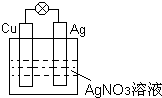 I.①如图所示,负极材料是
I.①如图所示,负极材料是查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com