
����Ŀ��X��Y��Z��W ������ԭ��������������Ķ�����Ԫ�أ�W �������������� X ��������������1����X��Y��ZΪͬһ����Ԫ�أ�X��Y��Z���һ�ֻ�����(ZXY)2 �Ľṹʽ��ͼ��ʾ������˵���������
![]()
A.������ WY �����õ����ȳ������
B.Y���������Ӧ��ˮ�������������
C.Y�ļ��⻯��ķе�һ������ Z
D.������(ZXY)2 ������ԭ�Ӿ����� 8 �����ȶ��ṹ
���𰸡�C
��������
X��Y��Z��W ������ԭ��������������Ķ�����Ԫ�أ�(ZXY)2 �Ľṹʽ�У�X����4�Ե��ӣ�ӦΪC��Si��W ��������������X��������������1������ԭ������W��X�����ԣ�Wֻ��ΪAl����XΪC��X��Y��ZΪͬһ����Ԫ�أ�(ZXY)2 �Ľṹʽ��Z����2�Ե��ӣ�Y����3�Ե��ӣ���ZӦΪO��YΪN����֮��X��Y��Z��W�ֱ�ΪC��N��O��Al�����ڴ˻����϶Ը�ѡ�������жϡ�
A. ���ݷ�����֪�������� WY��AlN��AlN��ԭ�Ӿ��壬�۵�ܸߣ����ȳ����Aѡ����ȷ��
B. Y���������Ӧ��ˮ�����У�HNO3��ǿ�ᣬHNO2�����ᣬBѡ����ȷ��
C. Y�ļ��⻯����NH3�������������壻Z�ļ��⻯����H2O����������Һ�壬���ԣ��е�H2O��NH3��Cѡ�����
D. ������(ZXY)2��(OCN)2������ʽ�ɱ�ʾΪ��![]() ������������ԭ��ͨ�����õ��Ӿ��ﵽ8�����ȶ��ṹ��Dѡ����ȷ��
������������ԭ��ͨ�����õ��Ӿ��ﵽ8�����ȶ��ṹ��Dѡ����ȷ��
��ѡC��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ָ����Ӧ�����ӷ���ʽ��ȷ����(����)
A. ��������ˮ��Cl2+H2O2H++Cl��+ClO��
B. ��FeSO4��Һ�м���H2SO4�ữ��KMnO4��Һ��5Fe2++MnO4��+8H+�T5Fe3++Mn2++4H2O
C. ����������ʯ��ˮ�м���������NaHCO3��Һ��Ca2++OH��+HCO3���TCaCO3��+H2O
D. ��ͭ���缫���NaCl��Һ��2Cl��+2H2O![]() H2��+Cl2��+2OH��
H2��+Cl2��+2OH��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ȡij������Ʒ��������ʵ�飺
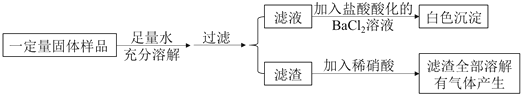
����ʵ�����ù�����Ʒ�ijɷֿ�����
A.Na2CO3��AgNO3��KNO3B.K2SO4��Ba(OH)2��Na2CO3
C.K2CO3��NaCl��Ba(NO3)2D.K2SO4��MgCl2��NaOH
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ڳ����ʵ�ʵ������У�Ϊ�˽���Һ�е�������ȫȥ����ͨ�����������ij������Լ���ijУ��ѧ����С��Ϊ�˳�ȥ�����к�������Na2SO4��MgCl2�����������ʵ�鲽�裺
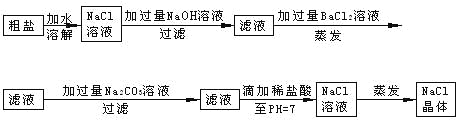
�Լ�Ҫ˵����
��1���������BaCl2����Һ��ԭ��___________________��
��2���������Na2CO3����Һ��ԭ��_________________________��
��3���μ�ϡ����ֱ��pH=7��Ŀ����_____________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ԭ���������������A��B��C��D��E��F����Ԫ�ء�����A�Ļ�̬ԭ����3����ͬ�ܼ������ܼ��еĵ�������ȣ�C�Ļ�̬ԭ��2p�ܼ��ϵ�δ�ɶԵ�������Aԭ�ӵ���ͬ��DΪ������������ԭ�Ӱ뾶��������Ԫ�أ�E��F��Cλ��ͬһ���壬F���ڵ�һ�������ڡ�
��1��![]() ԭ�ӻ�̬ʱ��Χ���ӹ����ʾʽΪ______��
ԭ�ӻ�̬ʱ��Χ���ӹ����ʾʽΪ______��
��2����A��B��C�γɵ�����![]() ��
��![]() ��Ϊ�ȵ����壬��
��Ϊ�ȵ����壬��![]() �ĽṹʽΪ______��
�ĽṹʽΪ______��
��3����֪����ԭ�ӷ����У���ԭ�Ӷ���ͬһƽ��������Щԭ�����ƽ�е�p�������p���ӿ��ڶ��ԭ�Ӽ��˶����γ�������![]() ����
����![]() ���
���![]() ��
��![]() ����
����![]() ������
������![]() ��ʾ������m��n�ֱ���������γɴ�
��ʾ������m��n�ֱ���������γɴ�![]() ���ĵ�������ԭ�Ӹ������籽�����д�
���ĵ�������ԭ�Ӹ������籽�����д�![]() ����ʾΪ
����ʾΪ![]()
�����������������![]() ��������______��
��������______��
![]()
![]()
��![]() �����д�
�����д�![]() �����Ա�ʾΪ______��
�����Ա�ʾΪ______��
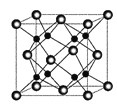
��4��![]() ��D�ܹ��γɻ�����X���侧���ṹ��ͼ��ʾ����������
��D�ܹ��γɻ�����X���侧���ṹ��ͼ��ʾ����������![]() ��������Cԭ�ӵ���λ��Ϊ______����ʽ���㾧��X���ܶ�______
��������Cԭ�ӵ���λ��Ϊ______����ʽ���㾧��X���ܶ�______![]() ��
��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���±�ΪԪ�����ڱ���һ���֣� �ش��������⡣
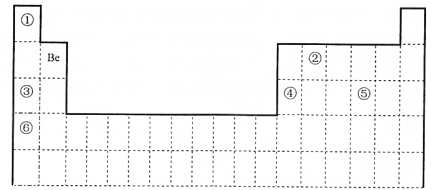
(1)�ҹ���ѧ�Ҳ��á�������귨�������������ˡ����䡣10Be ��9Be______________
a����ͬһ�ֺ��� b��������ͬ�������� c����Ϊͬ�������� d����Ϊͬλ��
(2)Ԫ�آٺ͢ڿ��γɶ��ֻ��������ģ�ͱ�ʾ�ķ����У��������ɢٺ͢��γɵ���_______(�����)��
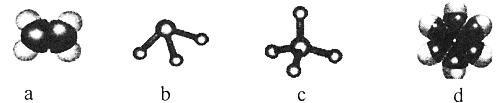
(3)Ԫ�آ�~���У���������ǿ����___(��Ԫ�ط���)���ڵĵ��ʺ͢ݵ�����������Ӧˮ�����Ũ��Һ��Ӧ�Ļ�ѧ����ʽΪ______________��
(4)��(53I) ������������Ԫ��֮һ��
�ٵ�(53I) �����ڱ��е�λ����______
��CI-��Br-��I-�Ļ�ԭ���ɴ�С��˳��Ϊ_______��
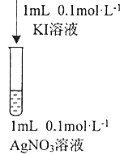
��������ʾ: Ag+��I-�ᷢ��������ԭ��Ӧ�������ֵ��ʣ���Ӧ�����ӷ���ʽΪ_______��ijͬѧ��ͼʵ����֤������Ӧ���۲쵽����Һ��Ϻ��������ֻ�ɫ���ǣ��ټ��������Һ��������������������������Ŀ���ԭ��:________________
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��A��B��C��DΪԭ�������������������Ԫ����A2-��B+������ͬ�ĵ��ӹ��ͣ�C�� DΪͬ����Ԫ����C�������������������������3����DԪ���������һ��δ�ɶԵ��ӡ��ش��������⣺
(1)����Ԫ���е縺��������______(��Ԫ�ط���)������Cԭ�ӵĺ�������Ų�ʽΪ__________��
(2)����A������ͬ�������壬���зе�ߵ���_____(�����ʽ)��ԭ����_______��
(3)C��D��Ӧ��������ɱ�Ϊ1��3�Ļ�����E�� E�����幹��Ϊ______������ԭ�ӵ��ӻ��������Ϊ______��
(4)������D2A�����幹��Ϊ___������ԭ�ӵļ۲���Ӷ���Ϊ______������D��ʪ���Na2CO3��Ӧ���Ʊ�D2A���仯ѧ����ʽΪ_________��
(5)A��B�ܹ��γɻ�����F���侧���ṹ��ͼ��ʾ������������a��0.566nm��������A ԭ�ӵ���λ��Ϊ_________����ʽ���㾧��F���ܶ�(g.cm-3)_____��

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ȼ��1g��Ȳ��C2H2�����ɶ�����̼��Һ̬ˮ���ų�����50kJ, ����һ��Ӧ���Ȼ�ѧ��Ӧ����ʽΪ�� ��
A. 2C2H2��g��+ 5O2��g�� �T4CO2��g��+ 2H2O��l�� ��H= +50kJ/mol
B. C2H2��g��+ 5/2O2��g���T2CO2��g��+ H2O��l�� ��H= +1300kJ/mol
C. 2C2H2+ 5O2�T4CO2+ 2H2O ��H=-2600kJ
D. 2C2H2��g��+ 5O2��g���T4CO2��g��+ 2H2O��l�� ��H=-2600kJ/mol
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����1��![]() ������ʳ�εĿ������������
������ʳ�εĿ������������![]() ��ֽ�����
��ֽ�����![]() ��KCN��
��KCN��![]() ��
��![]() C��C�����ʣ������������漰�ļ���Ԫ�صĵ�һ�������ɴ�С��˳��Ϊ______��
C��C�����ʣ������������漰�ļ���Ԫ�صĵ�һ�������ɴ�С��˳��Ϊ______��![]() �У���ԭ�Ӳ��Dz���
�У���ԭ�Ӳ��Dz���![]() �ӻ���������______��
�ӻ���������______��
��2��![]() ��̬Ϊ������ʱ��������Sԭ�ӵ��ӻ��������Ϊ______�����ӵ����幹��Ϊ______��
��̬Ϊ������ʱ��������Sԭ�ӵ��ӻ��������Ϊ______�����ӵ����幹��Ϊ______��![]() �������廷״�ṹ��ͼ1��ʾ���ýṹ��
�������廷״�ṹ��ͼ1��ʾ���ýṹ��![]() ������a��b���࣬b�ļ�������a�ļ����Ŀ���ԭ��Ϊ______��
������a��b���࣬b�ļ�������a�ļ����Ŀ���ԭ��Ϊ______��

��3����֪����ԭ�ӷ����У���ԭ�Ӷ���ͬһƽ��������Щԭ�����ƽ�е�p�������p���ӿ��ڶ��ԭ�Ӽ��˶����γ�������![]() ����
����![]() ���
���![]() ��
��![]() ����
����![]() ������
������![]() ��ʾ������m��n�ֱ���������γɴ�
��ʾ������m��n�ֱ���������γɴ�![]() ���ĵ�������ԭ�Ӹ������籽�����д�
���ĵ�������ԭ�Ӹ������籽�����д�![]() ����ʾΪ
����ʾΪ![]() ��
��
�����������������![]() ��������______��
��������______��
A.![]()
![]()
![]()
![]()
��![]() �����д�
�����д�![]() �����Ա�ʾΪ______��
�����Ա�ʾΪ______��
��4�����������ֵ��ʵĶѻ���ʽ����ͼ�ֱ���ͼ2��ͼ3��ʾ����������ԭ�ӵĿռ�������Ϊ______![]() �ú�
�ú�![]() ��ʽ�ӱ�ʾ
��ʽ�ӱ�ʾ![]() ��
��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com