
【题目】下列设备工作时,将化学能转化为热能的是
A. 硅太阳能电池 B. 铅蓄电池 C. 燃气灶 D. 电烤箱
 灵星计算小达人系列答案
灵星计算小达人系列答案 孟建平错题本系列答案
孟建平错题本系列答案科目:高中化学 来源: 题型:
【题目】学习了氯气的相关知识之后,某化学兴趣小组用下图所示仪器及试剂,进行了实验室制取氯气实验,并探究其相关化学性质。
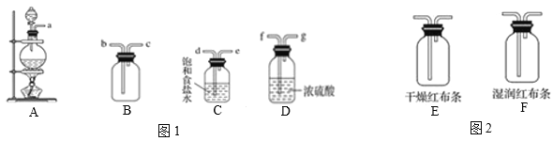
(1)若A中药品为MnO2和浓盐酸,请写出实验原理_____________________(用化学方程式表示)。
(2)将图1各仪器按先后顺序连接起来___________(用导管口处的字母表示)。
(3)C装置的作用_____________________。
(4)验满的方法为_____________________。
(5)把Cl2分别通入图2装置E和F,可以观察到什么现象______________________________;实验目的:_____________________。
(6)实验室除了可以用MnO2和浓盐酸制取Cl2,还可以用哪些药品与浓盐酸反应制取_______________________(用化学方程式表示其反应原理)
(7)该实验有哪些不足之处_____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)利用VSEPR推断分子或离子的空间构型。
PO![]() __________;CS2____________;AlBr3(共价分子)__________。
__________;CS2____________;AlBr3(共价分子)__________。
(2)有两种活性反应中间体粒子,它们的粒子中均含有1个碳原子和3个氢原子。请依据下面给出的这两种粒子的球棍模型,写出相应的化学式:
 ______;
______;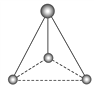 ______。
______。
(3)按要求写出第二周期非金属元素构成的中性分子的化学式。
平面三角形分子________,三角锥形分子________,四面体形分子________。
(4)为了解释和预测分子的空间构型,科学家在归纳了许多已知的分子空间构型的基础上,提出了一种十分简单的理论模型——价层电子对互斥模型。这种模型把分子分成两类:一类是____________________;另一类是____________________。BF3和NF3都是四个原子的分子,BF3的中心原子是________,NF3的中心原子是________;BF3分子的立体构型是平面三角形而NF3分子的立体构型是三角锥形的原因是____________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】《本草纲目》记载了烧酒的制造工艺:“凡酸坏之酒,皆可蒸烧”, “以烧酒复烧二次……价值数倍也”。其方法与分离下列物质的实验方法原理上相同的是
A.四氯化碳和水
B.硝酸钾和氯化钠
C.乙酸乙酯(沸点77 ℃)和乙酸(118 ℃)(两者互溶)
D.食盐水和泥沙
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应曾用于检测司机是否酒后驾驶:
2Cr2O![]() +3CH3CH2OH+16H++13H2O―→4[Cr(H2O)6]3++3CH3COOH
+3CH3CH2OH+16H++13H2O―→4[Cr(H2O)6]3++3CH3COOH
(1)Cr3+基态核外电子排布式为________;配合物[Cr(H2O)6]3+中,与Cr3+形成配位键的原子是______(填元素符号)。
(2)CH3COOH中C原子轨道杂化类型分别为____________;1 mol CH3COOH分子中含有σ键的数目为__________。
(3)与H2O互为等电子体的一种阳离子为________(填化学式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知A、B、C、D、E五种元素的原子序数依次增大,其中A原子所处的周期数、族序数都与其原子序数相等;B原子核外电子有6种不同的运动状态,s轨道电子数是p轨道电子数的两倍;D原子L层上有2对成对电子;E+离子核外有3层电子且M层3d轨道电子全充满。请回答下列问题:
(1)E元素基态原子的电子排布式为________。
(2)B、C、D三种元素的第一电离能数值由小到大的顺序为________(填元素符号),其原因是________________________________________________________________________。
(3)D元素与氟元素相比,电负性:D________(填“>”“=”或“<”)F,下列表述中能证明这一事实的是______(填选项序号)。
A.常温下氟气的颜色比D单质的颜色深 B.氟气与D的氢化物剧烈反应,产生D的单质
C.氟与D形成的化合物中D元素呈正价态 D.比较两元素的单质与氢气化合时得电子的数目
(4)由A、C两元素可形成化合物CA5含有的化学键类型为________。
(5)B2A4是重要的石油化工原料,B2A4的结构式为________。B2A4通过聚合反应可以生成一种有机高分子化合物,反应方程式为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】最近,国际上提出的“绿色化学”是指化学工业生产中( )。
A.对废水、废气、废渣进行严格处理
B.化学生产中不排放任何有害物质
C.化工厂及周围种草、种树、种花,使工厂成为花园式工厂
D.以绿色植物为原料,以生物催化剂实现化工生产过程的化学
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某100 mL溶液中含H2SO4 0.50 mol,加入下列物质,溶液导电性增强的是( )
A.0.50 mol Ba(OH)2B.100 mL水
C.0.50 mol 酒精D.0.50 mol Na2SO4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素W、X、Y、Z的原子序数依次增大,这些元素组成的单质和化合物转化关系如下图所示。其中C是淡黄色固体,B和E的水溶液均具有漂白性。下列说法不正确的是

A. 简单离子半径:Y>Z>X B. 沸点:D
C. 气态氢化物稳定性:Z>Y D. 0.1mol·L-1A溶液中:c(H+)>c(HY-)>c(Y2-)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com